총 43건
-
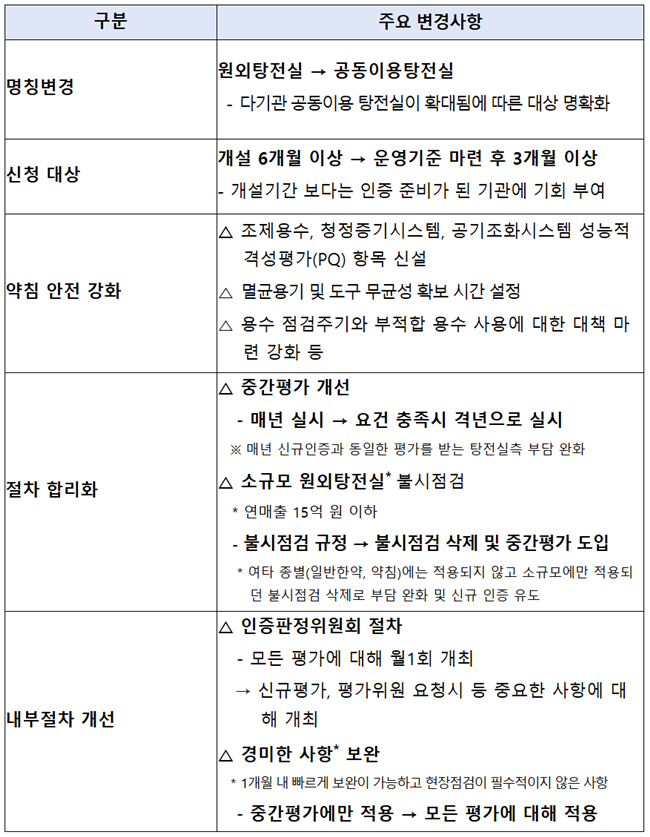 원외탕전실→공동이용탕전실 변경...약침조제 평가 강화[데일리팜=정흥준 기자] 복지부가 내년부터 원외탕전실 명칭을 공동이용탕전실로 변경하고 약침조제 평가기준을 강화한다.또 매년 실시하던 중간평가를 요건 충족 시 격년으로 실시해 부담을 완화하고, 소규모 탕전실 불시점검도 삭제한다.복지부는 오늘(21일) 원외탕전실 3주기 평가인증 기준안 공청회를 거쳐 최종 개정안을 확정할 계획이다.탕전실 평가인증제도는 지난 2018년 1주기 인증기준 도입 후 2022년 2주기 기준으로 개정한 바 있다. 이번에 3주기 인증기준이 개정되면 내년부터 2029년까지 적용될 예정이다. 복지부는 약침 조제 평가기준을 강화하고, 행정 절차는 합리화해 인증 부담을 낮추는 것이 주 개정 내용이라고 설명했다.다기관 공동이용 탕전실이 확대됨에 따라 명칭을 원외탕전실에서 공동이용탕전실로 바꾼다.신청대상은 ‘개설 6개월 이상’에서 운영기준 마련 후 3개월 이상으로 바꿔 인증 준비가 된 기관에 기회를 부여한다.약침안전 강화를 위해 조제용수, 청정증기시스템, 공기조화시스템 성능적격성평가 항목을 신설했다. 멸균용기 및 도구 무균성 확보 시간도 설정했다. 용수 점검주기와 부적합 용수 사용에 대한 대책 마련 강화 등도 달라진다.전국 원외탕전실 127곳 중 22개소가 인증을 받았다. 그 중 일반한약이 15곳, 약침이 7곳이다.정영훈 한의약정책관은 “이번 공청회를 통해 전문가와 현장의 의견을 적극 수렴해 한약조제시설 위생, 안전 관리체계를 강화하겠다. 또 조제한약의 안전 성과와 품질 일관성을 확보해 한약 신뢰도를 제고하고 나아가 국민건강증진에 기여하도록 노력하겠다”라고 밝혔다.2025-11-21 11:29:27정흥준
원외탕전실→공동이용탕전실 변경...약침조제 평가 강화[데일리팜=정흥준 기자] 복지부가 내년부터 원외탕전실 명칭을 공동이용탕전실로 변경하고 약침조제 평가기준을 강화한다.또 매년 실시하던 중간평가를 요건 충족 시 격년으로 실시해 부담을 완화하고, 소규모 탕전실 불시점검도 삭제한다.복지부는 오늘(21일) 원외탕전실 3주기 평가인증 기준안 공청회를 거쳐 최종 개정안을 확정할 계획이다.탕전실 평가인증제도는 지난 2018년 1주기 인증기준 도입 후 2022년 2주기 기준으로 개정한 바 있다. 이번에 3주기 인증기준이 개정되면 내년부터 2029년까지 적용될 예정이다. 복지부는 약침 조제 평가기준을 강화하고, 행정 절차는 합리화해 인증 부담을 낮추는 것이 주 개정 내용이라고 설명했다.다기관 공동이용 탕전실이 확대됨에 따라 명칭을 원외탕전실에서 공동이용탕전실로 바꾼다.신청대상은 ‘개설 6개월 이상’에서 운영기준 마련 후 3개월 이상으로 바꿔 인증 준비가 된 기관에 기회를 부여한다.약침안전 강화를 위해 조제용수, 청정증기시스템, 공기조화시스템 성능적격성평가 항목을 신설했다. 멸균용기 및 도구 무균성 확보 시간도 설정했다. 용수 점검주기와 부적합 용수 사용에 대한 대책 마련 강화 등도 달라진다.전국 원외탕전실 127곳 중 22개소가 인증을 받았다. 그 중 일반한약이 15곳, 약침이 7곳이다.정영훈 한의약정책관은 “이번 공청회를 통해 전문가와 현장의 의견을 적극 수렴해 한약조제시설 위생, 안전 관리체계를 강화하겠다. 또 조제한약의 안전 성과와 품질 일관성을 확보해 한약 신뢰도를 제고하고 나아가 국민건강증진에 기여하도록 노력하겠다”라고 밝혔다.2025-11-21 11:29:27정흥준 -
 "영리 비대면 플랫폼 도입한 캐나다·영국 재앙적 결과"[데일리팜=강혜경 기자] "새로운 기술을 도입한다는 명목으로 원격의료를 민간에 열어준 캐나다. 그 결과 1996년 이래 보편적 공공의료를 실현해 온 캐나다 의료는 이중 체계가 됐습니다. 부유층은 대기 줄을 건너뛰고 비싼 영리 부문의 의료를 이용할 수 있게 됐고, 공공 부문 대기 줄은 길어졌습니다. 돈 되는 곳으로 자원과 의사 인력이 몰리며 지역 공공클리닉은 운영이 중단되는 반면 원격 앱은 '2분 내 진료'를 약속하고 있습니다.전례 없던 과다 청구 문제도 불거졌습니다. 하루 321명의 환자를 진료했다며 연간 170만 달러(약 20억원)를 청구한 의사가 있었습니다. 플랫폼 기업이 환자 정보를 미국 기업에 한매하다 적발되기도 했습니다. 캐나다 보건의료 체계는 영리 플랫폼 도입으로 민영화의 길을 걷고 있습니다.영국(잉글랜드)에서는 바빌론(Babylon)이라는 회사가 원격의료 플랫폼을 2023년까지 운영했습니다. 바빌론은 국영의료시스템(NHS) 내에서 독립적인 진료소를 운영하면서 의사들을 고용해 원격의료를 했습니다. 비발론은 건강한 젊은 환자를 선별해 등록, 환자의 85% 이상이 20~39세였고 노인, 임산부, 치매 환자 같은 기저질환자는 '부적합' 대상자로 분류해 거부했습니다.영국은 의료기관이 환자 1인당 일정 비용을 받은 체계(인두제)인데, 큰 비용이 들지 않고 젊고 건강한 환자를 원격 클리닉이 다 끌어가면서 다른 NHS 국영 의료 클리닉들은 재정난을 겪게 되었습니다. 바빌론의 후신으로 사업을 이어가는 '이메드(eMed)'라는 플랫폼 기업은 NHS 진료를 제공하는 것처럼 정부 재정을 챙겨서는 GP(주치의) 진료당 59파운드(약 10만원)를 받는 유료 서비스로 유인해 영국 일차의료 부문의 영리화와 비용 상승을 주도하고 있습니다.미국 역시 원격 플랫폼이 난림하면서 불필요한 검사와 치료를 더 남발하게 만든다는 비판을 받고 있습니다. 의료인에게 진료 시간을 줄여 환자 수를 늘릴 것을 강요하고, 지키지 않는 의료진의 급여를 삭감하며 쫓아낸 사건 등이 알려져 있습니다. 다른 플랫폼은 그들이 투자한 약국의 수익을 높이기 위해 의료진에게 과다 약물 처방을 강요했습니다."이것이 모든 나라에서 문제 없이 활용된다는 원격의료 서비스의 실체입니다. 보건의료 학계에서 기업들이 원격의료 같은 디지털 기술을 확대한다는 명목으로 의료 시스템을 민영화하는 일관된 패턴이 발견된다는 평가를 하는 이유입니다. 국회가 면밀한 검토없이 이런 위험한 민영화 시스템을 도입해서는 절대 안 됩니다." 지난 9월 원격의료 법제화 중단 촉구 기자회견을 연 무상의료운동본부. 건강사회를위한약사회와 약사의미래를준비하는모임 등 30여개 단체가 속한 무상의료운동본부가 민간 영리 플랫폼 중심 원격의료 법제화에 반대입장을 밝혔다.27일 무상의료운동본부가 국회에 제출한 의견서에는 의료 부문을 지배·장악할 수 있는 플랫폼에 영리 기업 진입을 허용하는 것은 '심각한 의료민영화'라며, 실패한 민간 영리 플랫폼 중심의 시범사업을 중단하고 공공 플랫폼을 활용한 시범사업을 실시해야 한다는 주장이 담겨 있다.◆원격플랫폼 본질 '수익 위한 영리 기업'= 무상의료운동본부는 원격의료 플랫폼의 본질은 수익을 내려는 영리 기업으로, 현재는 적자를 감수하고 출혈 경쟁을 하며 이용자를 늘리는 데 집중하지만 법이 통과되고 충분한 이용자를 모으면 건당 중개 수수료를 받거나, 상단 노출을 위한 비용을 받는 등 수익 모델을 가질 것이 자명하다고 우려했다.결국 이는 과잉진료와 약물 남용 등으로 연계, 국민 건강과 생명은 물론 건보 재정에까지 악영향을 미칠 수밖에 없다는 주장이다.이들은 의료법이 개정되면 대기업이 본격 뛰어들 것이라고 전망했다. 특히 대기업 보험사들이 원격의료 플랫폼을 장악할 것이라는 게 이들의 설명이다.이미 KB손해보험 자회사인 KB헬스케어가 '올라케어'를 인수했으나, 굿닥에서 진료를 받으면 삼성생명 특정 보험상품 무료 가입이 가능한 방식의 공동 사업이 이뤄지고 있다는 것.본부는 "즉, 보험사가 지배 플랫폼을 소유·운영할 가능성이 높다. 이런 식으로 보험사가 의료기관을 지배·통제하는 구조가 바로 미국식 의료 모델"이라며 "미국식 의료 민영화인 HMO(민영보험사-의료기관 복합체) 구조가 한국에 도입되는 경로가 될 수 있다"고 지적했다.◆"커피 쿠폰 뿌려 비급여 약물 처방"= 무상의료운동본부는 원격의료가 '의료 취약 계층의 접근성 향상'을 명목으로 추진됐지만, 애초 의료 취약지와 고령층을 위한 사업이 아니라고 꼬집었다.일례로 약준모가 읍면 지역 거주자 502명을 대상으로 실시한 설문에 따르면, 60%는 스마트폰 앱 기반의 서비스 자체를 전혀 사용해 본 적 없었고 비대면 진료를 이용해 본 적 있는 사람은 전체의 약 5%, 60대 이상 응답자 중에서는 2.5%에 불과했다는 것.이들은 "플랫폼들이 시범사업 기간 동안 커피 쿠폰을 뿌려 손쉽게 비급여 약물을 처방받길 원하는 이들을 끌어모으는 데 혈안돼 있었을 뿐, 취약지 주민들은 애초 사업의 고려 대상이 아니었다"며 "오히려 영리 플랫폼이 활성화돼 상업 영역이 비대해지면 지역에서 응급환자·중환자 진료나 분만을 담당할 의사는 더욱 줄어들 것"이라고 우려했다.이어 '디지털 신산업 육성' 명목의 플랫폼 살리기 사업은 전혀 새롭고 혁신적인 기술이 아니라고 강조했다.유사한 수십 개의 기업이 난립하는 것 역시 같은 이유라는 것.본부는 "민간 영리 플랫폼은 수익을 내지 않는 상황에서도 SNS 전문약 불법 광고 등으로 약물 남용과 과잉의료를 부추겼고, 이는 부당 청구를 유발했다. 또 원하는 약 처방받기로 환자가 원하는 탈모, 다이어트 등 특정 전문약을 선택할 수 있게 하는 등 약물 쇼핑을 부추겼으며 처방후기를 허위로 작성해 달라는 뒷광고 요청 등 불법적 상업행위를 유발해 왔다"며 "정부는 영리 플랫폼을 금지시키고 정부가 공공 플랫폼을 구축해 운영해야 할 것"이라고 주문했다.한편 정부 역시 22일 의료계와 약계, 플랫폼 업계 등이 참석한 가운데 전문가 자문단 회의를 개최했다.2025-10-27 14:57:43강혜경
"영리 비대면 플랫폼 도입한 캐나다·영국 재앙적 결과"[데일리팜=강혜경 기자] "새로운 기술을 도입한다는 명목으로 원격의료를 민간에 열어준 캐나다. 그 결과 1996년 이래 보편적 공공의료를 실현해 온 캐나다 의료는 이중 체계가 됐습니다. 부유층은 대기 줄을 건너뛰고 비싼 영리 부문의 의료를 이용할 수 있게 됐고, 공공 부문 대기 줄은 길어졌습니다. 돈 되는 곳으로 자원과 의사 인력이 몰리며 지역 공공클리닉은 운영이 중단되는 반면 원격 앱은 '2분 내 진료'를 약속하고 있습니다.전례 없던 과다 청구 문제도 불거졌습니다. 하루 321명의 환자를 진료했다며 연간 170만 달러(약 20억원)를 청구한 의사가 있었습니다. 플랫폼 기업이 환자 정보를 미국 기업에 한매하다 적발되기도 했습니다. 캐나다 보건의료 체계는 영리 플랫폼 도입으로 민영화의 길을 걷고 있습니다.영국(잉글랜드)에서는 바빌론(Babylon)이라는 회사가 원격의료 플랫폼을 2023년까지 운영했습니다. 바빌론은 국영의료시스템(NHS) 내에서 독립적인 진료소를 운영하면서 의사들을 고용해 원격의료를 했습니다. 비발론은 건강한 젊은 환자를 선별해 등록, 환자의 85% 이상이 20~39세였고 노인, 임산부, 치매 환자 같은 기저질환자는 '부적합' 대상자로 분류해 거부했습니다.영국은 의료기관이 환자 1인당 일정 비용을 받은 체계(인두제)인데, 큰 비용이 들지 않고 젊고 건강한 환자를 원격 클리닉이 다 끌어가면서 다른 NHS 국영 의료 클리닉들은 재정난을 겪게 되었습니다. 바빌론의 후신으로 사업을 이어가는 '이메드(eMed)'라는 플랫폼 기업은 NHS 진료를 제공하는 것처럼 정부 재정을 챙겨서는 GP(주치의) 진료당 59파운드(약 10만원)를 받는 유료 서비스로 유인해 영국 일차의료 부문의 영리화와 비용 상승을 주도하고 있습니다.미국 역시 원격 플랫폼이 난림하면서 불필요한 검사와 치료를 더 남발하게 만든다는 비판을 받고 있습니다. 의료인에게 진료 시간을 줄여 환자 수를 늘릴 것을 강요하고, 지키지 않는 의료진의 급여를 삭감하며 쫓아낸 사건 등이 알려져 있습니다. 다른 플랫폼은 그들이 투자한 약국의 수익을 높이기 위해 의료진에게 과다 약물 처방을 강요했습니다."이것이 모든 나라에서 문제 없이 활용된다는 원격의료 서비스의 실체입니다. 보건의료 학계에서 기업들이 원격의료 같은 디지털 기술을 확대한다는 명목으로 의료 시스템을 민영화하는 일관된 패턴이 발견된다는 평가를 하는 이유입니다. 국회가 면밀한 검토없이 이런 위험한 민영화 시스템을 도입해서는 절대 안 됩니다." 지난 9월 원격의료 법제화 중단 촉구 기자회견을 연 무상의료운동본부. 건강사회를위한약사회와 약사의미래를준비하는모임 등 30여개 단체가 속한 무상의료운동본부가 민간 영리 플랫폼 중심 원격의료 법제화에 반대입장을 밝혔다.27일 무상의료운동본부가 국회에 제출한 의견서에는 의료 부문을 지배·장악할 수 있는 플랫폼에 영리 기업 진입을 허용하는 것은 '심각한 의료민영화'라며, 실패한 민간 영리 플랫폼 중심의 시범사업을 중단하고 공공 플랫폼을 활용한 시범사업을 실시해야 한다는 주장이 담겨 있다.◆원격플랫폼 본질 '수익 위한 영리 기업'= 무상의료운동본부는 원격의료 플랫폼의 본질은 수익을 내려는 영리 기업으로, 현재는 적자를 감수하고 출혈 경쟁을 하며 이용자를 늘리는 데 집중하지만 법이 통과되고 충분한 이용자를 모으면 건당 중개 수수료를 받거나, 상단 노출을 위한 비용을 받는 등 수익 모델을 가질 것이 자명하다고 우려했다.결국 이는 과잉진료와 약물 남용 등으로 연계, 국민 건강과 생명은 물론 건보 재정에까지 악영향을 미칠 수밖에 없다는 주장이다.이들은 의료법이 개정되면 대기업이 본격 뛰어들 것이라고 전망했다. 특히 대기업 보험사들이 원격의료 플랫폼을 장악할 것이라는 게 이들의 설명이다.이미 KB손해보험 자회사인 KB헬스케어가 '올라케어'를 인수했으나, 굿닥에서 진료를 받으면 삼성생명 특정 보험상품 무료 가입이 가능한 방식의 공동 사업이 이뤄지고 있다는 것.본부는 "즉, 보험사가 지배 플랫폼을 소유·운영할 가능성이 높다. 이런 식으로 보험사가 의료기관을 지배·통제하는 구조가 바로 미국식 의료 모델"이라며 "미국식 의료 민영화인 HMO(민영보험사-의료기관 복합체) 구조가 한국에 도입되는 경로가 될 수 있다"고 지적했다.◆"커피 쿠폰 뿌려 비급여 약물 처방"= 무상의료운동본부는 원격의료가 '의료 취약 계층의 접근성 향상'을 명목으로 추진됐지만, 애초 의료 취약지와 고령층을 위한 사업이 아니라고 꼬집었다.일례로 약준모가 읍면 지역 거주자 502명을 대상으로 실시한 설문에 따르면, 60%는 스마트폰 앱 기반의 서비스 자체를 전혀 사용해 본 적 없었고 비대면 진료를 이용해 본 적 있는 사람은 전체의 약 5%, 60대 이상 응답자 중에서는 2.5%에 불과했다는 것.이들은 "플랫폼들이 시범사업 기간 동안 커피 쿠폰을 뿌려 손쉽게 비급여 약물을 처방받길 원하는 이들을 끌어모으는 데 혈안돼 있었을 뿐, 취약지 주민들은 애초 사업의 고려 대상이 아니었다"며 "오히려 영리 플랫폼이 활성화돼 상업 영역이 비대해지면 지역에서 응급환자·중환자 진료나 분만을 담당할 의사는 더욱 줄어들 것"이라고 우려했다.이어 '디지털 신산업 육성' 명목의 플랫폼 살리기 사업은 전혀 새롭고 혁신적인 기술이 아니라고 강조했다.유사한 수십 개의 기업이 난립하는 것 역시 같은 이유라는 것.본부는 "민간 영리 플랫폼은 수익을 내지 않는 상황에서도 SNS 전문약 불법 광고 등으로 약물 남용과 과잉의료를 부추겼고, 이는 부당 청구를 유발했다. 또 원하는 약 처방받기로 환자가 원하는 탈모, 다이어트 등 특정 전문약을 선택할 수 있게 하는 등 약물 쇼핑을 부추겼으며 처방후기를 허위로 작성해 달라는 뒷광고 요청 등 불법적 상업행위를 유발해 왔다"며 "정부는 영리 플랫폼을 금지시키고 정부가 공공 플랫폼을 구축해 운영해야 할 것"이라고 주문했다.한편 정부 역시 22일 의료계와 약계, 플랫폼 업계 등이 참석한 가운데 전문가 자문단 회의를 개최했다.2025-10-27 14:57:43강혜경 -
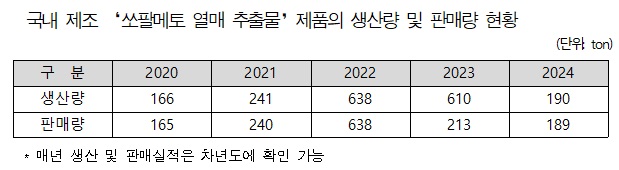 쏘팔메토 건기식 품질관리 강화…"생산·판매량 급감"[데일리팜=이정환 기자] 하위 법령 선진화 등 정부부처 간 협력 행정으로 쏘팔메토 열매 추출물을 원료로 만든 건강기능식품의 국내 생산량과 판매량이 급감한 것으로 집계됐다.국민들이 현행법이 규정한 정부 규격 위반 저품질 건기식 구매와 복용으로 경제적·건강적 손실을 입는 비율이 크게 줄어든 셈이다.식품의약품안전처가 농림수산식품부와 함께 소팔메토 건기식 품질관리를 한층 강화하는 행정을 편 게 생산량·판매량 급감 배경으로 이어졌다는 분석이 나온다.20일 더불어민주당 남인순 의원(서울송파구병·보건복지위)은 "식약처가 제출한 국내 제조 쏘팔메토 열매 추출물 제품의 생산량과 판매량 현황‘에 따르면, 쏘팔메토 생산량은 2020년 166톤에서 2022년 638톤으로 급증했다가, 지난해 196톤으로 급감했다. 쏘팔메토 판매량은 2020년 165톤에서 2022년 638톤으로 급증 후 2023년 생산량이 610톤이었는데도 판매량은 213톤으로 급감했고, 지난해 189톤을 판매했다"고 밝혔다. 식약처가 인정한 건기식 쏘팔메토 열매 추출물 기능성은 '전립선 건강' 유지에 도움을 줄 수 있음'이다.문제는 쏘팔메토는 원산지가 미국 플로리다, 조지아 등 남부지역으로 국내에서는 생산되지 않아 원료를 전량 수입하는데, 인도에서 원료를 수입하는 인도산 쏘팔메토 중 지표성분인 지방산과 로르산(lauric acid) 함량을 높이기 위해 값싼 팜유나 코코넛 오일 등 다른 원료를 첨가한 게 해외기관으로 부터 확인, 논란이 촉발된 점이다.남인순 의원은 식약처가 쏘팔메토 열매 추출물 품질관리 기준·규격을 개선하고, 농림부가 쏘팔메토 열매 추출물제품 원산지 표시 의무화 등 품질·안전관리를 강화한 이후 생산량과 판매량이 감소했다고 분석중이다.식약처는 쏘팔메토 열매 추출물 품질관리를 위해 총지방산과 식물스테롤의 규격·시험법을 신설하는 내용의 '건강기능식품의 기준 및 규격'고시를 개정했다.농림부는 식약처 요청에 따라 '농산물의 원산지표시 요령'고시를 개정해 농산물 가공품 중 건기식 원산지를 표시하는 대상 품목에 쏘팔메토 열매 추출물을 추가했다.특히 식약처는 쏘팔메토 열매 추출물의 기능성, 섭취 시 주의사항 등 온라인 카드뉴스를 홍보하고 쏘팔메토 관련 제품에 대한 오픈마켓 등 온라인 부당광고에 대해 집중점검을 실시했다. 그 결과 2023년 57건, 2024년 53건, 2025년 20건의 부당광고를 적발했고, 쏘팔메토 열매 추출물 기준& 8231;규격 개선 시행(’24.1) 후 건기식 쏘팔메토 열매 추출물 수입원료 총 93건을 검사한 결과 1건이 부적합으로 확인됐다.식약처는 부적합 내역에 대해 '지방산 50% 검출'로 총 지방산 80% 이상 규격에 못 미치고, '로르산 161mg/g 검출'로 표시량(220mg/g) 이상에 미치지 않았다고 밝혀, 쏘팔메토 지표성분인 지방산과 로르산이 건기식 규격에 미달했다고 밝혔다.2025-10-20 04:45:49이정환
쏘팔메토 건기식 품질관리 강화…"생산·판매량 급감"[데일리팜=이정환 기자] 하위 법령 선진화 등 정부부처 간 협력 행정으로 쏘팔메토 열매 추출물을 원료로 만든 건강기능식품의 국내 생산량과 판매량이 급감한 것으로 집계됐다.국민들이 현행법이 규정한 정부 규격 위반 저품질 건기식 구매와 복용으로 경제적·건강적 손실을 입는 비율이 크게 줄어든 셈이다.식품의약품안전처가 농림수산식품부와 함께 소팔메토 건기식 품질관리를 한층 강화하는 행정을 편 게 생산량·판매량 급감 배경으로 이어졌다는 분석이 나온다.20일 더불어민주당 남인순 의원(서울송파구병·보건복지위)은 "식약처가 제출한 국내 제조 쏘팔메토 열매 추출물 제품의 생산량과 판매량 현황‘에 따르면, 쏘팔메토 생산량은 2020년 166톤에서 2022년 638톤으로 급증했다가, 지난해 196톤으로 급감했다. 쏘팔메토 판매량은 2020년 165톤에서 2022년 638톤으로 급증 후 2023년 생산량이 610톤이었는데도 판매량은 213톤으로 급감했고, 지난해 189톤을 판매했다"고 밝혔다. 식약처가 인정한 건기식 쏘팔메토 열매 추출물 기능성은 '전립선 건강' 유지에 도움을 줄 수 있음'이다.문제는 쏘팔메토는 원산지가 미국 플로리다, 조지아 등 남부지역으로 국내에서는 생산되지 않아 원료를 전량 수입하는데, 인도에서 원료를 수입하는 인도산 쏘팔메토 중 지표성분인 지방산과 로르산(lauric acid) 함량을 높이기 위해 값싼 팜유나 코코넛 오일 등 다른 원료를 첨가한 게 해외기관으로 부터 확인, 논란이 촉발된 점이다.남인순 의원은 식약처가 쏘팔메토 열매 추출물 품질관리 기준·규격을 개선하고, 농림부가 쏘팔메토 열매 추출물제품 원산지 표시 의무화 등 품질·안전관리를 강화한 이후 생산량과 판매량이 감소했다고 분석중이다.식약처는 쏘팔메토 열매 추출물 품질관리를 위해 총지방산과 식물스테롤의 규격·시험법을 신설하는 내용의 '건강기능식품의 기준 및 규격'고시를 개정했다.농림부는 식약처 요청에 따라 '농산물의 원산지표시 요령'고시를 개정해 농산물 가공품 중 건기식 원산지를 표시하는 대상 품목에 쏘팔메토 열매 추출물을 추가했다.특히 식약처는 쏘팔메토 열매 추출물의 기능성, 섭취 시 주의사항 등 온라인 카드뉴스를 홍보하고 쏘팔메토 관련 제품에 대한 오픈마켓 등 온라인 부당광고에 대해 집중점검을 실시했다. 그 결과 2023년 57건, 2024년 53건, 2025년 20건의 부당광고를 적발했고, 쏘팔메토 열매 추출물 기준& 8231;규격 개선 시행(’24.1) 후 건기식 쏘팔메토 열매 추출물 수입원료 총 93건을 검사한 결과 1건이 부적합으로 확인됐다.식약처는 부적합 내역에 대해 '지방산 50% 검출'로 총 지방산 80% 이상 규격에 못 미치고, '로르산 161mg/g 검출'로 표시량(220mg/g) 이상에 미치지 않았다고 밝혀, 쏘팔메토 지표성분인 지방산과 로르산이 건기식 규격에 미달했다고 밝혔다.2025-10-20 04:45:49이정환 -
 미래바이오제약 제품 대거 회수...품질 부적합 우려[데일리팜=이탁순 기자] 미래바이오제약 12개 품목(일부 제조번호 한정)이 품질 부적합 우려로 회수 명령이 떨어졌다.이 회사는 지난 5월에도 같은 사유로 16개 제품(일부 제조번호 한정)에 회수 명령이 내려졌는데, 불과 4개월만에 대규모 회수 사례가 또 다시 발생한 것이다.품질관리가 제대로 되지 않았기 때문으로 풀이된다. 지난 9월 이 회사는 완제품에 대한 품질검사를 하지 않는 등의 이유로 행정처분도 받았다.식품의약품안전처는 지난 17일자로 하이드로핀정 등 미래바이오제약 12개 품목 일부 제조번호에 대해 회수 명령을 내렸다. 회수 사유는 유통제품의 품질 부적합이 우려된다는 것이다.이는 지난 9월 식약처가 품질관리 문제로 미래바이오제약을 처분한 것과 관련 있어 보인다.지난 9월 식약처는 완제품 품질검사 미실시(12개 품목), 제조기록서·시험일지 및 시험성적서 미작성(23개 품목), 검사명령 미이행(22개 품목) 등 사유로 관련 제품의 제조업무를 최대 6개월까지 정지시킨 바 있다.이번에 회수 명령이 떨어진 제품도 당시 식약처에 적발된 품목들이다.미래바이오제약은 지난 5월에도 16개 제품 일부 제조번호가 품질부적합 우려로 회수되는 등 품질관리가 제대로 이뤄지지 않고 있는 것으로 관측된다.이는 회사 경영 상황과 무관치 않아 보인다. 회사는 유동성 부족 위기를 타개하기 위해 생산시설 매각을 추진하고 있다. 매각 과정에서 제품 품질관리가 제대로 안 이뤄진 것 아니냐는 관측이 나온다.지난 6월 발행된 감사보고서에서 미래바이오제약은 2024년 당기 영업손실 11억2300만원, 보고기간 말 기준 유동부채 135억8000만원이 유동자산 27억9900만원을 초과하는 유동성 부족 상태에 있다는 진단을 받았다.미래바이오제약은 이에 대한 대응책으로 의약품 생산시설을 매각하고 신규 생산시설로의 이전을 통해 자금 확보 및 차입금 상환을 계획하고 있다고 감사보고서에서 전했다.하지만 감사인은 한정의견을 제시하면서 회사의 생산시설 매각 및 신규 생산시설 이전 계획의 실행 가능성, 관련 인허가의 적시 취득 여부, 생산 정상화 시점 및 수익성 확보 가능성 등에 대해 충분하고 적합한 감사증거를 입수하지 못했다고 전했다.미래바이오제약(미래제약)은 2002년 금강제약을 인수하면서 KGMP 시설 인증을 받았다. 현재 대표자는 김한석 씨다.경기도 안성 공단2로에 위치한 완제의약품 공장은 2027년 4월 24일까지 비무균-일반제제-내용고형제(정제, 캡슐제) 제형군에 대해 GMP 적합판정서가 발급돼 있다.2025-10-19 15:58:25이탁순
미래바이오제약 제품 대거 회수...품질 부적합 우려[데일리팜=이탁순 기자] 미래바이오제약 12개 품목(일부 제조번호 한정)이 품질 부적합 우려로 회수 명령이 떨어졌다.이 회사는 지난 5월에도 같은 사유로 16개 제품(일부 제조번호 한정)에 회수 명령이 내려졌는데, 불과 4개월만에 대규모 회수 사례가 또 다시 발생한 것이다.품질관리가 제대로 되지 않았기 때문으로 풀이된다. 지난 9월 이 회사는 완제품에 대한 품질검사를 하지 않는 등의 이유로 행정처분도 받았다.식품의약품안전처는 지난 17일자로 하이드로핀정 등 미래바이오제약 12개 품목 일부 제조번호에 대해 회수 명령을 내렸다. 회수 사유는 유통제품의 품질 부적합이 우려된다는 것이다.이는 지난 9월 식약처가 품질관리 문제로 미래바이오제약을 처분한 것과 관련 있어 보인다.지난 9월 식약처는 완제품 품질검사 미실시(12개 품목), 제조기록서·시험일지 및 시험성적서 미작성(23개 품목), 검사명령 미이행(22개 품목) 등 사유로 관련 제품의 제조업무를 최대 6개월까지 정지시킨 바 있다.이번에 회수 명령이 떨어진 제품도 당시 식약처에 적발된 품목들이다.미래바이오제약은 지난 5월에도 16개 제품 일부 제조번호가 품질부적합 우려로 회수되는 등 품질관리가 제대로 이뤄지지 않고 있는 것으로 관측된다.이는 회사 경영 상황과 무관치 않아 보인다. 회사는 유동성 부족 위기를 타개하기 위해 생산시설 매각을 추진하고 있다. 매각 과정에서 제품 품질관리가 제대로 안 이뤄진 것 아니냐는 관측이 나온다.지난 6월 발행된 감사보고서에서 미래바이오제약은 2024년 당기 영업손실 11억2300만원, 보고기간 말 기준 유동부채 135억8000만원이 유동자산 27억9900만원을 초과하는 유동성 부족 상태에 있다는 진단을 받았다.미래바이오제약은 이에 대한 대응책으로 의약품 생산시설을 매각하고 신규 생산시설로의 이전을 통해 자금 확보 및 차입금 상환을 계획하고 있다고 감사보고서에서 전했다.하지만 감사인은 한정의견을 제시하면서 회사의 생산시설 매각 및 신규 생산시설 이전 계획의 실행 가능성, 관련 인허가의 적시 취득 여부, 생산 정상화 시점 및 수익성 확보 가능성 등에 대해 충분하고 적합한 감사증거를 입수하지 못했다고 전했다.미래바이오제약(미래제약)은 2002년 금강제약을 인수하면서 KGMP 시설 인증을 받았다. 현재 대표자는 김한석 씨다.경기도 안성 공단2로에 위치한 완제의약품 공장은 2027년 4월 24일까지 비무균-일반제제-내용고형제(정제, 캡슐제) 제형군에 대해 GMP 적합판정서가 발급돼 있다.2025-10-19 15:58:25이탁순 -
 부적합 제품 출고 메디톡스에 과징금 4억5천만원 부과[데일리팜=이탁순 기자] 식약처가 주름 개선 치료 등에 사용되는 메디톡스 '메디톡신주(클로스트리디움보툴리눔독소A형)'에 대해 제조업무정지에 갈음하는 과징금을 부과했다.식약처는 22일자로 메디톡스에 과징금 총 4억5605만원의 행정처분을 내린다고 밝혔다.사유는 제조방법을 변경하지 않고 의약품을 제조·판매하고, 역가시험 결과 기준이 부적합다는 이유에서다. 또한 시험결과 부적합 제품을 출고하고, 시험성적서를 조작했다는 위반 내용도 포함됐다.이에 메디톡신주와 메디톡신주50단위에 대해 제조업무정지 3개월 25일을 갈음한 과징금 4억4275만원을 부과한다고 설명했다.또한 메디톡신주150단위에 대해서는 제조업무정지 2개월 10일을 갈음한 과징금 1330만원을 부과한다고 전했다.이번 처분은 양형을 합산해 나왔다. 또한 처분 확정 전 잠정 정지 기간(1개월 5일)을 제외한 기간에 과징금으로 갈음했다.앞서 식약처는 지난 2020년 6월 메디톡신 3개 품목에 대해 품목허가 취소 처분을 내렸었다. 하지만 법정 공방 끝에 대법원은 품묵허가 취소 처분을 취소하라는 판결을 내렸다.이에 식약처는 대법원 판결을 받아들이고, 업체 의견을 반영해 제조업무정지 처분 대신 과징금으로 갈음했다는 설명이다. 대법원도 이번 처분의 배경이 된 3가지 사유는 인정했다는 설명이다.2025-09-22 10:21:54이탁순
부적합 제품 출고 메디톡스에 과징금 4억5천만원 부과[데일리팜=이탁순 기자] 식약처가 주름 개선 치료 등에 사용되는 메디톡스 '메디톡신주(클로스트리디움보툴리눔독소A형)'에 대해 제조업무정지에 갈음하는 과징금을 부과했다.식약처는 22일자로 메디톡스에 과징금 총 4억5605만원의 행정처분을 내린다고 밝혔다.사유는 제조방법을 변경하지 않고 의약품을 제조·판매하고, 역가시험 결과 기준이 부적합다는 이유에서다. 또한 시험결과 부적합 제품을 출고하고, 시험성적서를 조작했다는 위반 내용도 포함됐다.이에 메디톡신주와 메디톡신주50단위에 대해 제조업무정지 3개월 25일을 갈음한 과징금 4억4275만원을 부과한다고 설명했다.또한 메디톡신주150단위에 대해서는 제조업무정지 2개월 10일을 갈음한 과징금 1330만원을 부과한다고 전했다.이번 처분은 양형을 합산해 나왔다. 또한 처분 확정 전 잠정 정지 기간(1개월 5일)을 제외한 기간에 과징금으로 갈음했다.앞서 식약처는 지난 2020년 6월 메디톡신 3개 품목에 대해 품목허가 취소 처분을 내렸었다. 하지만 법정 공방 끝에 대법원은 품묵허가 취소 처분을 취소하라는 판결을 내렸다.이에 식약처는 대법원 판결을 받아들이고, 업체 의견을 반영해 제조업무정지 처분 대신 과징금으로 갈음했다는 설명이다. 대법원도 이번 처분의 배경이 된 3가지 사유는 인정했다는 설명이다.2025-09-22 10:21:54이탁순 -
 식약처, 추석명절 건기식 거짓·과장 광고 점검[데일리팜=이혜경 기자] 식품의약품안전처(처장 오유경)는 추석 명절을 앞두고 국민이 안전한 식품을 구매할 수 있도록 9월 8일부터 12일까지 17개 지방자치단체와 함께 추석 성수식품의 위생관리 실태를 집중 점검한다고 밝혔다.이번 점검은 추석 명절에 선물 제수용으로 많이 소비되는 떡, 한과, 만두, 청주, 축산물(포장육 등), 건강기능식품(홍삼 등) 등을 제조하는 업체와 제수용 음식을 조리·판매하는 식품접객업체 총 5,860여 곳을 대상으로 실시된다.주요 점검 내용은 ▲무등록(신고) 제조·판매 ▲소비기한 경과제품 사용·판매 ▲건강진단 ▲냉장·냉동온도 기준 준수 ▲위생적 취급 여부 등이다.위생점검과 함께 선물·제수용 식품에 대한 유통단계(국내 유통)와 통관단계(수입식품) 검사도 강화한다.유통단계에는 떡·한과·전통주·고사리·참돔·포장육·액란·건강기능식품 등 1483여 건을 수거해 잔류농약, 중금속, 식중독균 등 항목을 집중 검사한다.통관단계에는 수입되는 ▲과채가공품(삶은 고사리 등)·식물성유지류(대두유, 참기름, 들기름 등)·어육살 등 가공식품(15품목) ▲목이버섯·도라지·돼지고기·명태·새우 등 농·축·수산물(12품목) ▲단일·복합 영양소제품·프로바이오틱스 등 건강기능식품(6품목)을 대상으로 중금속, 동물용의약품, 잔류농약 등에 대한 정밀검사를 실시한다.주요 점검 내용은 ▲질병의 예방·치료에 효능·효과가 있는 것으로 인식할 우려가 있는 광고 ▲의약품 또는 건강기능식품으로 오인·혼동시키는 광고 ▲거짓·과장·소비자 기만 광고 등이며, 특히 면역력 증진, 장 건강,혈행 건강 등의 표현으로 광고하는 온라인 게시물을 집중 점검한다.점검결과 위반업체에 대해서는 관련 법령에 따라 행정처분 등 조치하고, 부적합 제품은 신속히 회수·폐기(수입식품의 경우 수출국 반송 또는 폐기)해 시중에 유통되지 않도록 조치할 예정이다.식약처는 올해 설 명절에 실시한 합동점검 결과 총 7717곳 중 115곳(1.5%)을 적발했으며, 온라인 게시물 부당광고에 대한 모니터링 실시 결과 320건 중 45건(14.1%)을 적발해 관할기관에 행정처분 요청 등 조치한 바 있다.식약처는 올해 다이소, 편의점 등의 건강기능식품 판매가 크게 늘어남에 따라 안전관리를 강화하기 위한 현장점검(부당한 광고 위반 여부 포함)과 수거·검사도 실시한다.업계(다이소 본사, 한국편의점산업협회)에 위생적인 제품 보관·진열, 소비기한 준수 등 자발적인 위생안전 관리를 당부하는 한편 각 점포 매대에 소비자가 제품 정보와 섭취시 주의사항을 쉽게 확인할 수 있는 QR코드를 비치할 것을 요청했다.식약처는 앞으로도 명절 등 특정 시기에 소비가 증가하는 식품에 대한 사전 점검을 실시하여 안전관리를 강화하는 등 안전한 먹거리 환경을 조성하기 위해 최선을 다할 계획이다.2025-09-01 09:43:49이혜경
식약처, 추석명절 건기식 거짓·과장 광고 점검[데일리팜=이혜경 기자] 식품의약품안전처(처장 오유경)는 추석 명절을 앞두고 국민이 안전한 식품을 구매할 수 있도록 9월 8일부터 12일까지 17개 지방자치단체와 함께 추석 성수식품의 위생관리 실태를 집중 점검한다고 밝혔다.이번 점검은 추석 명절에 선물 제수용으로 많이 소비되는 떡, 한과, 만두, 청주, 축산물(포장육 등), 건강기능식품(홍삼 등) 등을 제조하는 업체와 제수용 음식을 조리·판매하는 식품접객업체 총 5,860여 곳을 대상으로 실시된다.주요 점검 내용은 ▲무등록(신고) 제조·판매 ▲소비기한 경과제품 사용·판매 ▲건강진단 ▲냉장·냉동온도 기준 준수 ▲위생적 취급 여부 등이다.위생점검과 함께 선물·제수용 식품에 대한 유통단계(국내 유통)와 통관단계(수입식품) 검사도 강화한다.유통단계에는 떡·한과·전통주·고사리·참돔·포장육·액란·건강기능식품 등 1483여 건을 수거해 잔류농약, 중금속, 식중독균 등 항목을 집중 검사한다.통관단계에는 수입되는 ▲과채가공품(삶은 고사리 등)·식물성유지류(대두유, 참기름, 들기름 등)·어육살 등 가공식품(15품목) ▲목이버섯·도라지·돼지고기·명태·새우 등 농·축·수산물(12품목) ▲단일·복합 영양소제품·프로바이오틱스 등 건강기능식품(6품목)을 대상으로 중금속, 동물용의약품, 잔류농약 등에 대한 정밀검사를 실시한다.주요 점검 내용은 ▲질병의 예방·치료에 효능·효과가 있는 것으로 인식할 우려가 있는 광고 ▲의약품 또는 건강기능식품으로 오인·혼동시키는 광고 ▲거짓·과장·소비자 기만 광고 등이며, 특히 면역력 증진, 장 건강,혈행 건강 등의 표현으로 광고하는 온라인 게시물을 집중 점검한다.점검결과 위반업체에 대해서는 관련 법령에 따라 행정처분 등 조치하고, 부적합 제품은 신속히 회수·폐기(수입식품의 경우 수출국 반송 또는 폐기)해 시중에 유통되지 않도록 조치할 예정이다.식약처는 올해 설 명절에 실시한 합동점검 결과 총 7717곳 중 115곳(1.5%)을 적발했으며, 온라인 게시물 부당광고에 대한 모니터링 실시 결과 320건 중 45건(14.1%)을 적발해 관할기관에 행정처분 요청 등 조치한 바 있다.식약처는 올해 다이소, 편의점 등의 건강기능식품 판매가 크게 늘어남에 따라 안전관리를 강화하기 위한 현장점검(부당한 광고 위반 여부 포함)과 수거·검사도 실시한다.업계(다이소 본사, 한국편의점산업협회)에 위생적인 제품 보관·진열, 소비기한 준수 등 자발적인 위생안전 관리를 당부하는 한편 각 점포 매대에 소비자가 제품 정보와 섭취시 주의사항을 쉽게 확인할 수 있는 QR코드를 비치할 것을 요청했다.식약처는 앞으로도 명절 등 특정 시기에 소비가 증가하는 식품에 대한 사전 점검을 실시하여 안전관리를 강화하는 등 안전한 먹거리 환경을 조성하기 위해 최선을 다할 계획이다.2025-09-01 09:43:49이혜경 -
 경남도, 약국·도매·동물병원 부적합 동물약 유통 단속[데일리팜=강신국 기자] 경남도는 시군과 함동으로 부적합 동물용 의약품 유통 및 사용 사전 예방을 위해 오는 20일부터 9월 16일까지 동물약 유통 점검에 나선다고 18일 밝혔다. 점검 대상은 도내 동물약국 718곳, 동물용 의약품 도매상 32곳, 동물병원 354곳이다.주요 점검사항은 동물용 의약품 관리, 무허가 및 유통기간 경과 제품 등 보관·판매, 판매업 시설 적합성, 약사 관리, 처방 대상 동물용 의약품 처방전에 따른 판매 준수 등이다.위반 사항 적발 시 현장지도 및 시정조치하고 법령 위반 사항에 대한 확인서 징수와 행정처분을 취할 계획이다.아울러 시중 유통 항생물질, 화학제제 등 동물약품 수거검사를 병행 실시하여, 성분 및 함량 미달 등 부적합 제품은 수거·폐기 등 규정에 따라 조치할 방침이다.정창근 동물방역과장은 "철저한 단속을 통해 부정 동물약품 유통을 사전 예방해 축산농가와 반려동물 보호자가 동물약품을 믿고 사용할 수 있는 안전한 동물의료 환경을 조성하겠다"고 말했다.2025-08-18 09:03:43강신국
경남도, 약국·도매·동물병원 부적합 동물약 유통 단속[데일리팜=강신국 기자] 경남도는 시군과 함동으로 부적합 동물용 의약품 유통 및 사용 사전 예방을 위해 오는 20일부터 9월 16일까지 동물약 유통 점검에 나선다고 18일 밝혔다. 점검 대상은 도내 동물약국 718곳, 동물용 의약품 도매상 32곳, 동물병원 354곳이다.주요 점검사항은 동물용 의약품 관리, 무허가 및 유통기간 경과 제품 등 보관·판매, 판매업 시설 적합성, 약사 관리, 처방 대상 동물용 의약품 처방전에 따른 판매 준수 등이다.위반 사항 적발 시 현장지도 및 시정조치하고 법령 위반 사항에 대한 확인서 징수와 행정처분을 취할 계획이다.아울러 시중 유통 항생물질, 화학제제 등 동물약품 수거검사를 병행 실시하여, 성분 및 함량 미달 등 부적합 제품은 수거·폐기 등 규정에 따라 조치할 방침이다.정창근 동물방역과장은 "철저한 단속을 통해 부정 동물약품 유통을 사전 예방해 축산농가와 반려동물 보호자가 동물약품을 믿고 사용할 수 있는 안전한 동물의료 환경을 조성하겠다"고 말했다.2025-08-18 09:03:43강신국 -
 한독 면역항암제 민쥬비, 림프종 새 치료 옵션 제시[데일리팜=노병철 기자] 최근 치료제가 제한적이었던 미만성 거대 B세포 림프종(DLBCL)에 새로운 치료제들이 속속 추가되고 있다.DLBCL은 림프종의 한 종류로 림프절 또는 다른 장기에 악성B세포가 급격히 증식하는 암이다.2024년 중앙암등록본부에 따르면 2022년 한 해 동안 새롭게 발생한 림프종 환자는 6447명이었고, 이 중 90% 이상이 비호지킨림프종이었다.그 중에서도 미만성 거대 B세포 림프종은 비호지킨림프종의 가장 흔한 아형으로, 매년 약 3000명이 새롭게 진단받는다.10명 중 4명의 DLBCL 환자가 1차 치료 후 재발 또는 불응DLBCL은 매우 공격적인 질환으로 약 40%의 환자가 초기 치료에서 재발 또는 불응을 하는 것으로 보고되고 있다.1차 치료인 리툭시맙과 싸이클로포스파마이드, 독소루비신, 빈크리스틴, 프레드니솔론 (R-CHOP) 치료를 받은 고령 DLBCL 환자의 5년 생존율은 58%로 확인되었다.이와 비교해 재발한 DLBCL 환자는 이후 치료인 구제요법에도 1년 생존율이 28%에 불과할 정도로 예후가 불량하다.국내 연구에 따르면, 2차 치료를 받은 재발성/불응성DLBCL 환자들의 중위 무진행 생존기간(질병이 진행하지 않으면서 생존한 기간)은 4.47개월, 중위 생존기간은 8.9개월로 나타났다.재발 또는 불응 환자의 50%는 표준 2차 치료 옵션인 자가조혈모세포이식(ASCT)이 가능하다.하지만 ASCT가 부적합한 50%의 환자들은 ‘구제항암요법’이라고 불리는 항암 치료를 받게 된다.세포독성항암제들을 중점적으로 사용하는 구제항암요법은 다양한 부작용이 나타나 고령 환자 및 의료진의 미충족 의료수요가 존재해왔다.잇따라 국내 허가 및 접근성 확대 중인 재발성/불응성 DLBCL 신약들다행히 2023년부터 DLBCL 신약들이 국내에 진입하고, 보험 급여 등재를 진행하며 치료 옵션이 다양해지고 있다.그 가운데 2023년 6월에는 국내에서 2차 치료제로 사용할 수 있는 면역항암제 민쥬비가 허가를 받았다.민쥬비(타파시타맙)는 현재 치료 옵션이 제한적인 이식이 부적합한 DLBCL의 2차 치료에 사용할 수 있는 치료제이다. 글로벌 바이오파마슈티컬 회사인 인사이트의 제품으로 한독이 국내 공급을 담당하고 있다.민쥬비는 자가조혈모세포이식(ASCT)이 적합하지 않고 한 가지 이상의 이전 치료에 실패한 재발성 또는 불응성인 DLBCL 성인 환자에서 레날리도마이드와 병용요법, 이후 단독요법으로 허가를 받았다. 아직 보험급여 전이지만 치료가 필요한 환자들에게 투약되고 있다.DLBCL 환자들이 진단 당시에 65세 이상이라는 점을 고려하면, 내약성은 매우 중요하지만, ASCT 혹은 고용량 항암요법은 취약한 환자들에게 부적합하다.하지만, 민쥬비와 레날리도마이드의 병용요법은 이런 환자군에서 전통 화학요법의 대안으로 제시된 내약성 있는 무화학 요법(non-cytotoxic)이다.악성 B세포 혈액암 치료의 중심에 서 있는 CD19번 단백질을 특징적으로 표적하는 단일클론항체제제인 민쥬비는 면역조절제인 레날리도마이드와 병용해 치료한다. DLBCL 2차 치료제 민쥬비, 2차에서 선제적으로 사용했을 때 우수한 효과민쥬비는 L-MIND 연구의 5년 추적 결과에서 이식이 부적합한 재발성/불응성 DLBCL 성인 환자를 대상으로 의미있는 치료 효과를 보였다.민쥬비와 레날리도마이드의 병용요법 이후 민쥬비의 단일요법을 투여한 결과, 1차 평가 변수인 ORR(Objective Response Rate)은 최고 57.5%, CR(Complete Response)은 41.3%로 나타났다.특히, 2차 치료에 민쥬비를 사용했을 경우 ORR은 67.5%, CR은 52.5%로 나타나 2차 치료에 민쥬비를 선제적으로 사용했을 때 더욱 우수한 효과를 보이는 것으로 확인됐다.2차 치료에서 사용 시 무진행 생존기간은 23.5 개월, 중위 생존기간은 65.5개월이라는 추적기간 동안 도달하지 않았다.이와 더불어 민쥬비는 L-MIND 연구 뿐 아니라, 예후가 비교적 나쁜 실제 진료 환경에서도 치료 성과를 보였다.프랑스의 실제 임상 환경(Real-World)에서 중위 연령 78세와 예후가 불량한 원발성 불응성 또는 1년 이내 조기재발 환자군이 71%가 포함된 이식 부적합 재발성/불응성 DLBCL 환자군을 대상으로 진행한 다기관 후양적 EarlyMIND 연구 결과에서 민쥬비는 L-MIND 연구와 유사한 46.8%의 ORR과 29%의 CR 비율을 보였다.또, 완전 관해를 얻은 환자군에서는 중위 관해 유지 기간이 추적기간 동안 도달하지 않는(Not Reached) 결과를 나타냈다.2025-08-18 06:00:07노병철
한독 면역항암제 민쥬비, 림프종 새 치료 옵션 제시[데일리팜=노병철 기자] 최근 치료제가 제한적이었던 미만성 거대 B세포 림프종(DLBCL)에 새로운 치료제들이 속속 추가되고 있다.DLBCL은 림프종의 한 종류로 림프절 또는 다른 장기에 악성B세포가 급격히 증식하는 암이다.2024년 중앙암등록본부에 따르면 2022년 한 해 동안 새롭게 발생한 림프종 환자는 6447명이었고, 이 중 90% 이상이 비호지킨림프종이었다.그 중에서도 미만성 거대 B세포 림프종은 비호지킨림프종의 가장 흔한 아형으로, 매년 약 3000명이 새롭게 진단받는다.10명 중 4명의 DLBCL 환자가 1차 치료 후 재발 또는 불응DLBCL은 매우 공격적인 질환으로 약 40%의 환자가 초기 치료에서 재발 또는 불응을 하는 것으로 보고되고 있다.1차 치료인 리툭시맙과 싸이클로포스파마이드, 독소루비신, 빈크리스틴, 프레드니솔론 (R-CHOP) 치료를 받은 고령 DLBCL 환자의 5년 생존율은 58%로 확인되었다.이와 비교해 재발한 DLBCL 환자는 이후 치료인 구제요법에도 1년 생존율이 28%에 불과할 정도로 예후가 불량하다.국내 연구에 따르면, 2차 치료를 받은 재발성/불응성DLBCL 환자들의 중위 무진행 생존기간(질병이 진행하지 않으면서 생존한 기간)은 4.47개월, 중위 생존기간은 8.9개월로 나타났다.재발 또는 불응 환자의 50%는 표준 2차 치료 옵션인 자가조혈모세포이식(ASCT)이 가능하다.하지만 ASCT가 부적합한 50%의 환자들은 ‘구제항암요법’이라고 불리는 항암 치료를 받게 된다.세포독성항암제들을 중점적으로 사용하는 구제항암요법은 다양한 부작용이 나타나 고령 환자 및 의료진의 미충족 의료수요가 존재해왔다.잇따라 국내 허가 및 접근성 확대 중인 재발성/불응성 DLBCL 신약들다행히 2023년부터 DLBCL 신약들이 국내에 진입하고, 보험 급여 등재를 진행하며 치료 옵션이 다양해지고 있다.그 가운데 2023년 6월에는 국내에서 2차 치료제로 사용할 수 있는 면역항암제 민쥬비가 허가를 받았다.민쥬비(타파시타맙)는 현재 치료 옵션이 제한적인 이식이 부적합한 DLBCL의 2차 치료에 사용할 수 있는 치료제이다. 글로벌 바이오파마슈티컬 회사인 인사이트의 제품으로 한독이 국내 공급을 담당하고 있다.민쥬비는 자가조혈모세포이식(ASCT)이 적합하지 않고 한 가지 이상의 이전 치료에 실패한 재발성 또는 불응성인 DLBCL 성인 환자에서 레날리도마이드와 병용요법, 이후 단독요법으로 허가를 받았다. 아직 보험급여 전이지만 치료가 필요한 환자들에게 투약되고 있다.DLBCL 환자들이 진단 당시에 65세 이상이라는 점을 고려하면, 내약성은 매우 중요하지만, ASCT 혹은 고용량 항암요법은 취약한 환자들에게 부적합하다.하지만, 민쥬비와 레날리도마이드의 병용요법은 이런 환자군에서 전통 화학요법의 대안으로 제시된 내약성 있는 무화학 요법(non-cytotoxic)이다.악성 B세포 혈액암 치료의 중심에 서 있는 CD19번 단백질을 특징적으로 표적하는 단일클론항체제제인 민쥬비는 면역조절제인 레날리도마이드와 병용해 치료한다. DLBCL 2차 치료제 민쥬비, 2차에서 선제적으로 사용했을 때 우수한 효과민쥬비는 L-MIND 연구의 5년 추적 결과에서 이식이 부적합한 재발성/불응성 DLBCL 성인 환자를 대상으로 의미있는 치료 효과를 보였다.민쥬비와 레날리도마이드의 병용요법 이후 민쥬비의 단일요법을 투여한 결과, 1차 평가 변수인 ORR(Objective Response Rate)은 최고 57.5%, CR(Complete Response)은 41.3%로 나타났다.특히, 2차 치료에 민쥬비를 사용했을 경우 ORR은 67.5%, CR은 52.5%로 나타나 2차 치료에 민쥬비를 선제적으로 사용했을 때 더욱 우수한 효과를 보이는 것으로 확인됐다.2차 치료에서 사용 시 무진행 생존기간은 23.5 개월, 중위 생존기간은 65.5개월이라는 추적기간 동안 도달하지 않았다.이와 더불어 민쥬비는 L-MIND 연구 뿐 아니라, 예후가 비교적 나쁜 실제 진료 환경에서도 치료 성과를 보였다.프랑스의 실제 임상 환경(Real-World)에서 중위 연령 78세와 예후가 불량한 원발성 불응성 또는 1년 이내 조기재발 환자군이 71%가 포함된 이식 부적합 재발성/불응성 DLBCL 환자군을 대상으로 진행한 다기관 후양적 EarlyMIND 연구 결과에서 민쥬비는 L-MIND 연구와 유사한 46.8%의 ORR과 29%의 CR 비율을 보였다.또, 완전 관해를 얻은 환자군에서는 중위 관해 유지 기간이 추적기간 동안 도달하지 않는(Not Reached) 결과를 나타냈다.2025-08-18 06:00:07노병철 -
 식약처, 의약외품 마스크 품질검사...4개 부적합[데일리팜=이혜경 기자] 식품의약품안전처(처장 오유경)는 의약외품 마스크의 품질 확보를 위해 지난 3월 온·오프라인에서 유통되는 보건용마스크, 비말차단용마스크, 수술용마스크 240개 제품을 수거·검사한 결과, 보건용마스크 4개 제품이 부적합으로 나타났다고 28일 밝혔다.식약처는 품목별로 분진포집효율(보건용), 액체저항성(비말차단용·수술용)을 검사했으며, 보건용마스크 4개 제품이 분진포집효율에서 기준에 미달 해당 제조업체에 판매 중단을 조치했다.부적합 마스크는 '의약품안전나라(nedrug.mfds.go.kr) → 고시/공고/알림 → 안전성정보 → 회수·폐기 또는 행정처분'에서 확인 가능하다.최근 분집포집효율로 회수 조치가 이뤄진 품목은 알원의 '수마스크(KF94)(대형)', 제이트로닉스의 '블루나투디패션황사방역마스크(KF94)(대형,중형,소형)', 힐링케어의 '힐링케어보건용마스크(KF94)(대형)(흰색)' 등이 있다.분진포집효율은 작은 입자(에어로졸)를 걸러내는 정도(비율)를 측정하는 시험으로, 황사, 미세먼지 등 입자성 유해물질로부터 호흡기를 보호하는 보건용마스크의 성능을 평가하는 주요 항목이다.액체저항성시험은 마스크에 물이 침투하는 시간을 측정하여 액체 저항성을 측정하는 시험으로. 비말차단·수술용마스크 성능을 평가하는 항목이다.식약처는 앞으로도 다소비 의약외품에 대해 국민안심을 최우선으로 하여 적합한 품질의 제품이 유통될 수 있도록 지속적으로 의약외품 수거·검사를 실시하는 등 의약외품 안전관리에 최선을 다할 계획이다.2025-07-28 16:05:46이혜경
식약처, 의약외품 마스크 품질검사...4개 부적합[데일리팜=이혜경 기자] 식품의약품안전처(처장 오유경)는 의약외품 마스크의 품질 확보를 위해 지난 3월 온·오프라인에서 유통되는 보건용마스크, 비말차단용마스크, 수술용마스크 240개 제품을 수거·검사한 결과, 보건용마스크 4개 제품이 부적합으로 나타났다고 28일 밝혔다.식약처는 품목별로 분진포집효율(보건용), 액체저항성(비말차단용·수술용)을 검사했으며, 보건용마스크 4개 제품이 분진포집효율에서 기준에 미달 해당 제조업체에 판매 중단을 조치했다.부적합 마스크는 '의약품안전나라(nedrug.mfds.go.kr) → 고시/공고/알림 → 안전성정보 → 회수·폐기 또는 행정처분'에서 확인 가능하다.최근 분집포집효율로 회수 조치가 이뤄진 품목은 알원의 '수마스크(KF94)(대형)', 제이트로닉스의 '블루나투디패션황사방역마스크(KF94)(대형,중형,소형)', 힐링케어의 '힐링케어보건용마스크(KF94)(대형)(흰색)' 등이 있다.분진포집효율은 작은 입자(에어로졸)를 걸러내는 정도(비율)를 측정하는 시험으로, 황사, 미세먼지 등 입자성 유해물질로부터 호흡기를 보호하는 보건용마스크의 성능을 평가하는 주요 항목이다.액체저항성시험은 마스크에 물이 침투하는 시간을 측정하여 액체 저항성을 측정하는 시험으로. 비말차단·수술용마스크 성능을 평가하는 항목이다.식약처는 앞으로도 다소비 의약외품에 대해 국민안심을 최우선으로 하여 적합한 품질의 제품이 유통될 수 있도록 지속적으로 의약외품 수거·검사를 실시하는 등 의약외품 안전관리에 최선을 다할 계획이다.2025-07-28 16:05:46이혜경 -
 심근병증에 자가유래 단핵세포 투여…"임상연구 재심의"[데일리팜=이정환 기자] 비허혈성 확장성 심근병증 환자에게 자가유래 단핵세포를 투여해 심부전 증상과 좌심실 기능 개선 효과를 평가하는 저위험 임상연구가 정부 위원회로부터 재심의 판정을 받았다.고위험 미만성 거대 B세포 림프종 환자를 대상으로 1차 관해유도요법 종료 후 유지 요법으로서 자가 사이토카인 유도 살해세포를 투여하는 중위험 임상연구도 재심의가 결정됐다.보건복지부(장관 조규홍)는 26일 열린 2025년 제6차 첨단재생의료 및 첨단바이오의약품 심의위원회(이하 심의위원회) 개최 결과를 공개했다.심의위원회는 재생의료기관에서 제출한 임상연구계획 총 7건(중위험 3건, 저위험 4건)을 심의했으며, 이 중 2건은 재심의하기로 결정했고, 5건은 부적합 의결하였다.재심의 결정된 첫 번째 과제는 비허혈성 확장성 심근병증 환자를 대상으로 환자 본인의 골수에서 유래한 단핵세포를 투여하여 심부전 증상과 좌심실 기능 개선 효과를 평가하기 위한 저위험 임상연구이다.‘비허혈성 확장성 심근병증’이란, 심부전 중 가역적이지 않은 형태의 심장 근육 질환이다.비정상적인 부하상태를 보이며, 중증 관상동맥 질환이 없는 상태에서 좌심실의 확장과 수축 기능 장애를 동반한다.재심의 된 두 번째 과제는 고위험 미만성 거대 B세포 림프종(DLBCL) 환자를 대상으로 1차 관해유도요법(R-CHOP 요법) 종료 후 유지 요법으로서 자가 사이토카인 유도 살해 세포(Cytokine-Induced Killer Cells, CIK)를 투여하는 중위험 임상연구다.‘미만성 거대 B세포 림프종(Diffuse Large B-Cell Lymphoma, DLBCL)’ 이란 림프구의 비정상적 증식을 특징으로 하는 혈액암으로 비호지킨 림프종 중 가장 흔한(전체 환자의 약 1/3) 아형이다.심의위원회에서는 위의 두 과제에 대하여 관련 자료의 보완 후 다시 논의하기로 결정했다.김우기 첨단재생의료 및 첨단바이오의약품 심의위원회 사무국장은 "심의위원회에서 심장·암 질환 등 생명에 치명적인 질환을 대상으로 한 임상연구계획이 심의됐다"며 "심의위원회와 사무국은 첨단재생의료를 이용해 중대·희귀·난치질환자에게 치료 기회를 제공하고, 첨단재생의료 기술을 발전시키기 위해 임상연구를 활성화할 수 있도록 지속적으로 노력하겠다"고 밝혔다.2025-06-27 11:39:11이정환
심근병증에 자가유래 단핵세포 투여…"임상연구 재심의"[데일리팜=이정환 기자] 비허혈성 확장성 심근병증 환자에게 자가유래 단핵세포를 투여해 심부전 증상과 좌심실 기능 개선 효과를 평가하는 저위험 임상연구가 정부 위원회로부터 재심의 판정을 받았다.고위험 미만성 거대 B세포 림프종 환자를 대상으로 1차 관해유도요법 종료 후 유지 요법으로서 자가 사이토카인 유도 살해세포를 투여하는 중위험 임상연구도 재심의가 결정됐다.보건복지부(장관 조규홍)는 26일 열린 2025년 제6차 첨단재생의료 및 첨단바이오의약품 심의위원회(이하 심의위원회) 개최 결과를 공개했다.심의위원회는 재생의료기관에서 제출한 임상연구계획 총 7건(중위험 3건, 저위험 4건)을 심의했으며, 이 중 2건은 재심의하기로 결정했고, 5건은 부적합 의결하였다.재심의 결정된 첫 번째 과제는 비허혈성 확장성 심근병증 환자를 대상으로 환자 본인의 골수에서 유래한 단핵세포를 투여하여 심부전 증상과 좌심실 기능 개선 효과를 평가하기 위한 저위험 임상연구이다.‘비허혈성 확장성 심근병증’이란, 심부전 중 가역적이지 않은 형태의 심장 근육 질환이다.비정상적인 부하상태를 보이며, 중증 관상동맥 질환이 없는 상태에서 좌심실의 확장과 수축 기능 장애를 동반한다.재심의 된 두 번째 과제는 고위험 미만성 거대 B세포 림프종(DLBCL) 환자를 대상으로 1차 관해유도요법(R-CHOP 요법) 종료 후 유지 요법으로서 자가 사이토카인 유도 살해 세포(Cytokine-Induced Killer Cells, CIK)를 투여하는 중위험 임상연구다.‘미만성 거대 B세포 림프종(Diffuse Large B-Cell Lymphoma, DLBCL)’ 이란 림프구의 비정상적 증식을 특징으로 하는 혈액암으로 비호지킨 림프종 중 가장 흔한(전체 환자의 약 1/3) 아형이다.심의위원회에서는 위의 두 과제에 대하여 관련 자료의 보완 후 다시 논의하기로 결정했다.김우기 첨단재생의료 및 첨단바이오의약품 심의위원회 사무국장은 "심의위원회에서 심장·암 질환 등 생명에 치명적인 질환을 대상으로 한 임상연구계획이 심의됐다"며 "심의위원회와 사무국은 첨단재생의료를 이용해 중대·희귀·난치질환자에게 치료 기회를 제공하고, 첨단재생의료 기술을 발전시키기 위해 임상연구를 활성화할 수 있도록 지속적으로 노력하겠다"고 밝혔다.2025-06-27 11:39:11이정환 -
 포장·표시 불량 의약품, 비만약 불법 광고 등 집중 점검[데일리팜=이혜경 기자] 식품의약품안전처가 오늘(23일)부터 27일까지 포장·표시 오류 회수업체 등을 대상으로 약사감시에 들어간다.이와 함께 비만치료제의 오남용을 예방하기 위해 취급 의료기관·약국을 중심으로 전문의약품의 대중광고, 허가사항 범위 외 정보에 대한 과대·거짓광고 여부 등을 점검한다.식약처는 의약품·바이오의약품·한약·의약외품·의료기기 안전관리 강화를 위해 지방식품의약품안전청·지방자치단체와 함께 '2025년 2분기 의료제품 분야별 기획합동감시'를 실시한다고 밝혔다.이번 합동감시는 ▲포장·표시 오류 회수업체 대상 조치·재발방지 방안 이행 여부 ▲비만치료제 취급 의료기관·약국 중심으로 광고 점검 ▲한약재(우황, 녹용) 원료의 품질관리 적정성 중점 점검 ▲코골이방지제 제조(수입)업체 품질 및 생리용품 판매업체 거짓·과장광고 점검 ▲수입·통관 단계의 다수 불법 수입 적발업체 실태 점검 등이 포함된다.우선 의약품의 경우 최근 포장·표시기재 오류 의약품의 회수가 지속적으로 발생함에 따라 포장·표시 불량으로 인한 회수 이력이 있는 제조업체를 점검한다.주요 점검 내용은 의약품 회수 시 업체가 제출한 후속조치 및 재발방지방안 이행 여부, 포장·표시 관련 공정에 대한 자율점검 후속조치 실시 여부 등이다.재발방지방안은 위반사항의 원인을 찾아 제거하고, 향후 재발방지를 위해 잠재적 부적합 원인을 제거하기 위한 조치 중 하나다.식약처는 지난해 9월 포장·표시 불량이 다빈도로 발생하는 제형(내용고형제) 제조업체를 대상으로 자율점검을 실시한 바 있다.점검 결과 후속조치 등을 이행하지 않았거나 위반이 확인되는 경우 행정처분 등 필요한 조치를 할 예정이다.여름을 맞아 비만환자 치료에 사용하는 GLP-1 계열 비만치료 바이오의약품을 투약 후기와 함께 '살 빼는 약'으로 소개하는 온라인 게시물이나 환자 대기실에 홍보물 비치하는 등 전문의약품의 불법 광고로 인한 오남용 우려가 높아지고 있다.이에 따라 식약처는 비만치료제의 오남용을 예방하기 위해 취급 의료기관·약국을 중심으로 ▲광고 매체 또는 수단을 이용한 전문의약품의 대중광고 여부 ▲허가사항 범위 외 정보를 불특정 다수에게 과대·거짓광고 여부 등을 점검한다.점검 결과 위반이 확인되는 의료기관·약국, 필요시 도매상 또는 제약업체에 대해 행정지도, 행정처분 등 필요한 조치를 할 예정이다.녹용, 우황 등의 대표적인 고가 한약재에 대한 철저한 품질관리가 필요한 만큼 한약재 제조업소와 우황청심원 등 우황 함유 한약(생약)제제 제조업체를 점검한다.주요 점검 내용은 ▲원료 및 완제품 품질검사의 적정성 ▲원료 보관관리와 완제품 제조관리의 적정성 등이며, 점검 결과 위반이 확인된 경우 행정처분 등 필요한 조치를 할 예정이다.코고는 소음의 감소 및 억제를 위해 사용하는 코골이방지제의 안전한 유통환경을 확보하기 위해 제조(수입)업체 대상으로 ▲원자재 및 완제품의 품질검사 수행 여부 ▲미생물 품질관리 ▲제조시설의 위생관리 적정 여부 등을 점검한다.또한, 다수의 온라인 판매사이트에서 동일한 광고 위반내용으로 적발된 생리용품 판매업체를 대상으로 거짓·과장광고 점검을 실시하고, 위반이 확인된 광고가 제조(수입)업체로부터 제공된 경우 제조(수입)업체도 점검한다.점검 결과 위반이 확인된 의약외품 제조(수입)업체 및 판매업체에 대해 행정지도, 행정처분 등 필요한 조치를 할 예정이다.허가받지 않은 불법 의료기기를 해외직구, 구매대행 등을 통해 수입하여 적발된 사례가 지속적으로 발생함에 따라, 의료기기 수입·통관 단계에서 불법 의료기기 반입으로 다수 적발된 업체를 점검한다.주요 점검 내용은 ▲불법 수입 의료기기 불법 유통 여부 ▲반송 또는 폐기 조치 여부 ▲그 외 의료기기법 위반 사항 등이다.점검 결과 불법 수입 의료기기를 보관하거나 반송·폐기하지 않고 판매업체 등에 유통하는 등 위반이 확인된 업체에 대해서는 행정처분 등 조치를 할 예정이다.식약처는 이번 기획합동감시의 내실을 기하기 위해 지방식품의약품안전청과 지방자치단체(시& 8729;도, 시& 8729;군& 8729;구)가 함께하는 ‘2025년 2분기 의료제품 분야 감시원 교육’(6.19.~20.)에서 점검방법 등 사전교육을 실시했다.식약처는 "앞으로도 국민 안전을 확보하기 위해 의료제품을 대상으로 지속적인 점검을 실시하고, 품질과 안전이 확보된 의료제품을 국민이 사용할 수 있도록 최선을 다하겠다"고 밝혔다.2025-06-23 09:00:48이혜경
포장·표시 불량 의약품, 비만약 불법 광고 등 집중 점검[데일리팜=이혜경 기자] 식품의약품안전처가 오늘(23일)부터 27일까지 포장·표시 오류 회수업체 등을 대상으로 약사감시에 들어간다.이와 함께 비만치료제의 오남용을 예방하기 위해 취급 의료기관·약국을 중심으로 전문의약품의 대중광고, 허가사항 범위 외 정보에 대한 과대·거짓광고 여부 등을 점검한다.식약처는 의약품·바이오의약품·한약·의약외품·의료기기 안전관리 강화를 위해 지방식품의약품안전청·지방자치단체와 함께 '2025년 2분기 의료제품 분야별 기획합동감시'를 실시한다고 밝혔다.이번 합동감시는 ▲포장·표시 오류 회수업체 대상 조치·재발방지 방안 이행 여부 ▲비만치료제 취급 의료기관·약국 중심으로 광고 점검 ▲한약재(우황, 녹용) 원료의 품질관리 적정성 중점 점검 ▲코골이방지제 제조(수입)업체 품질 및 생리용품 판매업체 거짓·과장광고 점검 ▲수입·통관 단계의 다수 불법 수입 적발업체 실태 점검 등이 포함된다.우선 의약품의 경우 최근 포장·표시기재 오류 의약품의 회수가 지속적으로 발생함에 따라 포장·표시 불량으로 인한 회수 이력이 있는 제조업체를 점검한다.주요 점검 내용은 의약품 회수 시 업체가 제출한 후속조치 및 재발방지방안 이행 여부, 포장·표시 관련 공정에 대한 자율점검 후속조치 실시 여부 등이다.재발방지방안은 위반사항의 원인을 찾아 제거하고, 향후 재발방지를 위해 잠재적 부적합 원인을 제거하기 위한 조치 중 하나다.식약처는 지난해 9월 포장·표시 불량이 다빈도로 발생하는 제형(내용고형제) 제조업체를 대상으로 자율점검을 실시한 바 있다.점검 결과 후속조치 등을 이행하지 않았거나 위반이 확인되는 경우 행정처분 등 필요한 조치를 할 예정이다.여름을 맞아 비만환자 치료에 사용하는 GLP-1 계열 비만치료 바이오의약품을 투약 후기와 함께 '살 빼는 약'으로 소개하는 온라인 게시물이나 환자 대기실에 홍보물 비치하는 등 전문의약품의 불법 광고로 인한 오남용 우려가 높아지고 있다.이에 따라 식약처는 비만치료제의 오남용을 예방하기 위해 취급 의료기관·약국을 중심으로 ▲광고 매체 또는 수단을 이용한 전문의약품의 대중광고 여부 ▲허가사항 범위 외 정보를 불특정 다수에게 과대·거짓광고 여부 등을 점검한다.점검 결과 위반이 확인되는 의료기관·약국, 필요시 도매상 또는 제약업체에 대해 행정지도, 행정처분 등 필요한 조치를 할 예정이다.녹용, 우황 등의 대표적인 고가 한약재에 대한 철저한 품질관리가 필요한 만큼 한약재 제조업소와 우황청심원 등 우황 함유 한약(생약)제제 제조업체를 점검한다.주요 점검 내용은 ▲원료 및 완제품 품질검사의 적정성 ▲원료 보관관리와 완제품 제조관리의 적정성 등이며, 점검 결과 위반이 확인된 경우 행정처분 등 필요한 조치를 할 예정이다.코고는 소음의 감소 및 억제를 위해 사용하는 코골이방지제의 안전한 유통환경을 확보하기 위해 제조(수입)업체 대상으로 ▲원자재 및 완제품의 품질검사 수행 여부 ▲미생물 품질관리 ▲제조시설의 위생관리 적정 여부 등을 점검한다.또한, 다수의 온라인 판매사이트에서 동일한 광고 위반내용으로 적발된 생리용품 판매업체를 대상으로 거짓·과장광고 점검을 실시하고, 위반이 확인된 광고가 제조(수입)업체로부터 제공된 경우 제조(수입)업체도 점검한다.점검 결과 위반이 확인된 의약외품 제조(수입)업체 및 판매업체에 대해 행정지도, 행정처분 등 필요한 조치를 할 예정이다.허가받지 않은 불법 의료기기를 해외직구, 구매대행 등을 통해 수입하여 적발된 사례가 지속적으로 발생함에 따라, 의료기기 수입·통관 단계에서 불법 의료기기 반입으로 다수 적발된 업체를 점검한다.주요 점검 내용은 ▲불법 수입 의료기기 불법 유통 여부 ▲반송 또는 폐기 조치 여부 ▲그 외 의료기기법 위반 사항 등이다.점검 결과 불법 수입 의료기기를 보관하거나 반송·폐기하지 않고 판매업체 등에 유통하는 등 위반이 확인된 업체에 대해서는 행정처분 등 조치를 할 예정이다.식약처는 이번 기획합동감시의 내실을 기하기 위해 지방식품의약품안전청과 지방자치단체(시& 8729;도, 시& 8729;군& 8729;구)가 함께하는 ‘2025년 2분기 의료제품 분야 감시원 교육’(6.19.~20.)에서 점검방법 등 사전교육을 실시했다.식약처는 "앞으로도 국민 안전을 확보하기 위해 의료제품을 대상으로 지속적인 점검을 실시하고, 품질과 안전이 확보된 의료제품을 국민이 사용할 수 있도록 최선을 다하겠다"고 밝혔다.2025-06-23 09:00:48이혜경 -
 건기식 표시·광고 심의 통일…협회 '공통심의기준' 발간[데일리팜=강혜경 기자] 한국건강기능식품협회(회장 정명수)가 건강기능식품의 표시·광고 심의기준을 통일하기 위해 소비자공익네트워크와 공동으로 '건강기능식품 표시·광고 공통심의기준'을 발간했다.소비자공익네트워크와 한국식품산업협회, 한국건강기능식품협회로 구성된 '식품 등 표시·광고 자율심의기구'는 정례협의체를 운영하며 심의기준의 정합성을 높이기 위해 지속적으로 협업해 왔고, 그 일환으로 공통심의기준을 발간하게 됐다는 설명이다.공통심의기준은 ▲관련 법령 및 운영규정 ▲광고 작성시 유의사항 ▲심의 가이드라인 ▲기능성 품목별 기준 ▲표시·광고 적합·부적합 사례 등으로 구성됐다.협회 관계자는 "이번 공통심의기준은 다양한 분야별 전문가들이 지혜를 모아 시대의 변화에 부합하는 합리적인 기준을 마련하고자 노력한 결과"라며 "앞으로도 건기식 표시·광고 심의가 내실있게 이뤄지고 지속적으로 발전할 수 있도록 적극 지원하겠다"고 말했다.건강기능식품 표시·광고 공통심의기준’은 각 심의기구 홈페이지에서 열람할 수 있다.2025-06-17 17:06:48강혜경
건기식 표시·광고 심의 통일…협회 '공통심의기준' 발간[데일리팜=강혜경 기자] 한국건강기능식품협회(회장 정명수)가 건강기능식품의 표시·광고 심의기준을 통일하기 위해 소비자공익네트워크와 공동으로 '건강기능식품 표시·광고 공통심의기준'을 발간했다.소비자공익네트워크와 한국식품산업협회, 한국건강기능식품협회로 구성된 '식품 등 표시·광고 자율심의기구'는 정례협의체를 운영하며 심의기준의 정합성을 높이기 위해 지속적으로 협업해 왔고, 그 일환으로 공통심의기준을 발간하게 됐다는 설명이다.공통심의기준은 ▲관련 법령 및 운영규정 ▲광고 작성시 유의사항 ▲심의 가이드라인 ▲기능성 품목별 기준 ▲표시·광고 적합·부적합 사례 등으로 구성됐다.협회 관계자는 "이번 공통심의기준은 다양한 분야별 전문가들이 지혜를 모아 시대의 변화에 부합하는 합리적인 기준을 마련하고자 노력한 결과"라며 "앞으로도 건기식 표시·광고 심의가 내실있게 이뤄지고 지속적으로 발전할 수 있도록 적극 지원하겠다"고 말했다.건강기능식품 표시·광고 공통심의기준’은 각 심의기구 홈페이지에서 열람할 수 있다.2025-06-17 17:06:48강혜경 -
 세계 첫 텔로머레이스 억제제 '라이텔로'...국내 도입 예상5편: First-in-class 텔로머레이스 억제제, 골수이형성증후군 치료제 '라이텔로(Imetelstat)' 라이텔로(Rytelo& 9415;, 성분명: 이메텔스타트, Imetelstat, Geron)는 세계 최초의 올리고뉴클레오타이드 텔로머레이스 억제제(Oligonucleotide telomerase inhibitor)로 2024년 6월 미국 FDA와 2025년 3월 유럽 EMA에서 '적혈구 자극제(ESA)에 반응하지 않거나 효과가 소실되었거나 투여가 불가능한, 수혈 의존성 빈혈이 있으며 8주 동안 적어도 4단위 이상의 적혈구 수혈이 필요한 저위험에서 중간 1단계 위험군의 성인 골수이형성증후군(low-to intermediate-1 risk myelodysplastic syndromes, MDS) 환자 치료'에 승인되었다.대부분의 암세포 및 암 전구세포(cancer progenitor cells)는 높은 텔로머레이스 활성과 텔로미어 유지 능력을 통해 세포가 정상적인 복제 제한 없이 무한히 분열할 수 있는 능력(세포 불사성, cellular immortality)을 가지게 되므로, 텔로머레이스는 암 치료의 유망한 표적 중 하나가 된다이러한 기전에 기반하여 개발된 이메텔스타트는 텔로머레이스를 표적으로 하는 13개 염기 서열의 올리고뉴클레오타이드로, 인간 텔로머레이스 RNA(human telomerase RNA, hTR)의 주형(template) 영역에 선택적으로 결합하여 텔로머레이스 활성을 경쟁적으로 억제함으로써 암세포를 사멸한다.이메텔스타트의 약동학(PK), 약력학(PD), 용량-반응 관계(dose-response relationship), 유효성 및 안전성은 고형암 및 혈액암을 포함한 다양한 종양 모델에서 in vitro, in vivo, 그리고 임상시험을 통해 평가되었다. 특히, 저위험 골수형성이상증후군(LR-MDS) 및 골수증식성 종양을 포함한 혈액질환을 대상으로 한 연구가 집중적으로 수행되었다.핵심 3상 임상시험인 IMerge 연구에 따르면, 이메텔스타트 투여군은 위약군 대비 8주 및 24주 이상에서 적혈구 수혈 비의존성(red blood cell-transfusion independence, RBC-TI)에 도달한 환자의 비율이 통계적으로 유의하게 높았으며, 주요 이상반응으로는 일시적이며 조절 가능한 호중구감소증(neutropenia) 및 혈소판감소증(thrombocytopenia)이 관찰되어, 전반적으로 관리 가능한 안전성 프로파일을 보였다.저위험에서 중간 1단계 위험군의 성인 골수이형성증후군(Low-to intermediate-1 risk myelodysplastic syndromes, MDS)은 무엇인가?골수이형성증후군(MDS)은 혈액 생성 줄기세포의 클론성 이상으로 인해 발생하는 혈액 종양 질환군으로, 골수 내 이형성(dysplasia)과 비효율적인 조혈(hematopoiesis)을 특징으로 한다. 이 질환은 빈혈, 백혈구 감소증, 혈소판 감소증 등의 다양한 혈구감소증(cytopenia)이 나타날 수 있다.일부 MDS 환자는 급성 골수성 백혈병(AML)으로 진행되기도 하여, 임상 경과를 더욱 복잡하게 만든다. MDS 환자의 예후는 매우 다양하며, 염색체 이상 및 혈구감소증의 중증도와 같은 요인에 따라 영향을 받는다. 따라서, MDS 환자의 임상 경과와 치료 반응은 매우 다양하므로, 정확한 예후 분류는 치료 전략 수립 및 예후 예측에 있어 필수적이다.가장 널리 사용되는 예후 평가 시스템은 1997년 제시된 국제 예후 점수 시스템( International Prognostic Scoring System, IPSS)이며, 골수 내 아세포(blast) 비율, 세포유전학적 이상(cytogenetics), 혈구감소증의 수 등 세 가지 지표를 기반으로 환자를 위험(Low), 중간-1위험(Intermediate-1), 중간-2위험(Intermediate-2), 고위험(High)의 네 군으로 분류한다.이 중 저위험에서 중간-1위험군(low-to intermediate-1 risk)은 IPSS 점수 기준으로 0~1.0점에 해당하며, 비교적 안정된 임상 경과를 보이고, 적혈구 자극제(ESA)나 보존적 치료 등의 저강도 요법이 우선적으로 고려된다.2012년에는 기존 IPSS의 한계를 보완하기 위해 개정된 국제 예후 점수 시스템(IPSS-R)이 제안되었다. IPSS-R은 세포유전학적 이상을 5단계로 세분화하고, 골수 아세포 비율, 혈색소 농도, 혈소판 수, 절대 호중구 수 등 보다 정량적인 지표를 반영함으로써 환자를 매우 저위험(very low), 저위험(low), 중간위험(intermediate), 고위험(high), 매우 고위험(very high)의 5단계로 분류한다. 이 중 IPSS-R의 저위험 및 중간위험군은 대체로 기존 IPSS의 저위험 및 중간-1위험군과 대응된다.저위험~중간-1위험군 MDS 환자는 일반적으로 생존 기간이 길고, 급성 골수성 백혈병(AML)으로의 진행 위험이 낮은 편이나, 수혈 의존성 빈혈, 증상성 혈구감소증, 분자 유전학적 이상 유무에 따라 치료 방법의 세분화가 필요하다. 최근에는 유전자 변이 기반의 위험도 분류가 병용되며, 보다 정밀한 예후 예측과 치료 맞춤화에 기여하고 있다.이러한 MDS는 텔로미어(telomere) 단축과 관련된 조혈 줄기세포 기능 저하와 병적 클론의 형성을 특징으로 하며, 일부 클론은 텔로머레이스(telomerase)를 재활성화하여 불사성(immortality)을 획득하고 질환의 진행에 관여한다. 텔로머레이스는 이러한 병태생리적 역할로 인해 MDS에서 유망한 치료 표적이 된다.텔로미어(Telomere)는 어떤 물질인가? 2009년 노벨 생리의학상은 엘리자베스 블랙번(Elizabeth Blackburn), 캐럴 그라이더(Carol Greider), 잭 쇼스택(Jack Szostak)에게 수여되었다. 이들은 염색체 말단에 위치한 특수한 반복 서열 구조인 텔로미어(telomere)와 그 유지에 관여하는 효소인 텔로머레이스(telomerase)를 규명함으로써, 세포 분열 과정에서 유전 정보가 어떻게 안정적으로 보존되는지를 설명하는 데 기여하였다.노벨위원회는 "이들 세 명의 연구는 염색체가 세포 분열 과정 중 퇴화를 방지하고, 완전하게 복제될 수 있는지를 둘러싼 오랜 생물학적 의문에 대한 해답을 제공하였다"고 평가하였다.텔로미어에는 세포의 염색체 말단에 반복적인 DNA 서열이 존재하며, 이는 유전물질의 손상을 방지하고 염색체의 구조적 안정성을 유지하는 역할을 수행한다. 그러나 체세포는 분열을 반복할수록 텔로미어 길이(telomere length)가 '모래시계'처럼 점진적으로 짧아지며, 일정 임계점에 도달하면 세포는 증식을 멈추고 세포 노화(senescence)나 세포자멸사사(apoptosis)를 유도하게 된다(Figure 1).이때 텔로머레이스는 텔로미어의 말단을 연장할 수 있는 효소로 세포의 수명을 연장시키고, 이론적으로는 세포의 불사성(immortality)를 유도할 가능성을 지닌다. 이러한 텔로미어는 생물체의 노화 과정과 직접적으로 연관되어 있고, 또한 대부분의 암세포는 텔로머레이스의 활성을 통해 텔로미어 길이를 유지하거나 연장함으로써 무한 증식 능력을 가지게 된다. 즉, 텔로미어 단축은 세포 노화를 유도하는 반면, 텔로미어 보존은 암세포의 지속적 증식을 가능하게 한다. 따라서, 텔로미어 기능의 조절은 노화 억제 혹은 암 치료를 위한 잠재적 전략으로 제시되고 있다.텔로머레이스(Telomerase)란 무엇인가? 텔로머레이스(Telomerase)는 염색체 말단에 있는 3' 말단 돌출부(3' overhang)에 반복적인 염기서열을 추가하는 기능을 가진 리보핵단백질 복합체(ribonucleoprotein complex)로, 역전사효소(reverse transcriptase) 활성을 갖는다. 3' 말단 돌출부는 이중가닥 DNA 말단에서 한 가닥이 다른 가닥보다 더 길어 돌출된 형태로, 텔로미어 구조에서 텔로머레이스가 인식하고 작용하는 주요 부위이다.텔로머레이스는 자체의 RNA 구성요소인 TERC(telomerase RNA component)를 주형(template)으로 삼아, TERT(telomerase reverse transcriptase)의 역전사 효소 활성을 통해 반복적인 TTAGGG 염기서열을 합성함으로써 염색체 말단의 텔로미어를 연장한다(Figure 2). 인간의 경우, 텔로머레이스는 인간 텔로머레이스 역전사효소(human telomerase reverse transcriptase, hTERT) 유전자에 의해 암호화되는 촉매 소단위(catalytic subunit)와 인간 텔로머레이스 RNA(human telomerase RNA, hTR) 유전자 산물인 RNA 주형(template)을 중심으로 구성된 복합체이다. 여기에 dyskerin, NHP2, NOP10, GAR1 등 다양한 보조 단백질들이 결합하여, 효소 복합체의 구조적 안정성과 기능적 활성을 조절한다.텔로머레이스를 ‘자동차’ 전체에 비유한다면, TERT는 실제로 DNA를 합성하는 역할을 수행하는 ‘엔진’에 해당하며, hTR(또는 TERC)는 어떤 염기서열을 합성할지를 지시하는 ‘설계도’에 해당하는 RNA 주형으로 볼 수 있다.인체 내 약 120여 종의 세포 중 대부분은 텔로미어를 합성하는 효소인 텔로머레이스의 활성을 갖지 않으며, 이로 인해 세포는 분열이 반복될수록 텔로미어가 점진적으로 단축되고, 결국 복제에 따른 세포 노화(replicative senescence)에 도달하게 된다. 반면, 일부 높은 분열 능력을 가진 조직의 세포들은 예외적으로 텔로머레이스 활성을 유지한다.이러한 세포에는 모낭(hair follicle), 구강 편평상피(squamous epithelium), 피부 표피의 기저층(basal layer of epidermis), 제2형 폐포상피세포(type 2 alveolar epithelial cells), 간세포(hepatocytes), 장의 장선(intestinal crypts), 정원세포(spermatogonia) 등이 있다. 이들 세포에서 텔로머레이스 활성이 결여될 경우, 조직의 항상성 유지 및 생식 기능에 중대한 장애가 초래된다.특히, 정자 형성에 관여하는 정원세포(spermatogonia)에서 텔로머레이스 활성이 결여되면, 정자의 텔로미어 길이가 충분히 유지되지 못하고 단축된 상태로 전달된다. 이로 인해 형성된 배아는 텔로미어 단축에 기인한 세포 노화가 조기에 시작되며, 조기 노화(progeria)와 유사한 양상을 보일 수 있다. 실제로 이는 복제 양 돌리(Dolly) 사례에서 관찰된 바 있으며, 단축된 텔로미어가 수명 감소와 밀접하게 연관됨을 시사한다.이는 일반적인 체세포에서는 텔로머레이스 활성이 매우 낮은 수준으로 유지하지만, 생식세포와 줄기세포에서는 해당 효소가 구성효소(constitutive enzyme)로서 지속적으로 발현된다. 구성효소는 소화효소와 같이 항상 일정 수준으로 활성화되어 있는 효소이다.이에 반해 유도효소(inducible enzyme)는 특정 자극(예: 약물, 독성물질 등)에 의해 후천적으로 유도되는 효소이다. 이러한 분류 기준에 따라 텔로머레이스는 생식세포 및 줄기세포에서 구성효소로 기능하며, 암세포에서는 구성효소 및 유도효소적 특성을 보이는 이중적 성격을 가진다고 볼 수 있다.줄기세포 중에서도 배아줄기세포(embryonic stem cells) 및 유도만능줄기세포(induced pluripotent stem cells)는 고도로 안정된 텔로머레이스 활성을 보이며, 이로 인해 세포 분열에 따른 텔로미어의 단축이 거의 발생하지 않고, 복제에 따른 세포 노화에도 이르지 않는다.반면, 중간엽줄기세포(mesenchymal stem cells), 신경줄기세포(neural stem cells), 조혈모세포(hematopoietic stem cells) 등 성체 유래 줄기세포에서는 텔로머레이스 활성이 상대적으로 낮으며, 이로 인해 제한적인 텔로미어 단축이 관찰된다.TERT(Telomerase reverse transcriptase)란 무엇인가? 대부분의 체세포는 약 60~80회의 분열(population doublings) 이후 텔로미어가 임계 길이에 도달하게 되며, 이 시점에서 이중가닥 DNA 절단(double-strand break) 신호가 유도되어 복제에 따른 노화로 전환된다.이러한 현상은 체세포 내에서 텔로머레이스 활성이 거의 존재하지 않기 때문에 발생하는데, 이는 텔로머레이스의 RNA 구성 요소인 TERC(hTR)가 존재하더라도, 촉매 활성을 담당하는 TERT 유전자의 전사가 억제되어 있기 때문이다. 따라서, TERT 발현의 억제는 체세포에서 텔로머레이스 활성이 결핍되는 주요 원인이며, 텔로미어 단축의 분자적 기전으로 작용한다.뿐만 아니라, TERT는 단순한 텔로미어 연장 기능 외에도 텔로미어 말단의 캡핑(capping)과 전체 구조 유지에도 중요한 역할을 한다. 이는 다양한 암종의 약 80~90%에서는 TERT 발현이 재활성화되어 텔로머레이스 활성이 증가되어 있으며, 암세포의 불사화와 밀접하게 연관되어 있다.결과적으로, TERT 발현은 텔로미어 연장과 세포 노화 회피를 통해 암세포 특성이 획득되는 초기 단계에서 결정적인 분자 표지자로 작용한다. 이러한 TERT 발현 유도는 다양한 내& 8226;외부 요인 중 유전자 불안정성과 돌연변이가 가장 대표적인 기전으로 제시되고 있다.암의 발생 과정에서 텔로미어 길이의 보존이 빈번히 동반되며, 이는 주로 인간 텔로머레이스 역전사효소(hTERT)의 발현 증가에 따른 텔로머레이스 활성의 재개로 설명된다. 따라서 TERT의 발현 조절 기전은 텔로머레이스 기반 항암 치료법의 핵심 표적으로 주목받고 있으며, 암세포 특이적 바이오마커로서의 임상적 활용 가능성 또한 높다.텔로머레이스와 암과의 관계는 어떠한가? 텔로머레이스의 비정상적인 재활성화는 암세포에서 흔히 관찰되는데, 이는 텔로미어 단축으로 유도되는 세포자멸사를 회피하고 무한 증식 능력을 획득하는 데 핵심적인 기전으로 작용한다. 실제로, 전체 고형암 및 혈액암의 약 90% 이상에서 텔로머레이스 활성이 현저히 증가되어 있음이 관찰된다.여러 암 조직 생검에서 텔로머레이스 활성의 증가가 종양의 병기 및 악성도와 유의한 상관관계를 보이는 반면, 대부분의 정상 성인 조직에서는 텔로머레이스 활성이 거의 검출되지 않으며, 일부 조혈모세포나 면역세포에서만 일시적으로 나타나는 것으로 알려져 있다.이는 암세포 및 암전구세포에서 공통적으로 관찰되는 높은 수준의 텔로머레이스 발현과 텔로미어 유지 현상을 억제하여 암세포의 증식을 제한하는 치료 방법이 된다.특히, RNA 기반 치료법은 텔로머레이스의 RNA 구성요소인 hTR 또는 hTERT mRNA를 표적으로 하여 효소 활성을 간접적으로 억제하는 방식으로 주목받고 있다. 이 중 안티센스 올리고뉴클레오타이드(antisense oligonucleotides, ASO) 및 RNA 간섭(small interfering RNA, siRNA) 기술은 텔로머레이스 기능을 선택적으로 차단할 수 있는 새로운 접근법이다.대표적 예로는 이멜스타트(Imetelstat)가 있으며, 이는 인간 텔로머레이스 RNA(hTR)의 주형 영역에 상보적으로 결합하는 리간드 결합형 ASO로 설계되어, 텔로미어 연장 과정을 억제함으로써 암세포의 증식 억제를 유도한다. 이와 같은 RNA 기반 접근은 텔로머레이스 억제를 통한 항암 치료의 새로운 패러다임을 제시하며, 표적 치료제 개발에 있어 중요한 진전을 이끌고 있다.텔로머레이스 억제를 통한 항암 치료 전략은? 텔로머레이스를 표적으로 한 항암제 개발은 다양한 작용기전을 바탕으로 다방면에서 진행되고 있으며, 크게 RNA 기반 억제제, 전사 억제 화합물, G-사중나선 안정화제, 그리고 면역치료 백신 전략으로 구분할 수 있다.1. RNA 기반 억제제 가장 활발히 연구되고 있는 접근은 안티센스 올리고뉴클레오타이드(ASO) 또는 RNA 간섭(siRNA) 기술을 활용하여 텔로머레이스 RNA 구성요소(hTR 또는 TERC)를 표적으로 하는 전략이다. 이들 억제제는 텔로머레이스 복합체 내의 RNA 주형에 상보적으로 결합함으로써 효소 활성을 억제하거나, RNase H 의존적 분해를 유도하여 텔로머레이스 기능을 근본적으로 차단한다.대표적 약제인 이멜스타트(Imetelstat)는 티오포스포라마이드(thio-phosphoramidate) 변형을 적용한 ASO로, hTR의 템플릿 영역에 결합하여 텔로미어 연장을 저해한다.2. hTERT 전사 억제 저분자 화합물 이 저분자 화합물은 텔로머레이스의 촉매 소단위인 hTERT 유전자의 전사를 직접 억제하는 방식으로, 프로모터 영역 조절 또는 후성유전학적 메커니즘을 통해 유전자 발현 자체를 낮춘다. 일부 저분자 화합물은 hTERT 단백질에 직접 결합하여 효소 활성을 차단한다. 식물 유래 플라보노이드(예: genistein)가 TERT 전사를 억제하는 기능이 보고된 바 있으나 낮은 선택성과 잠재적인 세포독성으로 인해 임상 적용에는 제한이 있다.3. G-사중나선(G-quadruplex) 안정화제 이 안정화제는 텔로미어 말단에서 형성되는 G-사중나선 구조를 안정화시켜 텔로머레이스의 접근을 물리적으로 차단하는 방식이다. 해당 구조는 G-rich 반복 서열에서 자연적으로 형성되며, 일부 저분자 화합물은 이 구조에 특이적으로 결합하여 G-quadruplex 형태의 유지 및 안정화를 유도한다.이 방법은 효소가 아닌 기질을 표적으로 한다는 점에서 기존 억제제와 구별되며, 비교적 빠른 약효 발현이 가능하다. 그러나 G-rich 서열이 텔로미어 외에도 다양한 유전자의 조절부위에 존재하기 때문에, 표적 특이성 확보가 주요 과제로 남아 있다.4. 텔로머레이스를 항원으로 활용한 면역치료 텔로머레이스를 면역계의 표적으로 활용하는 전략도 개발되고 있다. 이는 hTERT 유래 펩타이드를 기반으로 하는 항암 백신을 통해, 텔로머레이스를 발현하는 종양세포를 면역세포가 인식하고 제거하도록 유도한다. 비소세포폐암(NSCLC), 췌장암 등 다양한 고형암에서 임상시험이 진행되고 있으며, 면역기억 반응을 통한 재발 억제 효과가 기대된다. 다만, 환자의 HLA 유형 및 종양미세환경(TME)에 따라 치료 반응의 편차가 존재하여, 정밀한 환자 선별 전략이 병행되어야 한다.이와 같이 텔로머레이스 억제 전략은 암세포 특이성이 높고 장기적인 종양 억제 효과를 유도할 수 있다는 점에서 유망한 접근이다. 그러나 기전상 텔로미어 길이의 점진적 단축을 필요로 하므로, 치료 효과 발현까지 수 주에서 수 개월이 소요되는 경향이 있다. 또한, 일부 암에서는 텔로머레이스 비의존적인 대체적 길이 조절(ALT, alternative lengthening of telomeres) 경로가 활성화되어 있어 단독요법으로는 제한적일 수 있다.이러한 한계를 극복하기 위해, 최근에는 DNA 손상 유도제, 면역관문억제제(PD-1/PD-L1 억제제), PARP 억제제 등과의 병용요법이 시도되고 있다. 또한 텔로머레이스 발현 수준, 텔로미어 길이 상태, ALT 경로 활성 여부 등을 고려한 환자 맞춤형 정밀의학적 접근이 병행됨으로써, 텔로머레이스 억제제의 임상적 유용성은 점차 확대되고 있다.뉴클레오타이드(Nucleotide)와 합성 올리고뉴클레오타이드의 차이는? 뉴클레오타이드는 모든 생명체에 보편적으로 존재하는 저분자 유기 화합물로, DNA와 RNA와 같은 핵산의 기본 단위이며 에너지 전달(ATP, GTP), 세포 신호전달(cAMP, cGMP), 효소 보조인자(NAD& 8314;, FAD) 등의 생리적 기능에 필수적인 역할을 수행한다. 이러한 분자는 세포 내에서 de novo 합성 경로 또는 재활용 경로(salvage pathway)를 통해 지속적으로 생성되며, 생명 유지에 핵심적인 역할을 한다.이에 반해, 올리고뉴클레오타이드는 일반적으로 몇 개에서 수십 개의 뉴클레오타이드가 공유결합으로 연결된 짧은 핵산 서열로, 인공적으로 합성된 생체분자이다. 자연적으로는 microRNA나 small nuclear RNA와 같은 일부 예외적인 경우를 제외하면 생체 내에서 잘 합성되지 않으며, 주로 화학적으로 합성되어 특정 유전 서열의 인식이나 분자 기능의 조절을 목적으로 활용된다.합성 올리고뉴클레오타이드는 분자생물학, 진단, 치료, 유전자 조작 등 다양한 분야에서 핵심 도구로 활용되고 있으며, 기능, 표적, 화학적 변형에 따라 , 다음과 같이 분류된다.첫째, 기능적 측면에서 ▲ mRNA 또는 pre-mRNA에 결합하여 유전자 발현을 억제하거나 RNA 스플라이싱을 조절하는 안티센스 올리고뉴클레오타이드(antisense oligonucleotide, ASO), ▲ RNA 간섭(RNAi)을 유도하여 표적 mRNA의 분해를 유도하는 소간섭 RNA(siRNA) 또는 마이크로 RNA(miRNA) 유사체, ▲ 고특이적으로 단백질에 결합하여 기능을 저해하거나 조절하는 압타머(aptamer), ▲ CRISPR 시스템에서 유전자 편집을 유도하는 가이드 RNA(guide RNA, gRNA), ▲ 전사인자와 결합하여 표적 유전자 조절을 간섭하는 디코이(decoy), ▲ PCR, qPCR, 유전자 탐지 등 핵산 분석 기술에 사용하는 프라이머(primer) / 프로브(probe) 등으로 분류된다.둘째, 표적 및 작용기전에 따라 ▲ DNA, ▲ mRNA, ▲ pre-mRNA, 또는 단백질 등 다양한 분자에 작용할 수 있으며, 그 기전은 전사 억제, 번역 차단, RNA 스플라이싱 조절, 단백질-핵산 상호작용 차단 등으로 확장된다.셋째, 화학 구조적 변형 측면에서 천연형(natural-type) 외에도 약물 안정성 및 효율성을 개선하기 위한 다양한 화학적 변형이 도입된다. 대표적으로 ▲ 인산기 산소를 황으로 치환하여 핵산분해효소 내성 증가를 위한 phosphorothioate(PS), ▲ 리보스의 2′ 위치에 화학기 추가로 결합력과 안정성 증가를 위한 2′-O-methyl RNA 및 2′-fluoro RNA, ▲ 리보스 고정을 통해 고결합 친화성 및 특이성 확보한 locked nucleic acid(LNA), ▲ 간세포 타깃팅 또는 세포 내 전달력 향상을 위한 GalNAc 또는 지질을 접합시킨 conjugated oligonucleotide 등이 있으며, 이는 체내 안정성, 표적 결합력, 약물 전달 효율성을 향상시키는 데 기여한다.요약하면, 뉴클레오타이드는 생명체 내에서 합성되는 주요 생리활성 분자인 반면, 올리고뉴클레오타이드는 외부에서 합성되어 생체 내 특정 유전자나 분자 기전을 정교하게 조절하기 위한 인공 핵산 서열이라는 점에서, 양자는 생성 방식과 생리적 존재 양상에서 본질적으로 다르다. 그럼에도 불구하고, 올리고뉴클레오타이드는 자연계 핵산의 기능을 모방하거나 확장함으로써 차세대 핵산 기반 치료제 및 진단 기술의 핵심 플랫폼으로 부상하고 있다.ASO(Antisense Oligonucleotide, 안티센스 올리고뉴클레오타이드)란? ASO는 mRNA를 표적으로 설계된 짧은 합성 단일가닥 DNA 분자로, 특정 mRNA 서열과 상보적으로 결합함으로써 유전자 발현을 억제하거나 조절하는 기능을 수행한다(Figure. 3).ASO는 비교적 간단한 화학 구조를 기반으로 하면서도, 전사체의 분해 유도, RNA 스플라이싱 (splicing) 조절, 번역 억제 등 다양한 작용기전을 통해 유전 정보의 흐름을 정교하게 제어할 수 있는 장점을 가진다.ASO의 작용기전은 화학적 변형 방식과 결합 표적에 따라 다양하게 구분된다. 대표적으로 RNase H 매개 분해는 ASO가 표적 mRNA와 이중가닥을 형성한 후, 세포 내 RNase H 효소에 의해 해당 mRNA가 분해되어 단백질 생성을 원천적으로 차단하는 기전이다.또한, 스플라이싱 조절용 ASO는 pre-mRNA의 엑손/인트론 경계부에 결합하여, 엑손 스키핑(skipping) 또는 보존을 유도함으로써 단백질의 구조와 기능을 변형시킬 수 있다. 이 외에도 번역 개시 억제, mRNA 안정성 저해 등 다양한 방식으로 작용이 가능하다.이러한 특성을 바탕으로, ASO는 기존 소분자 화합물이나 단백질 기반 치료제와 달리 기능 상실(loss-of-function) 혹은 기능 획득(gain-of-function) 유전자 돌연변이 모두를 정교하게 조절할 수 있다.그러나 ASO 치료제는 면역반응 유발, 비표적 결합(off-target effect), 체내 약물 전달 효율 등의 한계를 지니고 있으며, 이를 극복하기 위해 phosphorothioate 치환, 2′-O-methyl 및 LNA 변형, GalNAc 결합을 통한 간세포 표적화, 지질 나노입자 기반 전달체 등 다양한 기술적 발전이 이루어지고 있다.이러한 발전은 ASO의 치료적 효능을 향상시키는 데 핵심적인 기여를 하고 있으며, ASO 기반 핵산 치료제가 차세대 정밀의학 기반의 분자표적 치료제로 자리매김할 수 있는 가능성을 높이고 있다.텔로머레이스 표적 올리고뉴클레오타이드(Telomerase-targeted oligonucleotide, TTO)란? TTO는 표적 핵산 서열에 상보적으로 결합하는 구조를 가지면서도, 기존의 ASO와는 본질적으로 다른 작용기전을 가진다. 즉 일반적인 ASO는 mRNA의 분해(RNase H 의존적 경로) 또는 스플라이싱 조절을 통해 단백질 생성을 억제하지만, TTO는 hTR의 템플릿 서열에 직접 결합함으로써 텔로머레이스 효소 복합체의 활성 부위를 차단한다. 이는 효소의 기질 인식 및 촉매 반응 자체를 방해하는 비정형(non-canonical) ASO로 분류된다.이러한 TTO는 효소 작용 자체의 차단을 통해 효소 기능 차단(enzyme activity inhibition)이라는 새로운 패러다임을 제공한다. 특히 텔로머레이스 활성이 높은 암세포에서 선택적으로 작용함으로써, 정상세포에 대한 영향을 최소화하면서 암 특이적 억제 효과를 유도할 수 있다.대표적인 TTO로는 이메텔스타트(Imetelstat)가 있으며, 이는 hTR의 템플릿 영역에 상보적으로 결합하는 티오인산화(thio-phosphoramidate) 올리고뉴클레오타이드로 설계되었다.이메텔스타트는 어떤 약제인가? 이메텔스타트(Imetelstat, 제품명: 라이텔로 정맥주사, Rytelo®)는 텔로머레이스를 직접 표적으로 하는 최초의 올리고뉴클레오타이드 기반 치료제로, 2024년 미국 FDA로부터 승인받은 이후 골수이형성증후군(MDS) 치료 영역에서 새로운 치료 축으로 부상하고 있다. 이 약제의 승인 적응증은 "8주간 4단위 이상의 적혈구 수혈이 필요한 수혈 의존성 빈혈을 가진 저위험~중간-1 위험군 MDS 성인 환자 중, 적혈구생성자극제(ESA)에 반응하지 않거나 반응이 소실되었거나, 투여가 불가능한 경우"이다.이메텔스타트는 기존의 ASO와는 구별되는 비정형 ASO로 분류되며, 비정상적인 텔로머레이스 활성을 보이는 악성 조혈모세포(HSCs) 및 전구세포(HPCs)를 선택적으로 억제함으로써 병적 클론의 제거와 정상 조혈 기능의 회복을 유도하는 질환 수정형(disease-modifying) 치료 제이다.분자 구조적으로, 이메텔스타트는 13개의 뉴클레오타이드로 구성된 단일가닥 DNA 서열이며, 티오인산화(thio-phosphoramidate) 변형을 통해 핵산분해효소(nuclease) 저항성, 수용성, 대사적 안정성 등의 약물학적 특성이 향상되었다. 또한 5′ 말단에 팔미토일기(palmitoyl group)가 결합되어 소수성을 증가시켜 세포막 투과성 및 세포 내 유지성을 강화하며, 별도의 형질전환 과정 없이도 세포 내 작용이 가능하도록 설계되었다.전임상 연구에서는 이메텔스타트의 약물 노출과 텔로머레이스 억제 간의 명확한 약력학적 상관성이 확인되었고, 텔로머레이스 활성을 50% 이상 억제하는 수준의 약리 효과가 임상적으로 확보 가능한 범위 내에 있음이 입증되었다. 또한, 골수증식성 질환 모델(예: 본태성 혈소판증, 골수섬유증, 급성 골수성 백혈병 등)에서는 시험관 내(in vitro) 및 생체 내(in vivo) 실험 모두에서 강력한 항종양 활성을 나타냈다.특히 저위험 MDS 환자에서 이메텔스타트는 텔로미어 단축, hTERT 과발현, 분화 억제 등으로 특징지어지는 병적 조혈모세포 및 전구세포를 선택적으로 제거함으로써, 정상 조혈의 회복과 함께 적혈구 수혈 비의존 기간(RBC-TI)의 연장, 혈색소 수치의 향상, 염색체 이상 클론 및 돌연변이 부담의 감소를 유도하였다.아울러, 이메텔스타트는 면역회피 특성을 가진 악성 클론에서도 항암 활성을 유지함으로써, 기존 면역항암제 또는 세포독성 항암제에 비해 임상적 적용 가능성이 높다. 현재 진행 중인 다수의 임상시험 결과에 따라, MDS뿐 아니라 골수섬유증(myelofibrosis), 기타 혈액암 영역으로의 적응증 확장 가능성도 제시되고 있다.이메텔스타트의 약리 기전은? 이메텔스타트는 TERT-targeting telomerase complex inhibtor 또는 RNA-template targeting telomerase inhibitor로, 인간 텔로머라제의 RNA 구성 요소(hTR)의 주형 영역에 상보적으로 결합하여 텔로머레이스 복합체의 활성 부위에서 기질 결합 및 연장을 직접 차단한다. 즉 hTR의 주형 서열(3′-CAAUCCCAAUC-5′)에 상보적인 염기서열(5′-palmitate-TAGGGTTAGACAA-NH₂-3′)이 결합함으로써, 텔로머레이스 효소의 활성을 억제하여 텔로미어 말단에 반복 서열을 추가하는 기능을 경쟁적으로 차단한다. 이로 인해 암세포 내에서의 텔로미어 길이가 점진적으로 짧아지며, 결국 세포 노화 또는 세포자멸사를 유도하게 된다(Figure 4). 골수이형성증후군(MDS) 및 악성 줄기세포 및 전구세포에서 텔로머레이스 활성 및 인간 텔로머레이스 역전사효소(hTERT) RNA 발현이 증가한 것으로 보고되었다. 이에 여러 연구에서 이메텔스타트 치료가 텔로미어 길이 감소, 악성 줄기세포 및 전구세포의 증식 감소, 그리고 세포자멸사를 유도함으로써 세포 증식 억제 및 수명 단축 효과를 나타낸 것으로 보고되었다.또한, 이 약제는 텔로머레이스의 촉매 소단위인 hTERT의 발현을 억제함으로써 효소 활성을 이중적으로 저해하는데, 이 hTERT는 텔로머레이스 활성을 조절하는 주요 속도 제한 인자(rate-limiting component)로 알려져 있다.이러한 이멜스타트의 작용 기전은 항원-항체 반응이나 면역세포 활성화를 기반으로 하는 기존 면역항암제와는 달리, 종양 세포의 분열 및 생존을 유지하는 내재적 기전인 텔로머레이스 의존성을 직접 차단한다는 점에서 근본적인 차별성을 갖는다.이멜스타트(RYTELO& 9415;) 3상 임상은 어떻게 진행되었나? 이메텔스타트의 임상적 유효성은 IMerge 3상 연구를 통해 입증되었다. 본 연구는 무작위배정, 이중눈가림, 위약대조, 다기관 임상시험으로 설계되었으며, 저위험 또는 중간-1위험군 골수이형성증후군(MDS) 환자 중 수혈 의존성을 보이는 성인 178명을 대상으로 시행되었다. 환자 등록 기준은 무작위배정 16주 전의 8주간 기간 동안 적어도 4단위 이상의 적혈구 수혈 필요 이력이 있는 경우로 정의되었다.등록 환자들은 모두 적혈구생성자극제(ESA)에 반응이 없었거나 반응이 소실되었거나, ESA 투여가 적절하지 않다고 판단된 경우였다. 주요 포함 기준에는 절대 호중구 수치 ≥ 1.5 × 10& 8313;/L, 혈소판 수 ≥ 75 × 10& 8313;/L이 포함되었으며, del(5q) 염색체 이상 보유자, 레날리도마이드(Lenalidomide) 또는 아자시티딘(Azacitidine)과 데시타빈(Decitabine) 같은 저메틸화제(hypomethylating agents, HMA) 치료 이력이 있는 환자는 제외되었다.무작위배정은 2:1 비율로 수행되어, RYTELO 7.1 mg/kg 정맥주사군(n=118) 또는 위약군(n=60)에 배정되었으며, 28일 주기(cycle)로 반복 투여되었다. 치료는 질병 진행, 용인할 수 없는 독성, 또는 환자의 자의적 중단 시점까지 지속되었다. 무작위배정은 기존 RBC 수혈 부담 및 IPSS 위험군 등급을 기준으로 계층화되었다. 모든 환자에게는 필요 시 적혈구 수혈을 포함한 지지요법(supportive care)이 병행 제공되었다.평가 기간은 RYTELO 투여군에서 중앙 추적기간 19.5개월(범위: 1.4& 8211;36.2개월), 위약군에서 17.5개월(범위: 0.7& 8211;34.3개월)이었으며, 주요 유효성 평가 변수는 적혈구 수혈 독립(RBC transfusion independence, RBC-TI) 달성 비율이었다. 이는 무작위배정 이후부터 차기 항암 치료 개시 전까지의 기간 중 연속된 8주(≥56일) 또는 연속된 24주(≥168일) 동안 적혈구 수혈이 전혀 이루어지지 않은 경우로 정의되었다.그 결과, 8주 이상 RBC-TI 도달률은 RYTELO 군에서 39.8%(95% CI: 30.9& 8211;49.3)로, 위약군의 15.0%(95% CI: 7.1& 8211;26.6) 대비 통계적으로 유의하게 높았다(p < 0.001). 또한 24주 이상 RBC-TI 도달률 역시 RYTELO 군에서 28.0% (95% CI: 20.1& 8211;37.0)로, 위약군 3.3% (95% CI: 0.4& 8211;11.5)와 비교하여 유의한 차이를 보였다(p < 0.001). 이러한 결과는 RYTELO가 ESA 불응 또는 부적합 환자군에서 수혈 의존성을 유의하게 줄이고, 적혈구계 조혈 회복을 유도할 수 있는 잠재력을 입증하는 것으로 해석된다.안전성 측면은 RYTELO 군에서 위약군 대비 ≥10% 이상, ≥5% 차이를 보인 주요 이상반응은 혈소판 감소, 백혈구 감소, 호중구 감소, AST/ALT/ALP 상승, 피로, 부분 트롬보플라스틴 시간 연장, 관절/근육통, COVID-19 감염, 두통 등이었다.따라서, RYTELO는 저위험 MDS 환자에서 임상적으로 의미 있는 수혈 독립 향상을 유도하였으며, 전반적으로 관리 가능한 안전성 프로파일을 보였다. 권장 투여 용량은 7.1 mg/kg이며, 4주마다 2시간에 걸쳐 정맥 투여한다. 이멜스타트의 앞으로의 예상은? 골수이형성증후군(MDS)은 조혈모세포의 분화 및 성숙에 결함이 생겨 비정상적 조혈과 말초 혈구감소증을 유발하는 이질적인 클론성 조혈장애이다. 특히 저위험군 MDS 환자에서는 만성적인 적혈구 수혈 의존성 빈혈이 주요 임상 양상으로 나타나며, 삶의 질 저하 및 철분 과부하에 의한 이차적 장기 손상이 주요 합병증으로 작용한다.현재까지 이들 환자에서 사용 가능한 치료제로는 적혈구생성자극제(ESA) 및 저메틸화제(HMA) 등이 있으나, 반응률의 한계와 장기 치료 효과에 대한 의문이 지속적으로 제기되고 있다.텔로머레이스는 텔로미어 길이를 유지하여 세포의 분열 한계를 극복하게 하는 핵심 효소로, 대부분의 암세포 및 악성 조혈모세포에서 비정상적으로 활성이 증가되어 있는 것이 특징이다. 이러한 활성을 선택적으로 억제함으로써 병적 조혈세포의 증식을 제한하고 정상 조혈을 회복시키는 접근은 질환의 근본 기전을 타겟으로 하는 질환 수정형(disease-modifying) 치료전략으로 주목받고 있다.이메텔스타트(Imetelstat)는 인간 텔로머레이스 복합체(hTERT/hTR)에 직접 결합하여 활성을 경쟁적으로 억제하는 first-in-class 올리고뉴클레오타이드 기반 치료제로, 텔로미어 유지 능력을 상실하게 하여 세포 자멸사 및 증식 억제를 유도한다. 특히 병적 조혈모세포(HSCs/HPCs)와 백혈병 줄기세포(LSCs)에 선택적으로 작용하며, 정상 조혈세포에 대한 영향은 제한적으로 보고되고 있다.IMerge 3상 임상시험에서 이메텔스타트는 ESA에 반응하지 않거나 부적합한 저위험~중간-1 위험군 MDS 환자를 대상으로 통계적으로 유의한 적혈구 수혈 독립 효과를 입증하였다. 8주 이상 수혈 독립률(RBC-TI)은 이메텔스타트군에서 39.8%, 위약군에서 15.0%로 나타났으며, 24주 이상 수혈 독립률도 각각 17.8%와 1.6%로 유의한 차이를 보였다. 이는 기존 치료옵션에 반응하지 않는 환자 집단에 있어 새로운 치료 패러다임을 제시한 근거로 평가된다.다만, 현재 이메텔스타트는 저위험 MDS + ESA 실패 + 수혈 의존성 빈혈이라는 제한된 적응증으로 승인되어 있으며, TP53 돌연변이나 고위험군 MDS는 제외 대상에 해당된다. 또한 치료 효과 발현까지 수 주에서 수개월이 소요되며, 호중구감소증(72%) 및 혈소판감소증(65%) 등 고빈도의 혈액학적 이상반응이 동반될 수 있다는 점은 임상적 고려가 필요하다.그럼에도 불구하고, 텔로머레이스라는 근원적 분자 표적을 겨냥한 이메텔스타트는 기존 화학요법 및 면역조절제와는 차별화된 기전을 통해 조혈계 악성질환에 있어 정밀의학적 치료 전략으로서의 가능성을 보여주고 있다. 이미 미국 및 유럽에서 승인된 약제로서, 향후 국내 도입과 더불어 적응증 확대, 병용요법, 고위험 환자군에서의 임상적 검토가 필요할 것으로 예상한다.참고문헌 1. Alexander Vaiserman, Dmytro Krasnienkov “Telomere Length as a Marker of Biological Age: State-of-the-Art, Open Issues, and Future Perspectives” Front. Genet. 11:630186(2021). 2. Virginia Boccardi “Aging, Cancer, and Inflammation: The Telomerase Connection” J. Mol. Sci. 2024, 25(15), 8542. 3. Virginia Boccardi, and Luigi Marano “Aging, Cancer, and Inflammation: The Telomerase Connection” Int. J. Mol. Sci. 2024, 25, 8542. 4. Zachary Schrank, Nabiha Khan, Chike Osude, Sanjana Singh et al. “Oligonucleotides Targeting Telomeres and Telomerase in Cancer” Molecules 2018, 23, 2267. 5. Ashley L. Lennoxm, Fei Huang, Melissa Kelly Behrs, Mario Gonz& 225;lez-Sales et al. “Imetelstat, a novel, first-in-class telomerase inhibitor:Mechanism of action” Clin Transl Sci. 2024;17:e70076 6. 기타 인터넷 자료(보도 자료, 제품 설명서 등)2025-06-13 06:24:02최병철 박사
세계 첫 텔로머레이스 억제제 '라이텔로'...국내 도입 예상5편: First-in-class 텔로머레이스 억제제, 골수이형성증후군 치료제 '라이텔로(Imetelstat)' 라이텔로(Rytelo& 9415;, 성분명: 이메텔스타트, Imetelstat, Geron)는 세계 최초의 올리고뉴클레오타이드 텔로머레이스 억제제(Oligonucleotide telomerase inhibitor)로 2024년 6월 미국 FDA와 2025년 3월 유럽 EMA에서 '적혈구 자극제(ESA)에 반응하지 않거나 효과가 소실되었거나 투여가 불가능한, 수혈 의존성 빈혈이 있으며 8주 동안 적어도 4단위 이상의 적혈구 수혈이 필요한 저위험에서 중간 1단계 위험군의 성인 골수이형성증후군(low-to intermediate-1 risk myelodysplastic syndromes, MDS) 환자 치료'에 승인되었다.대부분의 암세포 및 암 전구세포(cancer progenitor cells)는 높은 텔로머레이스 활성과 텔로미어 유지 능력을 통해 세포가 정상적인 복제 제한 없이 무한히 분열할 수 있는 능력(세포 불사성, cellular immortality)을 가지게 되므로, 텔로머레이스는 암 치료의 유망한 표적 중 하나가 된다이러한 기전에 기반하여 개발된 이메텔스타트는 텔로머레이스를 표적으로 하는 13개 염기 서열의 올리고뉴클레오타이드로, 인간 텔로머레이스 RNA(human telomerase RNA, hTR)의 주형(template) 영역에 선택적으로 결합하여 텔로머레이스 활성을 경쟁적으로 억제함으로써 암세포를 사멸한다.이메텔스타트의 약동학(PK), 약력학(PD), 용량-반응 관계(dose-response relationship), 유효성 및 안전성은 고형암 및 혈액암을 포함한 다양한 종양 모델에서 in vitro, in vivo, 그리고 임상시험을 통해 평가되었다. 특히, 저위험 골수형성이상증후군(LR-MDS) 및 골수증식성 종양을 포함한 혈액질환을 대상으로 한 연구가 집중적으로 수행되었다.핵심 3상 임상시험인 IMerge 연구에 따르면, 이메텔스타트 투여군은 위약군 대비 8주 및 24주 이상에서 적혈구 수혈 비의존성(red blood cell-transfusion independence, RBC-TI)에 도달한 환자의 비율이 통계적으로 유의하게 높았으며, 주요 이상반응으로는 일시적이며 조절 가능한 호중구감소증(neutropenia) 및 혈소판감소증(thrombocytopenia)이 관찰되어, 전반적으로 관리 가능한 안전성 프로파일을 보였다.저위험에서 중간 1단계 위험군의 성인 골수이형성증후군(Low-to intermediate-1 risk myelodysplastic syndromes, MDS)은 무엇인가?골수이형성증후군(MDS)은 혈액 생성 줄기세포의 클론성 이상으로 인해 발생하는 혈액 종양 질환군으로, 골수 내 이형성(dysplasia)과 비효율적인 조혈(hematopoiesis)을 특징으로 한다. 이 질환은 빈혈, 백혈구 감소증, 혈소판 감소증 등의 다양한 혈구감소증(cytopenia)이 나타날 수 있다.일부 MDS 환자는 급성 골수성 백혈병(AML)으로 진행되기도 하여, 임상 경과를 더욱 복잡하게 만든다. MDS 환자의 예후는 매우 다양하며, 염색체 이상 및 혈구감소증의 중증도와 같은 요인에 따라 영향을 받는다. 따라서, MDS 환자의 임상 경과와 치료 반응은 매우 다양하므로, 정확한 예후 분류는 치료 전략 수립 및 예후 예측에 있어 필수적이다.가장 널리 사용되는 예후 평가 시스템은 1997년 제시된 국제 예후 점수 시스템( International Prognostic Scoring System, IPSS)이며, 골수 내 아세포(blast) 비율, 세포유전학적 이상(cytogenetics), 혈구감소증의 수 등 세 가지 지표를 기반으로 환자를 위험(Low), 중간-1위험(Intermediate-1), 중간-2위험(Intermediate-2), 고위험(High)의 네 군으로 분류한다.이 중 저위험에서 중간-1위험군(low-to intermediate-1 risk)은 IPSS 점수 기준으로 0~1.0점에 해당하며, 비교적 안정된 임상 경과를 보이고, 적혈구 자극제(ESA)나 보존적 치료 등의 저강도 요법이 우선적으로 고려된다.2012년에는 기존 IPSS의 한계를 보완하기 위해 개정된 국제 예후 점수 시스템(IPSS-R)이 제안되었다. IPSS-R은 세포유전학적 이상을 5단계로 세분화하고, 골수 아세포 비율, 혈색소 농도, 혈소판 수, 절대 호중구 수 등 보다 정량적인 지표를 반영함으로써 환자를 매우 저위험(very low), 저위험(low), 중간위험(intermediate), 고위험(high), 매우 고위험(very high)의 5단계로 분류한다. 이 중 IPSS-R의 저위험 및 중간위험군은 대체로 기존 IPSS의 저위험 및 중간-1위험군과 대응된다.저위험~중간-1위험군 MDS 환자는 일반적으로 생존 기간이 길고, 급성 골수성 백혈병(AML)으로의 진행 위험이 낮은 편이나, 수혈 의존성 빈혈, 증상성 혈구감소증, 분자 유전학적 이상 유무에 따라 치료 방법의 세분화가 필요하다. 최근에는 유전자 변이 기반의 위험도 분류가 병용되며, 보다 정밀한 예후 예측과 치료 맞춤화에 기여하고 있다.이러한 MDS는 텔로미어(telomere) 단축과 관련된 조혈 줄기세포 기능 저하와 병적 클론의 형성을 특징으로 하며, 일부 클론은 텔로머레이스(telomerase)를 재활성화하여 불사성(immortality)을 획득하고 질환의 진행에 관여한다. 텔로머레이스는 이러한 병태생리적 역할로 인해 MDS에서 유망한 치료 표적이 된다.텔로미어(Telomere)는 어떤 물질인가? 2009년 노벨 생리의학상은 엘리자베스 블랙번(Elizabeth Blackburn), 캐럴 그라이더(Carol Greider), 잭 쇼스택(Jack Szostak)에게 수여되었다. 이들은 염색체 말단에 위치한 특수한 반복 서열 구조인 텔로미어(telomere)와 그 유지에 관여하는 효소인 텔로머레이스(telomerase)를 규명함으로써, 세포 분열 과정에서 유전 정보가 어떻게 안정적으로 보존되는지를 설명하는 데 기여하였다.노벨위원회는 "이들 세 명의 연구는 염색체가 세포 분열 과정 중 퇴화를 방지하고, 완전하게 복제될 수 있는지를 둘러싼 오랜 생물학적 의문에 대한 해답을 제공하였다"고 평가하였다.텔로미어에는 세포의 염색체 말단에 반복적인 DNA 서열이 존재하며, 이는 유전물질의 손상을 방지하고 염색체의 구조적 안정성을 유지하는 역할을 수행한다. 그러나 체세포는 분열을 반복할수록 텔로미어 길이(telomere length)가 '모래시계'처럼 점진적으로 짧아지며, 일정 임계점에 도달하면 세포는 증식을 멈추고 세포 노화(senescence)나 세포자멸사사(apoptosis)를 유도하게 된다(Figure 1).이때 텔로머레이스는 텔로미어의 말단을 연장할 수 있는 효소로 세포의 수명을 연장시키고, 이론적으로는 세포의 불사성(immortality)를 유도할 가능성을 지닌다. 이러한 텔로미어는 생물체의 노화 과정과 직접적으로 연관되어 있고, 또한 대부분의 암세포는 텔로머레이스의 활성을 통해 텔로미어 길이를 유지하거나 연장함으로써 무한 증식 능력을 가지게 된다. 즉, 텔로미어 단축은 세포 노화를 유도하는 반면, 텔로미어 보존은 암세포의 지속적 증식을 가능하게 한다. 따라서, 텔로미어 기능의 조절은 노화 억제 혹은 암 치료를 위한 잠재적 전략으로 제시되고 있다.텔로머레이스(Telomerase)란 무엇인가? 텔로머레이스(Telomerase)는 염색체 말단에 있는 3' 말단 돌출부(3' overhang)에 반복적인 염기서열을 추가하는 기능을 가진 리보핵단백질 복합체(ribonucleoprotein complex)로, 역전사효소(reverse transcriptase) 활성을 갖는다. 3' 말단 돌출부는 이중가닥 DNA 말단에서 한 가닥이 다른 가닥보다 더 길어 돌출된 형태로, 텔로미어 구조에서 텔로머레이스가 인식하고 작용하는 주요 부위이다.텔로머레이스는 자체의 RNA 구성요소인 TERC(telomerase RNA component)를 주형(template)으로 삼아, TERT(telomerase reverse transcriptase)의 역전사 효소 활성을 통해 반복적인 TTAGGG 염기서열을 합성함으로써 염색체 말단의 텔로미어를 연장한다(Figure 2). 인간의 경우, 텔로머레이스는 인간 텔로머레이스 역전사효소(human telomerase reverse transcriptase, hTERT) 유전자에 의해 암호화되는 촉매 소단위(catalytic subunit)와 인간 텔로머레이스 RNA(human telomerase RNA, hTR) 유전자 산물인 RNA 주형(template)을 중심으로 구성된 복합체이다. 여기에 dyskerin, NHP2, NOP10, GAR1 등 다양한 보조 단백질들이 결합하여, 효소 복합체의 구조적 안정성과 기능적 활성을 조절한다.텔로머레이스를 ‘자동차’ 전체에 비유한다면, TERT는 실제로 DNA를 합성하는 역할을 수행하는 ‘엔진’에 해당하며, hTR(또는 TERC)는 어떤 염기서열을 합성할지를 지시하는 ‘설계도’에 해당하는 RNA 주형으로 볼 수 있다.인체 내 약 120여 종의 세포 중 대부분은 텔로미어를 합성하는 효소인 텔로머레이스의 활성을 갖지 않으며, 이로 인해 세포는 분열이 반복될수록 텔로미어가 점진적으로 단축되고, 결국 복제에 따른 세포 노화(replicative senescence)에 도달하게 된다. 반면, 일부 높은 분열 능력을 가진 조직의 세포들은 예외적으로 텔로머레이스 활성을 유지한다.이러한 세포에는 모낭(hair follicle), 구강 편평상피(squamous epithelium), 피부 표피의 기저층(basal layer of epidermis), 제2형 폐포상피세포(type 2 alveolar epithelial cells), 간세포(hepatocytes), 장의 장선(intestinal crypts), 정원세포(spermatogonia) 등이 있다. 이들 세포에서 텔로머레이스 활성이 결여될 경우, 조직의 항상성 유지 및 생식 기능에 중대한 장애가 초래된다.특히, 정자 형성에 관여하는 정원세포(spermatogonia)에서 텔로머레이스 활성이 결여되면, 정자의 텔로미어 길이가 충분히 유지되지 못하고 단축된 상태로 전달된다. 이로 인해 형성된 배아는 텔로미어 단축에 기인한 세포 노화가 조기에 시작되며, 조기 노화(progeria)와 유사한 양상을 보일 수 있다. 실제로 이는 복제 양 돌리(Dolly) 사례에서 관찰된 바 있으며, 단축된 텔로미어가 수명 감소와 밀접하게 연관됨을 시사한다.이는 일반적인 체세포에서는 텔로머레이스 활성이 매우 낮은 수준으로 유지하지만, 생식세포와 줄기세포에서는 해당 효소가 구성효소(constitutive enzyme)로서 지속적으로 발현된다. 구성효소는 소화효소와 같이 항상 일정 수준으로 활성화되어 있는 효소이다.이에 반해 유도효소(inducible enzyme)는 특정 자극(예: 약물, 독성물질 등)에 의해 후천적으로 유도되는 효소이다. 이러한 분류 기준에 따라 텔로머레이스는 생식세포 및 줄기세포에서 구성효소로 기능하며, 암세포에서는 구성효소 및 유도효소적 특성을 보이는 이중적 성격을 가진다고 볼 수 있다.줄기세포 중에서도 배아줄기세포(embryonic stem cells) 및 유도만능줄기세포(induced pluripotent stem cells)는 고도로 안정된 텔로머레이스 활성을 보이며, 이로 인해 세포 분열에 따른 텔로미어의 단축이 거의 발생하지 않고, 복제에 따른 세포 노화에도 이르지 않는다.반면, 중간엽줄기세포(mesenchymal stem cells), 신경줄기세포(neural stem cells), 조혈모세포(hematopoietic stem cells) 등 성체 유래 줄기세포에서는 텔로머레이스 활성이 상대적으로 낮으며, 이로 인해 제한적인 텔로미어 단축이 관찰된다.TERT(Telomerase reverse transcriptase)란 무엇인가? 대부분의 체세포는 약 60~80회의 분열(population doublings) 이후 텔로미어가 임계 길이에 도달하게 되며, 이 시점에서 이중가닥 DNA 절단(double-strand break) 신호가 유도되어 복제에 따른 노화로 전환된다.이러한 현상은 체세포 내에서 텔로머레이스 활성이 거의 존재하지 않기 때문에 발생하는데, 이는 텔로머레이스의 RNA 구성 요소인 TERC(hTR)가 존재하더라도, 촉매 활성을 담당하는 TERT 유전자의 전사가 억제되어 있기 때문이다. 따라서, TERT 발현의 억제는 체세포에서 텔로머레이스 활성이 결핍되는 주요 원인이며, 텔로미어 단축의 분자적 기전으로 작용한다.뿐만 아니라, TERT는 단순한 텔로미어 연장 기능 외에도 텔로미어 말단의 캡핑(capping)과 전체 구조 유지에도 중요한 역할을 한다. 이는 다양한 암종의 약 80~90%에서는 TERT 발현이 재활성화되어 텔로머레이스 활성이 증가되어 있으며, 암세포의 불사화와 밀접하게 연관되어 있다.결과적으로, TERT 발현은 텔로미어 연장과 세포 노화 회피를 통해 암세포 특성이 획득되는 초기 단계에서 결정적인 분자 표지자로 작용한다. 이러한 TERT 발현 유도는 다양한 내& 8226;외부 요인 중 유전자 불안정성과 돌연변이가 가장 대표적인 기전으로 제시되고 있다.암의 발생 과정에서 텔로미어 길이의 보존이 빈번히 동반되며, 이는 주로 인간 텔로머레이스 역전사효소(hTERT)의 발현 증가에 따른 텔로머레이스 활성의 재개로 설명된다. 따라서 TERT의 발현 조절 기전은 텔로머레이스 기반 항암 치료법의 핵심 표적으로 주목받고 있으며, 암세포 특이적 바이오마커로서의 임상적 활용 가능성 또한 높다.텔로머레이스와 암과의 관계는 어떠한가? 텔로머레이스의 비정상적인 재활성화는 암세포에서 흔히 관찰되는데, 이는 텔로미어 단축으로 유도되는 세포자멸사를 회피하고 무한 증식 능력을 획득하는 데 핵심적인 기전으로 작용한다. 실제로, 전체 고형암 및 혈액암의 약 90% 이상에서 텔로머레이스 활성이 현저히 증가되어 있음이 관찰된다.여러 암 조직 생검에서 텔로머레이스 활성의 증가가 종양의 병기 및 악성도와 유의한 상관관계를 보이는 반면, 대부분의 정상 성인 조직에서는 텔로머레이스 활성이 거의 검출되지 않으며, 일부 조혈모세포나 면역세포에서만 일시적으로 나타나는 것으로 알려져 있다.이는 암세포 및 암전구세포에서 공통적으로 관찰되는 높은 수준의 텔로머레이스 발현과 텔로미어 유지 현상을 억제하여 암세포의 증식을 제한하는 치료 방법이 된다.특히, RNA 기반 치료법은 텔로머레이스의 RNA 구성요소인 hTR 또는 hTERT mRNA를 표적으로 하여 효소 활성을 간접적으로 억제하는 방식으로 주목받고 있다. 이 중 안티센스 올리고뉴클레오타이드(antisense oligonucleotides, ASO) 및 RNA 간섭(small interfering RNA, siRNA) 기술은 텔로머레이스 기능을 선택적으로 차단할 수 있는 새로운 접근법이다.대표적 예로는 이멜스타트(Imetelstat)가 있으며, 이는 인간 텔로머레이스 RNA(hTR)의 주형 영역에 상보적으로 결합하는 리간드 결합형 ASO로 설계되어, 텔로미어 연장 과정을 억제함으로써 암세포의 증식 억제를 유도한다. 이와 같은 RNA 기반 접근은 텔로머레이스 억제를 통한 항암 치료의 새로운 패러다임을 제시하며, 표적 치료제 개발에 있어 중요한 진전을 이끌고 있다.텔로머레이스 억제를 통한 항암 치료 전략은? 텔로머레이스를 표적으로 한 항암제 개발은 다양한 작용기전을 바탕으로 다방면에서 진행되고 있으며, 크게 RNA 기반 억제제, 전사 억제 화합물, G-사중나선 안정화제, 그리고 면역치료 백신 전략으로 구분할 수 있다.1. RNA 기반 억제제 가장 활발히 연구되고 있는 접근은 안티센스 올리고뉴클레오타이드(ASO) 또는 RNA 간섭(siRNA) 기술을 활용하여 텔로머레이스 RNA 구성요소(hTR 또는 TERC)를 표적으로 하는 전략이다. 이들 억제제는 텔로머레이스 복합체 내의 RNA 주형에 상보적으로 결합함으로써 효소 활성을 억제하거나, RNase H 의존적 분해를 유도하여 텔로머레이스 기능을 근본적으로 차단한다.대표적 약제인 이멜스타트(Imetelstat)는 티오포스포라마이드(thio-phosphoramidate) 변형을 적용한 ASO로, hTR의 템플릿 영역에 결합하여 텔로미어 연장을 저해한다.2. hTERT 전사 억제 저분자 화합물 이 저분자 화합물은 텔로머레이스의 촉매 소단위인 hTERT 유전자의 전사를 직접 억제하는 방식으로, 프로모터 영역 조절 또는 후성유전학적 메커니즘을 통해 유전자 발현 자체를 낮춘다. 일부 저분자 화합물은 hTERT 단백질에 직접 결합하여 효소 활성을 차단한다. 식물 유래 플라보노이드(예: genistein)가 TERT 전사를 억제하는 기능이 보고된 바 있으나 낮은 선택성과 잠재적인 세포독성으로 인해 임상 적용에는 제한이 있다.3. G-사중나선(G-quadruplex) 안정화제 이 안정화제는 텔로미어 말단에서 형성되는 G-사중나선 구조를 안정화시켜 텔로머레이스의 접근을 물리적으로 차단하는 방식이다. 해당 구조는 G-rich 반복 서열에서 자연적으로 형성되며, 일부 저분자 화합물은 이 구조에 특이적으로 결합하여 G-quadruplex 형태의 유지 및 안정화를 유도한다.이 방법은 효소가 아닌 기질을 표적으로 한다는 점에서 기존 억제제와 구별되며, 비교적 빠른 약효 발현이 가능하다. 그러나 G-rich 서열이 텔로미어 외에도 다양한 유전자의 조절부위에 존재하기 때문에, 표적 특이성 확보가 주요 과제로 남아 있다.4. 텔로머레이스를 항원으로 활용한 면역치료 텔로머레이스를 면역계의 표적으로 활용하는 전략도 개발되고 있다. 이는 hTERT 유래 펩타이드를 기반으로 하는 항암 백신을 통해, 텔로머레이스를 발현하는 종양세포를 면역세포가 인식하고 제거하도록 유도한다. 비소세포폐암(NSCLC), 췌장암 등 다양한 고형암에서 임상시험이 진행되고 있으며, 면역기억 반응을 통한 재발 억제 효과가 기대된다. 다만, 환자의 HLA 유형 및 종양미세환경(TME)에 따라 치료 반응의 편차가 존재하여, 정밀한 환자 선별 전략이 병행되어야 한다.이와 같이 텔로머레이스 억제 전략은 암세포 특이성이 높고 장기적인 종양 억제 효과를 유도할 수 있다는 점에서 유망한 접근이다. 그러나 기전상 텔로미어 길이의 점진적 단축을 필요로 하므로, 치료 효과 발현까지 수 주에서 수 개월이 소요되는 경향이 있다. 또한, 일부 암에서는 텔로머레이스 비의존적인 대체적 길이 조절(ALT, alternative lengthening of telomeres) 경로가 활성화되어 있어 단독요법으로는 제한적일 수 있다.이러한 한계를 극복하기 위해, 최근에는 DNA 손상 유도제, 면역관문억제제(PD-1/PD-L1 억제제), PARP 억제제 등과의 병용요법이 시도되고 있다. 또한 텔로머레이스 발현 수준, 텔로미어 길이 상태, ALT 경로 활성 여부 등을 고려한 환자 맞춤형 정밀의학적 접근이 병행됨으로써, 텔로머레이스 억제제의 임상적 유용성은 점차 확대되고 있다.뉴클레오타이드(Nucleotide)와 합성 올리고뉴클레오타이드의 차이는? 뉴클레오타이드는 모든 생명체에 보편적으로 존재하는 저분자 유기 화합물로, DNA와 RNA와 같은 핵산의 기본 단위이며 에너지 전달(ATP, GTP), 세포 신호전달(cAMP, cGMP), 효소 보조인자(NAD& 8314;, FAD) 등의 생리적 기능에 필수적인 역할을 수행한다. 이러한 분자는 세포 내에서 de novo 합성 경로 또는 재활용 경로(salvage pathway)를 통해 지속적으로 생성되며, 생명 유지에 핵심적인 역할을 한다.이에 반해, 올리고뉴클레오타이드는 일반적으로 몇 개에서 수십 개의 뉴클레오타이드가 공유결합으로 연결된 짧은 핵산 서열로, 인공적으로 합성된 생체분자이다. 자연적으로는 microRNA나 small nuclear RNA와 같은 일부 예외적인 경우를 제외하면 생체 내에서 잘 합성되지 않으며, 주로 화학적으로 합성되어 특정 유전 서열의 인식이나 분자 기능의 조절을 목적으로 활용된다.합성 올리고뉴클레오타이드는 분자생물학, 진단, 치료, 유전자 조작 등 다양한 분야에서 핵심 도구로 활용되고 있으며, 기능, 표적, 화학적 변형에 따라 , 다음과 같이 분류된다.첫째, 기능적 측면에서 ▲ mRNA 또는 pre-mRNA에 결합하여 유전자 발현을 억제하거나 RNA 스플라이싱을 조절하는 안티센스 올리고뉴클레오타이드(antisense oligonucleotide, ASO), ▲ RNA 간섭(RNAi)을 유도하여 표적 mRNA의 분해를 유도하는 소간섭 RNA(siRNA) 또는 마이크로 RNA(miRNA) 유사체, ▲ 고특이적으로 단백질에 결합하여 기능을 저해하거나 조절하는 압타머(aptamer), ▲ CRISPR 시스템에서 유전자 편집을 유도하는 가이드 RNA(guide RNA, gRNA), ▲ 전사인자와 결합하여 표적 유전자 조절을 간섭하는 디코이(decoy), ▲ PCR, qPCR, 유전자 탐지 등 핵산 분석 기술에 사용하는 프라이머(primer) / 프로브(probe) 등으로 분류된다.둘째, 표적 및 작용기전에 따라 ▲ DNA, ▲ mRNA, ▲ pre-mRNA, 또는 단백질 등 다양한 분자에 작용할 수 있으며, 그 기전은 전사 억제, 번역 차단, RNA 스플라이싱 조절, 단백질-핵산 상호작용 차단 등으로 확장된다.셋째, 화학 구조적 변형 측면에서 천연형(natural-type) 외에도 약물 안정성 및 효율성을 개선하기 위한 다양한 화학적 변형이 도입된다. 대표적으로 ▲ 인산기 산소를 황으로 치환하여 핵산분해효소 내성 증가를 위한 phosphorothioate(PS), ▲ 리보스의 2′ 위치에 화학기 추가로 결합력과 안정성 증가를 위한 2′-O-methyl RNA 및 2′-fluoro RNA, ▲ 리보스 고정을 통해 고결합 친화성 및 특이성 확보한 locked nucleic acid(LNA), ▲ 간세포 타깃팅 또는 세포 내 전달력 향상을 위한 GalNAc 또는 지질을 접합시킨 conjugated oligonucleotide 등이 있으며, 이는 체내 안정성, 표적 결합력, 약물 전달 효율성을 향상시키는 데 기여한다.요약하면, 뉴클레오타이드는 생명체 내에서 합성되는 주요 생리활성 분자인 반면, 올리고뉴클레오타이드는 외부에서 합성되어 생체 내 특정 유전자나 분자 기전을 정교하게 조절하기 위한 인공 핵산 서열이라는 점에서, 양자는 생성 방식과 생리적 존재 양상에서 본질적으로 다르다. 그럼에도 불구하고, 올리고뉴클레오타이드는 자연계 핵산의 기능을 모방하거나 확장함으로써 차세대 핵산 기반 치료제 및 진단 기술의 핵심 플랫폼으로 부상하고 있다.ASO(Antisense Oligonucleotide, 안티센스 올리고뉴클레오타이드)란? ASO는 mRNA를 표적으로 설계된 짧은 합성 단일가닥 DNA 분자로, 특정 mRNA 서열과 상보적으로 결합함으로써 유전자 발현을 억제하거나 조절하는 기능을 수행한다(Figure. 3).ASO는 비교적 간단한 화학 구조를 기반으로 하면서도, 전사체의 분해 유도, RNA 스플라이싱 (splicing) 조절, 번역 억제 등 다양한 작용기전을 통해 유전 정보의 흐름을 정교하게 제어할 수 있는 장점을 가진다.ASO의 작용기전은 화학적 변형 방식과 결합 표적에 따라 다양하게 구분된다. 대표적으로 RNase H 매개 분해는 ASO가 표적 mRNA와 이중가닥을 형성한 후, 세포 내 RNase H 효소에 의해 해당 mRNA가 분해되어 단백질 생성을 원천적으로 차단하는 기전이다.또한, 스플라이싱 조절용 ASO는 pre-mRNA의 엑손/인트론 경계부에 결합하여, 엑손 스키핑(skipping) 또는 보존을 유도함으로써 단백질의 구조와 기능을 변형시킬 수 있다. 이 외에도 번역 개시 억제, mRNA 안정성 저해 등 다양한 방식으로 작용이 가능하다.이러한 특성을 바탕으로, ASO는 기존 소분자 화합물이나 단백질 기반 치료제와 달리 기능 상실(loss-of-function) 혹은 기능 획득(gain-of-function) 유전자 돌연변이 모두를 정교하게 조절할 수 있다.그러나 ASO 치료제는 면역반응 유발, 비표적 결합(off-target effect), 체내 약물 전달 효율 등의 한계를 지니고 있으며, 이를 극복하기 위해 phosphorothioate 치환, 2′-O-methyl 및 LNA 변형, GalNAc 결합을 통한 간세포 표적화, 지질 나노입자 기반 전달체 등 다양한 기술적 발전이 이루어지고 있다.이러한 발전은 ASO의 치료적 효능을 향상시키는 데 핵심적인 기여를 하고 있으며, ASO 기반 핵산 치료제가 차세대 정밀의학 기반의 분자표적 치료제로 자리매김할 수 있는 가능성을 높이고 있다.텔로머레이스 표적 올리고뉴클레오타이드(Telomerase-targeted oligonucleotide, TTO)란? TTO는 표적 핵산 서열에 상보적으로 결합하는 구조를 가지면서도, 기존의 ASO와는 본질적으로 다른 작용기전을 가진다. 즉 일반적인 ASO는 mRNA의 분해(RNase H 의존적 경로) 또는 스플라이싱 조절을 통해 단백질 생성을 억제하지만, TTO는 hTR의 템플릿 서열에 직접 결합함으로써 텔로머레이스 효소 복합체의 활성 부위를 차단한다. 이는 효소의 기질 인식 및 촉매 반응 자체를 방해하는 비정형(non-canonical) ASO로 분류된다.이러한 TTO는 효소 작용 자체의 차단을 통해 효소 기능 차단(enzyme activity inhibition)이라는 새로운 패러다임을 제공한다. 특히 텔로머레이스 활성이 높은 암세포에서 선택적으로 작용함으로써, 정상세포에 대한 영향을 최소화하면서 암 특이적 억제 효과를 유도할 수 있다.대표적인 TTO로는 이메텔스타트(Imetelstat)가 있으며, 이는 hTR의 템플릿 영역에 상보적으로 결합하는 티오인산화(thio-phosphoramidate) 올리고뉴클레오타이드로 설계되었다.이메텔스타트는 어떤 약제인가? 이메텔스타트(Imetelstat, 제품명: 라이텔로 정맥주사, Rytelo®)는 텔로머레이스를 직접 표적으로 하는 최초의 올리고뉴클레오타이드 기반 치료제로, 2024년 미국 FDA로부터 승인받은 이후 골수이형성증후군(MDS) 치료 영역에서 새로운 치료 축으로 부상하고 있다. 이 약제의 승인 적응증은 "8주간 4단위 이상의 적혈구 수혈이 필요한 수혈 의존성 빈혈을 가진 저위험~중간-1 위험군 MDS 성인 환자 중, 적혈구생성자극제(ESA)에 반응하지 않거나 반응이 소실되었거나, 투여가 불가능한 경우"이다.이메텔스타트는 기존의 ASO와는 구별되는 비정형 ASO로 분류되며, 비정상적인 텔로머레이스 활성을 보이는 악성 조혈모세포(HSCs) 및 전구세포(HPCs)를 선택적으로 억제함으로써 병적 클론의 제거와 정상 조혈 기능의 회복을 유도하는 질환 수정형(disease-modifying) 치료 제이다.분자 구조적으로, 이메텔스타트는 13개의 뉴클레오타이드로 구성된 단일가닥 DNA 서열이며, 티오인산화(thio-phosphoramidate) 변형을 통해 핵산분해효소(nuclease) 저항성, 수용성, 대사적 안정성 등의 약물학적 특성이 향상되었다. 또한 5′ 말단에 팔미토일기(palmitoyl group)가 결합되어 소수성을 증가시켜 세포막 투과성 및 세포 내 유지성을 강화하며, 별도의 형질전환 과정 없이도 세포 내 작용이 가능하도록 설계되었다.전임상 연구에서는 이메텔스타트의 약물 노출과 텔로머레이스 억제 간의 명확한 약력학적 상관성이 확인되었고, 텔로머레이스 활성을 50% 이상 억제하는 수준의 약리 효과가 임상적으로 확보 가능한 범위 내에 있음이 입증되었다. 또한, 골수증식성 질환 모델(예: 본태성 혈소판증, 골수섬유증, 급성 골수성 백혈병 등)에서는 시험관 내(in vitro) 및 생체 내(in vivo) 실험 모두에서 강력한 항종양 활성을 나타냈다.특히 저위험 MDS 환자에서 이메텔스타트는 텔로미어 단축, hTERT 과발현, 분화 억제 등으로 특징지어지는 병적 조혈모세포 및 전구세포를 선택적으로 제거함으로써, 정상 조혈의 회복과 함께 적혈구 수혈 비의존 기간(RBC-TI)의 연장, 혈색소 수치의 향상, 염색체 이상 클론 및 돌연변이 부담의 감소를 유도하였다.아울러, 이메텔스타트는 면역회피 특성을 가진 악성 클론에서도 항암 활성을 유지함으로써, 기존 면역항암제 또는 세포독성 항암제에 비해 임상적 적용 가능성이 높다. 현재 진행 중인 다수의 임상시험 결과에 따라, MDS뿐 아니라 골수섬유증(myelofibrosis), 기타 혈액암 영역으로의 적응증 확장 가능성도 제시되고 있다.이메텔스타트의 약리 기전은? 이메텔스타트는 TERT-targeting telomerase complex inhibtor 또는 RNA-template targeting telomerase inhibitor로, 인간 텔로머라제의 RNA 구성 요소(hTR)의 주형 영역에 상보적으로 결합하여 텔로머레이스 복합체의 활성 부위에서 기질 결합 및 연장을 직접 차단한다. 즉 hTR의 주형 서열(3′-CAAUCCCAAUC-5′)에 상보적인 염기서열(5′-palmitate-TAGGGTTAGACAA-NH₂-3′)이 결합함으로써, 텔로머레이스 효소의 활성을 억제하여 텔로미어 말단에 반복 서열을 추가하는 기능을 경쟁적으로 차단한다. 이로 인해 암세포 내에서의 텔로미어 길이가 점진적으로 짧아지며, 결국 세포 노화 또는 세포자멸사를 유도하게 된다(Figure 4). 골수이형성증후군(MDS) 및 악성 줄기세포 및 전구세포에서 텔로머레이스 활성 및 인간 텔로머레이스 역전사효소(hTERT) RNA 발현이 증가한 것으로 보고되었다. 이에 여러 연구에서 이메텔스타트 치료가 텔로미어 길이 감소, 악성 줄기세포 및 전구세포의 증식 감소, 그리고 세포자멸사를 유도함으로써 세포 증식 억제 및 수명 단축 효과를 나타낸 것으로 보고되었다.또한, 이 약제는 텔로머레이스의 촉매 소단위인 hTERT의 발현을 억제함으로써 효소 활성을 이중적으로 저해하는데, 이 hTERT는 텔로머레이스 활성을 조절하는 주요 속도 제한 인자(rate-limiting component)로 알려져 있다.이러한 이멜스타트의 작용 기전은 항원-항체 반응이나 면역세포 활성화를 기반으로 하는 기존 면역항암제와는 달리, 종양 세포의 분열 및 생존을 유지하는 내재적 기전인 텔로머레이스 의존성을 직접 차단한다는 점에서 근본적인 차별성을 갖는다.이멜스타트(RYTELO& 9415;) 3상 임상은 어떻게 진행되었나? 이메텔스타트의 임상적 유효성은 IMerge 3상 연구를 통해 입증되었다. 본 연구는 무작위배정, 이중눈가림, 위약대조, 다기관 임상시험으로 설계되었으며, 저위험 또는 중간-1위험군 골수이형성증후군(MDS) 환자 중 수혈 의존성을 보이는 성인 178명을 대상으로 시행되었다. 환자 등록 기준은 무작위배정 16주 전의 8주간 기간 동안 적어도 4단위 이상의 적혈구 수혈 필요 이력이 있는 경우로 정의되었다.등록 환자들은 모두 적혈구생성자극제(ESA)에 반응이 없었거나 반응이 소실되었거나, ESA 투여가 적절하지 않다고 판단된 경우였다. 주요 포함 기준에는 절대 호중구 수치 ≥ 1.5 × 10& 8313;/L, 혈소판 수 ≥ 75 × 10& 8313;/L이 포함되었으며, del(5q) 염색체 이상 보유자, 레날리도마이드(Lenalidomide) 또는 아자시티딘(Azacitidine)과 데시타빈(Decitabine) 같은 저메틸화제(hypomethylating agents, HMA) 치료 이력이 있는 환자는 제외되었다.무작위배정은 2:1 비율로 수행되어, RYTELO 7.1 mg/kg 정맥주사군(n=118) 또는 위약군(n=60)에 배정되었으며, 28일 주기(cycle)로 반복 투여되었다. 치료는 질병 진행, 용인할 수 없는 독성, 또는 환자의 자의적 중단 시점까지 지속되었다. 무작위배정은 기존 RBC 수혈 부담 및 IPSS 위험군 등급을 기준으로 계층화되었다. 모든 환자에게는 필요 시 적혈구 수혈을 포함한 지지요법(supportive care)이 병행 제공되었다.평가 기간은 RYTELO 투여군에서 중앙 추적기간 19.5개월(범위: 1.4& 8211;36.2개월), 위약군에서 17.5개월(범위: 0.7& 8211;34.3개월)이었으며, 주요 유효성 평가 변수는 적혈구 수혈 독립(RBC transfusion independence, RBC-TI) 달성 비율이었다. 이는 무작위배정 이후부터 차기 항암 치료 개시 전까지의 기간 중 연속된 8주(≥56일) 또는 연속된 24주(≥168일) 동안 적혈구 수혈이 전혀 이루어지지 않은 경우로 정의되었다.그 결과, 8주 이상 RBC-TI 도달률은 RYTELO 군에서 39.8%(95% CI: 30.9& 8211;49.3)로, 위약군의 15.0%(95% CI: 7.1& 8211;26.6) 대비 통계적으로 유의하게 높았다(p < 0.001). 또한 24주 이상 RBC-TI 도달률 역시 RYTELO 군에서 28.0% (95% CI: 20.1& 8211;37.0)로, 위약군 3.3% (95% CI: 0.4& 8211;11.5)와 비교하여 유의한 차이를 보였다(p < 0.001). 이러한 결과는 RYTELO가 ESA 불응 또는 부적합 환자군에서 수혈 의존성을 유의하게 줄이고, 적혈구계 조혈 회복을 유도할 수 있는 잠재력을 입증하는 것으로 해석된다.안전성 측면은 RYTELO 군에서 위약군 대비 ≥10% 이상, ≥5% 차이를 보인 주요 이상반응은 혈소판 감소, 백혈구 감소, 호중구 감소, AST/ALT/ALP 상승, 피로, 부분 트롬보플라스틴 시간 연장, 관절/근육통, COVID-19 감염, 두통 등이었다.따라서, RYTELO는 저위험 MDS 환자에서 임상적으로 의미 있는 수혈 독립 향상을 유도하였으며, 전반적으로 관리 가능한 안전성 프로파일을 보였다. 권장 투여 용량은 7.1 mg/kg이며, 4주마다 2시간에 걸쳐 정맥 투여한다. 이멜스타트의 앞으로의 예상은? 골수이형성증후군(MDS)은 조혈모세포의 분화 및 성숙에 결함이 생겨 비정상적 조혈과 말초 혈구감소증을 유발하는 이질적인 클론성 조혈장애이다. 특히 저위험군 MDS 환자에서는 만성적인 적혈구 수혈 의존성 빈혈이 주요 임상 양상으로 나타나며, 삶의 질 저하 및 철분 과부하에 의한 이차적 장기 손상이 주요 합병증으로 작용한다.현재까지 이들 환자에서 사용 가능한 치료제로는 적혈구생성자극제(ESA) 및 저메틸화제(HMA) 등이 있으나, 반응률의 한계와 장기 치료 효과에 대한 의문이 지속적으로 제기되고 있다.텔로머레이스는 텔로미어 길이를 유지하여 세포의 분열 한계를 극복하게 하는 핵심 효소로, 대부분의 암세포 및 악성 조혈모세포에서 비정상적으로 활성이 증가되어 있는 것이 특징이다. 이러한 활성을 선택적으로 억제함으로써 병적 조혈세포의 증식을 제한하고 정상 조혈을 회복시키는 접근은 질환의 근본 기전을 타겟으로 하는 질환 수정형(disease-modifying) 치료전략으로 주목받고 있다.이메텔스타트(Imetelstat)는 인간 텔로머레이스 복합체(hTERT/hTR)에 직접 결합하여 활성을 경쟁적으로 억제하는 first-in-class 올리고뉴클레오타이드 기반 치료제로, 텔로미어 유지 능력을 상실하게 하여 세포 자멸사 및 증식 억제를 유도한다. 특히 병적 조혈모세포(HSCs/HPCs)와 백혈병 줄기세포(LSCs)에 선택적으로 작용하며, 정상 조혈세포에 대한 영향은 제한적으로 보고되고 있다.IMerge 3상 임상시험에서 이메텔스타트는 ESA에 반응하지 않거나 부적합한 저위험~중간-1 위험군 MDS 환자를 대상으로 통계적으로 유의한 적혈구 수혈 독립 효과를 입증하였다. 8주 이상 수혈 독립률(RBC-TI)은 이메텔스타트군에서 39.8%, 위약군에서 15.0%로 나타났으며, 24주 이상 수혈 독립률도 각각 17.8%와 1.6%로 유의한 차이를 보였다. 이는 기존 치료옵션에 반응하지 않는 환자 집단에 있어 새로운 치료 패러다임을 제시한 근거로 평가된다.다만, 현재 이메텔스타트는 저위험 MDS + ESA 실패 + 수혈 의존성 빈혈이라는 제한된 적응증으로 승인되어 있으며, TP53 돌연변이나 고위험군 MDS는 제외 대상에 해당된다. 또한 치료 효과 발현까지 수 주에서 수개월이 소요되며, 호중구감소증(72%) 및 혈소판감소증(65%) 등 고빈도의 혈액학적 이상반응이 동반될 수 있다는 점은 임상적 고려가 필요하다.그럼에도 불구하고, 텔로머레이스라는 근원적 분자 표적을 겨냥한 이메텔스타트는 기존 화학요법 및 면역조절제와는 차별화된 기전을 통해 조혈계 악성질환에 있어 정밀의학적 치료 전략으로서의 가능성을 보여주고 있다. 이미 미국 및 유럽에서 승인된 약제로서, 향후 국내 도입과 더불어 적응증 확대, 병용요법, 고위험 환자군에서의 임상적 검토가 필요할 것으로 예상한다.참고문헌 1. Alexander Vaiserman, Dmytro Krasnienkov “Telomere Length as a Marker of Biological Age: State-of-the-Art, Open Issues, and Future Perspectives” Front. Genet. 11:630186(2021). 2. Virginia Boccardi “Aging, Cancer, and Inflammation: The Telomerase Connection” J. Mol. Sci. 2024, 25(15), 8542. 3. Virginia Boccardi, and Luigi Marano “Aging, Cancer, and Inflammation: The Telomerase Connection” Int. J. Mol. Sci. 2024, 25, 8542. 4. Zachary Schrank, Nabiha Khan, Chike Osude, Sanjana Singh et al. “Oligonucleotides Targeting Telomeres and Telomerase in Cancer” Molecules 2018, 23, 2267. 5. Ashley L. Lennoxm, Fei Huang, Melissa Kelly Behrs, Mario Gonz& 225;lez-Sales et al. “Imetelstat, a novel, first-in-class telomerase inhibitor:Mechanism of action” Clin Transl Sci. 2024;17:e70076 6. 기타 인터넷 자료(보도 자료, 제품 설명서 등)2025-06-13 06:24:02최병철 박사 -
 흑색종 환자에 '암타그비' 투여…중위험 연구 정부 승인[데일리팜=이정환 기자] 정부가 T세포 치료제 암타그비를 활용해 불응성 흑색종 환자를 치료하는 중위험 임상연구를 승인했다.동종 조혈모세포 이식 소아청소년 가운데 표준치료에 저항성·불응성을 보이는 다중 바이러스 감염증 환자에게 다중 바이러스 항원 특이적 면역세포인 T세포를 투여하는 고위험 임상연구도 허용했다.23일 보건복지부는 제5차 첨단재생의료 및 첨단바이오의약품 심의위원회 의결 결과를 통해 이같이 밝혔다.심의위는 가톨릭서울성모병원, 삼성서울병원 등 임상연구계획 총 4건(고위험 2건, 중위험 2건)을 심의했다. 이 중 2건은 적합, 2건은 부적합 의결했다.흑색종 환자 '암타그비' 투약 임상연구 승인적합 의결된 과제는 면역관문억제제 치료에 실패한 불응성(난치성) 흑색종 환자를 대상으로 환자 본인으로부터 유래한 종양침윤림프구(CT-SP)의 안전성·유효성 평가를 위한 중위험 임상연구이다.흑색종은 피부에 있는 멜라닌 세포에서 발생하는 악성종양이다. 피부암의 1~4%이지만 사망률은 가장 높다.종양침윤림프구는 종양 미세환경에 존재하는 림프구로 종양세포를 인지하고 파괴한다. 종양이질성과 종양세포의 면역기피를 극복하고 종양세포를 사멸시킬 가능성이 높다.종양침윤림프구 치료제는 고형암을 대상으로 세계 최초 허가된 T 세포치료제 '암타그비'다.국내외에서 다양한 고형암을 대상으로 종양침윤림프구 치료제의 임상시험이 진행 중이다.해당 연구는 국내에서 개발한 제조 방법으로 만든 종양침윤림프구를 투여하고 이상반응 확인 등 안전성 평가와 객관적 반응률·무진행 생존기간 등을 확인하는 유효성 평가를 목표로 한다.대부분의 기존 치료에 실패한 국내 흑색종 환자에게 종양침윤림프구를 이용한 새로운 치료 방법을 제공하기 위해서다.다중바이러스 감염 환자 T세포 투여도 허용동종 조혈모세포를 이식한 소아청소년 중 표준치료에 저항성·불응성을 보이는 다중 바이러스 감염 또는 관련 감염증 환자를 대상으로 다중 바이러스 항원 특이적 면역세포인 T 세포(VST)를 투여하는 고위험 임상연구다.동종조혈모세포이식 과정에서 주로 발생하는 이식편대숙주병은 기증자의 면역세포가 환자의 조직을 공격하는 주요 중증 합병증이다.이를 관리하기 위해 강력한 면역억제제가 사용되며 그 부작용으로 환자 전반적인 면역력이 약화되어 감염에 취약해진다.이로 인해 환자 체내 잠복감염 바이러스들이 재활성화되어 감염을 일으키는데, 기존 치료제인 항바이러스제는 여러 바이러스를 동시에 억제하기 어렵고 장기 사용 시 내성이 생길 수 있으며 신장·간독성이 높다.해당 연구는 다중 바이러스 항원에 특이적인 T 세포를 이용하여 동시에 다중 바이러스를 억제하고 면역 기억을 통해 장기적으로 재발도 방지하는 것을 목표로 한다.식품의약품안전처장은 고위험 임상연구 신속·병합 검토를 통해 연구자의 제출 자료가 타당함을 심의위원회에 통보했다.절차에 따라 재생의료기관은 식약처장 승인 통보를 받은 후 임상연구를 실시하게 된다.김우기 첨단재생의료 및 첨단바이오의약품 심의위원회 사무국장은 "심의위원회는 임상연구 활성화를 위해 보완이 필요한 임상연구계획에 대해 재심의 결정을 통해 연구자가 보완할 수 있도록 기회를 부여하여 최종 적합 의결했다"고 설명했다.2025-05-23 11:31:53이정환
흑색종 환자에 '암타그비' 투여…중위험 연구 정부 승인[데일리팜=이정환 기자] 정부가 T세포 치료제 암타그비를 활용해 불응성 흑색종 환자를 치료하는 중위험 임상연구를 승인했다.동종 조혈모세포 이식 소아청소년 가운데 표준치료에 저항성·불응성을 보이는 다중 바이러스 감염증 환자에게 다중 바이러스 항원 특이적 면역세포인 T세포를 투여하는 고위험 임상연구도 허용했다.23일 보건복지부는 제5차 첨단재생의료 및 첨단바이오의약품 심의위원회 의결 결과를 통해 이같이 밝혔다.심의위는 가톨릭서울성모병원, 삼성서울병원 등 임상연구계획 총 4건(고위험 2건, 중위험 2건)을 심의했다. 이 중 2건은 적합, 2건은 부적합 의결했다.흑색종 환자 '암타그비' 투약 임상연구 승인적합 의결된 과제는 면역관문억제제 치료에 실패한 불응성(난치성) 흑색종 환자를 대상으로 환자 본인으로부터 유래한 종양침윤림프구(CT-SP)의 안전성·유효성 평가를 위한 중위험 임상연구이다.흑색종은 피부에 있는 멜라닌 세포에서 발생하는 악성종양이다. 피부암의 1~4%이지만 사망률은 가장 높다.종양침윤림프구는 종양 미세환경에 존재하는 림프구로 종양세포를 인지하고 파괴한다. 종양이질성과 종양세포의 면역기피를 극복하고 종양세포를 사멸시킬 가능성이 높다.종양침윤림프구 치료제는 고형암을 대상으로 세계 최초 허가된 T 세포치료제 '암타그비'다.국내외에서 다양한 고형암을 대상으로 종양침윤림프구 치료제의 임상시험이 진행 중이다.해당 연구는 국내에서 개발한 제조 방법으로 만든 종양침윤림프구를 투여하고 이상반응 확인 등 안전성 평가와 객관적 반응률·무진행 생존기간 등을 확인하는 유효성 평가를 목표로 한다.대부분의 기존 치료에 실패한 국내 흑색종 환자에게 종양침윤림프구를 이용한 새로운 치료 방법을 제공하기 위해서다.다중바이러스 감염 환자 T세포 투여도 허용동종 조혈모세포를 이식한 소아청소년 중 표준치료에 저항성·불응성을 보이는 다중 바이러스 감염 또는 관련 감염증 환자를 대상으로 다중 바이러스 항원 특이적 면역세포인 T 세포(VST)를 투여하는 고위험 임상연구다.동종조혈모세포이식 과정에서 주로 발생하는 이식편대숙주병은 기증자의 면역세포가 환자의 조직을 공격하는 주요 중증 합병증이다.이를 관리하기 위해 강력한 면역억제제가 사용되며 그 부작용으로 환자 전반적인 면역력이 약화되어 감염에 취약해진다.이로 인해 환자 체내 잠복감염 바이러스들이 재활성화되어 감염을 일으키는데, 기존 치료제인 항바이러스제는 여러 바이러스를 동시에 억제하기 어렵고 장기 사용 시 내성이 생길 수 있으며 신장·간독성이 높다.해당 연구는 다중 바이러스 항원에 특이적인 T 세포를 이용하여 동시에 다중 바이러스를 억제하고 면역 기억을 통해 장기적으로 재발도 방지하는 것을 목표로 한다.식품의약품안전처장은 고위험 임상연구 신속·병합 검토를 통해 연구자의 제출 자료가 타당함을 심의위원회에 통보했다.절차에 따라 재생의료기관은 식약처장 승인 통보를 받은 후 임상연구를 실시하게 된다.김우기 첨단재생의료 및 첨단바이오의약품 심의위원회 사무국장은 "심의위원회는 임상연구 활성화를 위해 보완이 필요한 임상연구계획에 대해 재심의 결정을 통해 연구자가 보완할 수 있도록 기회를 부여하여 최종 적합 의결했다"고 설명했다.2025-05-23 11:31:53이정환 -
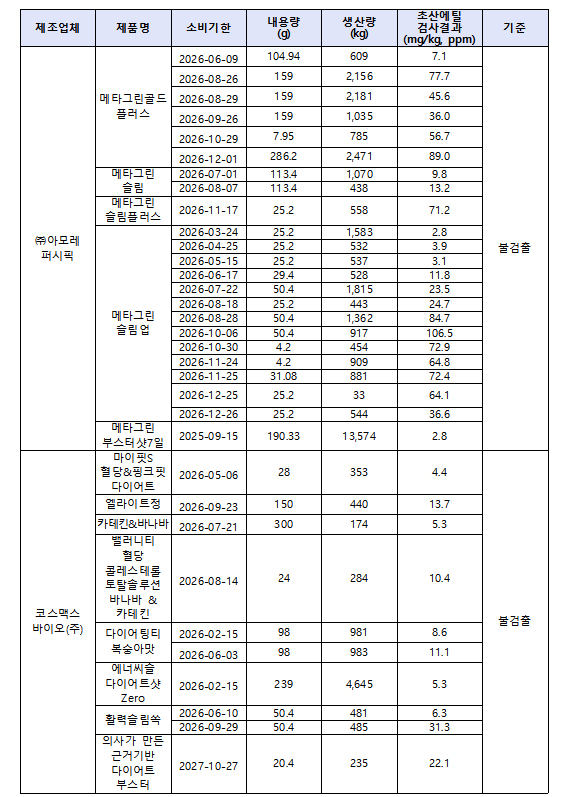 식약처, 초산에틸 규격 부적합 건강기능식품 13개 회수[데일리팜=이혜경 기자] 식품의약품안전처(처장 오유경)는 건강기능식품제조업체인 아모레퍼시픽(경기 안성시 소재)과 코스맥스바이오(충북 제천시 소재)에서 제조한 아래 13개 건강기능식품을 초산에틸 규격 위반으로 판매 중단 및 회수 조치한다고 21일 밝혔다.이들 제품은 초산에틸을 사용하지 않은 것으로 수입 신고된 녹차추출물을 원재료로 사용해 제조했다고 신고했지만, 해당 건강기능식품에서 초산에틸이 검출됐다.식약처는 "해당 제품을 구매한 소비자에게 섭취를 중단하고 구입처에 반품해 줄 것"을 당부했다. 회수 대상 제품 정보 초산에틸은 과일향이 있어 식품에 향을 더하거나 식품 원재료에서 특정 성분을 뽑아내는 용도로 사용되는 식품첨가물로 녹차추출물과 같은 건강기능식품 기능성 원료나 다류, 커피, 식용유지 등을 제조할 때 많이 사용된다.녹차추출물의 경우 원재료인 녹차 잎에서 기능성 성분인 카테킨을 추출하는데 쓰인다.코엔자임Q10, 밀크씨슬 추출물, 마리골드 추출물, 토마토 추출물 등 다양한 건강기능식품의 기능성 성분의 추출 용매로 이용된다.녹차추출물 제조 시 물 또는 주정, 초산에틸을 추출 용매로 사용할 수 있고, 초산에틸을 사용한 경우 50.0 mg/kg(ppm) 이하로 규격을 정하고 있다.이번 녹차추출물 경우 제조 시 물 또는 주정을 추출용매로 사용했으며, 초산에틸을 사용하지 않은 경우 초산에틸은 검출되면 안된다.이번 검사 결과 부적합 13개 제품에서 검출된 초산에틸의 양을 제품별1일 섭취량을 감안해 환산한 후 국제식량농업기구(FAO)/세계보건기구(WHO) FAO/WHO 합동식품첨가물전문가위원회(JECFA)에서 정하고 있는 초산에틸의 일일섭취허용량(ADI)과 비교한 결과, 일일섭취허용량(25 mg/kg·bw/day)의 약 0.0002~0.0104%로 인체에 위해를 일으킬 수준은 아닌 것으로 판단됐다.2025-05-21 12:28:59이혜경
식약처, 초산에틸 규격 부적합 건강기능식품 13개 회수[데일리팜=이혜경 기자] 식품의약품안전처(처장 오유경)는 건강기능식품제조업체인 아모레퍼시픽(경기 안성시 소재)과 코스맥스바이오(충북 제천시 소재)에서 제조한 아래 13개 건강기능식품을 초산에틸 규격 위반으로 판매 중단 및 회수 조치한다고 21일 밝혔다.이들 제품은 초산에틸을 사용하지 않은 것으로 수입 신고된 녹차추출물을 원재료로 사용해 제조했다고 신고했지만, 해당 건강기능식품에서 초산에틸이 검출됐다.식약처는 "해당 제품을 구매한 소비자에게 섭취를 중단하고 구입처에 반품해 줄 것"을 당부했다. 회수 대상 제품 정보 초산에틸은 과일향이 있어 식품에 향을 더하거나 식품 원재료에서 특정 성분을 뽑아내는 용도로 사용되는 식품첨가물로 녹차추출물과 같은 건강기능식품 기능성 원료나 다류, 커피, 식용유지 등을 제조할 때 많이 사용된다.녹차추출물의 경우 원재료인 녹차 잎에서 기능성 성분인 카테킨을 추출하는데 쓰인다.코엔자임Q10, 밀크씨슬 추출물, 마리골드 추출물, 토마토 추출물 등 다양한 건강기능식품의 기능성 성분의 추출 용매로 이용된다.녹차추출물 제조 시 물 또는 주정, 초산에틸을 추출 용매로 사용할 수 있고, 초산에틸을 사용한 경우 50.0 mg/kg(ppm) 이하로 규격을 정하고 있다.이번 녹차추출물 경우 제조 시 물 또는 주정을 추출용매로 사용했으며, 초산에틸을 사용하지 않은 경우 초산에틸은 검출되면 안된다.이번 검사 결과 부적합 13개 제품에서 검출된 초산에틸의 양을 제품별1일 섭취량을 감안해 환산한 후 국제식량농업기구(FAO)/세계보건기구(WHO) FAO/WHO 합동식품첨가물전문가위원회(JECFA)에서 정하고 있는 초산에틸의 일일섭취허용량(ADI)과 비교한 결과, 일일섭취허용량(25 mg/kg·bw/day)의 약 0.0002~0.0104%로 인체에 위해를 일으킬 수준은 아닌 것으로 판단됐다.2025-05-21 12:28:59이혜경 -
 가르시니아·녹차 건기식 12품목, 기능성분 함량 충족[데일리팜=이정환 기자] 가르시니아캄보지아, 녹차 등에서 추출한 원료로 만든 다이어트 건강기능식품 12개 제품의 체지방 감소 기능성분 함량이 1일 섭취량 기준을 모두 충족하는 것으로 확인됐다.다만 가르시니아의 경우 두 개 이상의 체지방 감소 기능성 물질을 중복 섭취하면 간독성 등 부작용이 생길 수 있어 소비자 주의가 요구된다.중금속과 미생물 등 안전성 역시 12개 제품 전부 기준에 적합했지만, 1개 제품은 추출용매인 초산에틸 잔류수준이 기준 부적합으로 나타났다.21일 한국소비자원은 체중 감소 건기식 품질·안전성 비교 결과를 공개했다.소비자원이 비교한 제품은 가르시니아 플러스, 그린몬스터 다이어트 스페셜2 가르시니아 900, 레드컷 가르시니아 비포, 스키니랩 가르시니아, 종근당 프리미엄 가르시니아 다이어트, 칼로-스탑 PLUS+, 녹차카테킨 다이어트 플러스, 메타그린 슬림업 30일, 사이클 다이어트 그린, GRN 올 뉴 초록이 시즌4, 카테킨400, 칼로커트 등 총 12개 품목이다.제품에 표시된 1일 섭취량 기준으로 가르시니아캄보지아 추출물 6개 제품은 기능성분(총(-)-HCA) 함량이 652㎎ ~ 999㎎, 녹차추출물 6개 제품은 기능성분(카테킨) 함량이 289㎎ ~ 467㎎으로 모두 관련 기준을 충족했다. 시험대상 12개 중 8개 제품은 비타민·무기질 및 기타 기능성분을 함유하고 있었으며, 모두 성분별 함량이 건강기능식품 기준을 충족했다. 가장 많은 제품에 들어간 영양성분은 판토텐산으로 총 6개 제품에 있었고 나이아신, 비타민C, 비타민B(B1,B2,B6)는 각각 4개 제품에 함유됐다. '카테킨 400(㈜더베이글)' 제품은 비타민·무기질이 12종으로 조사대상 제품 중 가장 많은 종류의 성분을 함유했으며, 각 영양성분은 1일 영양성분 기준치 대비 100% ~ 147% 수준이었다. 초산에틸은 식품첨가물로 추출용제나 향료로써 사용할 수 있는 기준과 용도가 정해져 있고 녹차추출물 제조 시 사용될 수 있다.이에 초산에틸 잔류량을 확인한 결과, 1개 제품이 잔류 기준에 부적합했다. 아모레퍼시픽 '메타그린 슬림업 30일'이 기준 부적합 품목이다. 해당 사업자는 소비자원 시정권고를 수용해 해당 원료를 사용한 전 제품을 회수하고 판매된 제품에 대해서는 환불 조치하기로 했다.식품의약품안전처는 해당 제품에 대한 수거검사를 진행했고, 검사 결과에 따라 건강기능식품법에 따른 회수 등의 행정조치를 진행 중이다.그 외 제조·가공 중 오염될 수 있는 중금속(납, 카드뮴, 비소, 수은)과 대장균군은 전 제품이 관련 기준에 적합했다.건기식은 관련 기준에 따라 기능성 원료에 적합한 주의사항을 표시해야 한다. 확인 결과 12개 제품 모두 관련 기준에 적합했다.다만, 가르시니아캄보지아 추출물은 체지방 감소 기능성을 표방하는 다른 건강기능식품과 함께 섭취 시 간 독성 등 이상 사례 발생 가능성이 보고된 바 있어 섭취에 주의가 필요하다.이에 '체지방 감소 기능성 제품의 중복섭취 주의 표시'를 조사한 결과 2개 제품에만 해당 표시가 있고, 나머지 10개 제품(9개 업체)은 별도 주의사항이 없어 추가 표시하도록 자율 개선을 권고했다.가르시니아캄보지아 추출물 6개 제품은 1일 섭취량(제품표시기준) 당 170원~921원으로 제품 간 5배, 녹차추출물 6개는 156원~5267원으로 제품 간 최대 34배 차이가 났다.가르시니아캄보지아 원료 제품은 `가르시니아 플러스(㈜대웅생명과학)'가 1일 섭취량(제품표시 기준) 당 가격이 170원으로 가장 저렴했고, 녹차추출물 원료 제품은 `녹차카테킨 다이어트 플러스(㈜대웅생명과학)'가 156원으로 가장 쌌다.2025-05-21 11:46:33이정환
가르시니아·녹차 건기식 12품목, 기능성분 함량 충족[데일리팜=이정환 기자] 가르시니아캄보지아, 녹차 등에서 추출한 원료로 만든 다이어트 건강기능식품 12개 제품의 체지방 감소 기능성분 함량이 1일 섭취량 기준을 모두 충족하는 것으로 확인됐다.다만 가르시니아의 경우 두 개 이상의 체지방 감소 기능성 물질을 중복 섭취하면 간독성 등 부작용이 생길 수 있어 소비자 주의가 요구된다.중금속과 미생물 등 안전성 역시 12개 제품 전부 기준에 적합했지만, 1개 제품은 추출용매인 초산에틸 잔류수준이 기준 부적합으로 나타났다.21일 한국소비자원은 체중 감소 건기식 품질·안전성 비교 결과를 공개했다.소비자원이 비교한 제품은 가르시니아 플러스, 그린몬스터 다이어트 스페셜2 가르시니아 900, 레드컷 가르시니아 비포, 스키니랩 가르시니아, 종근당 프리미엄 가르시니아 다이어트, 칼로-스탑 PLUS+, 녹차카테킨 다이어트 플러스, 메타그린 슬림업 30일, 사이클 다이어트 그린, GRN 올 뉴 초록이 시즌4, 카테킨400, 칼로커트 등 총 12개 품목이다.제품에 표시된 1일 섭취량 기준으로 가르시니아캄보지아 추출물 6개 제품은 기능성분(총(-)-HCA) 함량이 652㎎ ~ 999㎎, 녹차추출물 6개 제품은 기능성분(카테킨) 함량이 289㎎ ~ 467㎎으로 모두 관련 기준을 충족했다. 시험대상 12개 중 8개 제품은 비타민·무기질 및 기타 기능성분을 함유하고 있었으며, 모두 성분별 함량이 건강기능식품 기준을 충족했다. 가장 많은 제품에 들어간 영양성분은 판토텐산으로 총 6개 제품에 있었고 나이아신, 비타민C, 비타민B(B1,B2,B6)는 각각 4개 제품에 함유됐다. '카테킨 400(㈜더베이글)' 제품은 비타민·무기질이 12종으로 조사대상 제품 중 가장 많은 종류의 성분을 함유했으며, 각 영양성분은 1일 영양성분 기준치 대비 100% ~ 147% 수준이었다. 초산에틸은 식품첨가물로 추출용제나 향료로써 사용할 수 있는 기준과 용도가 정해져 있고 녹차추출물 제조 시 사용될 수 있다.이에 초산에틸 잔류량을 확인한 결과, 1개 제품이 잔류 기준에 부적합했다. 아모레퍼시픽 '메타그린 슬림업 30일'이 기준 부적합 품목이다. 해당 사업자는 소비자원 시정권고를 수용해 해당 원료를 사용한 전 제품을 회수하고 판매된 제품에 대해서는 환불 조치하기로 했다.식품의약품안전처는 해당 제품에 대한 수거검사를 진행했고, 검사 결과에 따라 건강기능식품법에 따른 회수 등의 행정조치를 진행 중이다.그 외 제조·가공 중 오염될 수 있는 중금속(납, 카드뮴, 비소, 수은)과 대장균군은 전 제품이 관련 기준에 적합했다.건기식은 관련 기준에 따라 기능성 원료에 적합한 주의사항을 표시해야 한다. 확인 결과 12개 제품 모두 관련 기준에 적합했다.다만, 가르시니아캄보지아 추출물은 체지방 감소 기능성을 표방하는 다른 건강기능식품과 함께 섭취 시 간 독성 등 이상 사례 발생 가능성이 보고된 바 있어 섭취에 주의가 필요하다.이에 '체지방 감소 기능성 제품의 중복섭취 주의 표시'를 조사한 결과 2개 제품에만 해당 표시가 있고, 나머지 10개 제품(9개 업체)은 별도 주의사항이 없어 추가 표시하도록 자율 개선을 권고했다.가르시니아캄보지아 추출물 6개 제품은 1일 섭취량(제품표시기준) 당 170원~921원으로 제품 간 5배, 녹차추출물 6개는 156원~5267원으로 제품 간 최대 34배 차이가 났다.가르시니아캄보지아 원료 제품은 `가르시니아 플러스(㈜대웅생명과학)'가 1일 섭취량(제품표시 기준) 당 가격이 170원으로 가장 저렴했고, 녹차추출물 원료 제품은 `녹차카테킨 다이어트 플러스(㈜대웅생명과학)'가 156원으로 가장 쌌다.2025-05-21 11:46:33이정환 -
 "부작용 속출 하는데"…건기식 중고거래 연장 반발[데일리팜=강혜경 기자] 식품의약품안전처가 개인간 건기식 거래 시범사업을 올해 연말까지 연장한다고 밝히면서 약사들의 반발이 커지고 있다.식약처는 오는 7일 종료 예정이던 건기식 소규모 개인간 거래 허용 시범사업 종료시한을 올해 12월 31일까지 연장한다고 밝혔다.개인간 거래된 제품에서 이상사례 발생 등 안전성 문제는 보고되지 않았고, 시범사업이 소비자 안전과 시장에 미치는 영향을 좀 더 살펴보겠다는 것이 정부 의견이다.번개장터를 통해 게시된 전문·일반약 거래. 하지만 이에 대한 약사들의 생각은 다르다. 개인간 건기식 거래가 빌미가 돼 일반약은 물론 전문약이 거래되는 사례는 물론, 복용·사용하던 의약품을 거래하는 사례 등 부작용이 속출했다는 것이다.약사나 소비자단체에 의해 적발된 불법 거래 건수 역시 적지 않다.대한약사회는 지난해 6월부터 올해 3월까지 진행한 시범사업 모니터링 결과 수도권에서만 375건의 위반 사례를 적발했다고 밝혔다.적발 사례 가운데는 전문약 연고제, 일반약 탈모치료제 등이 포함돼 있었다.약사회는 "모니터링 시간과 지역이 제한됐는데 이것을 전국, 24시간으로 확대하면 위반 사례가 훨씬 더 많을 것으로 예상된다"며 "드러난 사례들만 봐도 식약처가 제대로 모니터링을 하고 제한·단속하고 있는지 의문"이라고 문제를 제기했다.한국소비자원이 진행한 조사에서도 571건의 법·기준 위반 사례가 적발됐다.소비자원은 "중고거래 플랫폼 또는 일부 커뮤니티에서 의약품이 판매되는 사례가 67건 확인됐으며 이 가운데 비만치료제 주사제와 같은 처방이 필요한 전문의약품도 15건에 달하는 것으로 확인됐다"며 "거래불가·요건 부적합 건기식과 미신고 해외 식품 등까지 포함하면 571건"이라고 지적했다.지역 약사들 역시 시범사업 연장에 반대한다는 입장이다.지역의 한 약사는 "초창기 사후피임약, 암환자들을 위한 경장영양제 등 전문·일반약이 무작위하게 판매되던 것과 비교할 때 개인간 의약품 거래가 줄어들기는 했지만 여전히 영양제, 철분제, 연고제 등 일반약과 전문약이 판매되고 있다"면서 "불법 거래 등 부작용이 속출하고 있는데도 시범사업을 연장하겠다는 것은 이해되지 않는 처사"라고 꼬집었다.식약처는 중고거래가 가능한 플랫폼도 추가 확대하겠다고 밝히고 있다. 당근과 번개장터 이외 시범사업에 참여의사를 밝힌 중고나라 등 다른 플랫폼의 관리시스템 등을 살펴본 뒤 거래 가능 플랫폼을 추가로 확대한다는 계획이다.또 다른 약사도 "개인간 건기식 거래의 가장 큰 문제는 처분이 솜방망이에 그친다는 것"이라며 "'위반 게시글 삭제 조치' 이외 실효성 있는 처분 조치가 이행돼야 할 것"이라고 촉구했다.기존 플랫폼의 경우 1차 위반시 경고 조치 후 상품 삭제, 2차 위반시 3일 판매 제한, 3차 위반시 15일 판매 제한, 4차 위반시 30일 판매 제한, 5차 위반시 영구 판매 제한 조치 등을 표면적으로 내세우고 있으나 타인 명의 가입 등 사실상 이를 제재할 만한 수단이 없다는 지적이다.한편 이개호 더불어민주당 의원은 건기식판매업 신고자와 약사를 제외한 일반인들이 개인간 건기식 거래를 하지 못하도록 하는 건기식법 개정안을 대표발의했다.이 의원은 "법 사각지대를 악용한 건기식 중고거래가 사회적 문제를 초래하고 있다"며 "정부가 정한 기준에 따라 건기식 판매업소와 설비를 갖추지 않고, 지자체 신고 절차를 밟지 않은 일반인의 건기식 판매를 전면금지하는 취지의 법안으로, 무분별한 개인간 건기식 중고로 발생하는 국민 건강 문제와 건기식 유통 혼란 문제를 해소할 수 있을 것"이라고 설명했다.2025-05-02 11:12:25강혜경
"부작용 속출 하는데"…건기식 중고거래 연장 반발[데일리팜=강혜경 기자] 식품의약품안전처가 개인간 건기식 거래 시범사업을 올해 연말까지 연장한다고 밝히면서 약사들의 반발이 커지고 있다.식약처는 오는 7일 종료 예정이던 건기식 소규모 개인간 거래 허용 시범사업 종료시한을 올해 12월 31일까지 연장한다고 밝혔다.개인간 거래된 제품에서 이상사례 발생 등 안전성 문제는 보고되지 않았고, 시범사업이 소비자 안전과 시장에 미치는 영향을 좀 더 살펴보겠다는 것이 정부 의견이다.번개장터를 통해 게시된 전문·일반약 거래. 하지만 이에 대한 약사들의 생각은 다르다. 개인간 건기식 거래가 빌미가 돼 일반약은 물론 전문약이 거래되는 사례는 물론, 복용·사용하던 의약품을 거래하는 사례 등 부작용이 속출했다는 것이다.약사나 소비자단체에 의해 적발된 불법 거래 건수 역시 적지 않다.대한약사회는 지난해 6월부터 올해 3월까지 진행한 시범사업 모니터링 결과 수도권에서만 375건의 위반 사례를 적발했다고 밝혔다.적발 사례 가운데는 전문약 연고제, 일반약 탈모치료제 등이 포함돼 있었다.약사회는 "모니터링 시간과 지역이 제한됐는데 이것을 전국, 24시간으로 확대하면 위반 사례가 훨씬 더 많을 것으로 예상된다"며 "드러난 사례들만 봐도 식약처가 제대로 모니터링을 하고 제한·단속하고 있는지 의문"이라고 문제를 제기했다.한국소비자원이 진행한 조사에서도 571건의 법·기준 위반 사례가 적발됐다.소비자원은 "중고거래 플랫폼 또는 일부 커뮤니티에서 의약품이 판매되는 사례가 67건 확인됐으며 이 가운데 비만치료제 주사제와 같은 처방이 필요한 전문의약품도 15건에 달하는 것으로 확인됐다"며 "거래불가·요건 부적합 건기식과 미신고 해외 식품 등까지 포함하면 571건"이라고 지적했다.지역 약사들 역시 시범사업 연장에 반대한다는 입장이다.지역의 한 약사는 "초창기 사후피임약, 암환자들을 위한 경장영양제 등 전문·일반약이 무작위하게 판매되던 것과 비교할 때 개인간 의약품 거래가 줄어들기는 했지만 여전히 영양제, 철분제, 연고제 등 일반약과 전문약이 판매되고 있다"면서 "불법 거래 등 부작용이 속출하고 있는데도 시범사업을 연장하겠다는 것은 이해되지 않는 처사"라고 꼬집었다.식약처는 중고거래가 가능한 플랫폼도 추가 확대하겠다고 밝히고 있다. 당근과 번개장터 이외 시범사업에 참여의사를 밝힌 중고나라 등 다른 플랫폼의 관리시스템 등을 살펴본 뒤 거래 가능 플랫폼을 추가로 확대한다는 계획이다.또 다른 약사도 "개인간 건기식 거래의 가장 큰 문제는 처분이 솜방망이에 그친다는 것"이라며 "'위반 게시글 삭제 조치' 이외 실효성 있는 처분 조치가 이행돼야 할 것"이라고 촉구했다.기존 플랫폼의 경우 1차 위반시 경고 조치 후 상품 삭제, 2차 위반시 3일 판매 제한, 3차 위반시 15일 판매 제한, 4차 위반시 30일 판매 제한, 5차 위반시 영구 판매 제한 조치 등을 표면적으로 내세우고 있으나 타인 명의 가입 등 사실상 이를 제재할 만한 수단이 없다는 지적이다.한편 이개호 더불어민주당 의원은 건기식판매업 신고자와 약사를 제외한 일반인들이 개인간 건기식 거래를 하지 못하도록 하는 건기식법 개정안을 대표발의했다.이 의원은 "법 사각지대를 악용한 건기식 중고거래가 사회적 문제를 초래하고 있다"며 "정부가 정한 기준에 따라 건기식 판매업소와 설비를 갖추지 않고, 지자체 신고 절차를 밟지 않은 일반인의 건기식 판매를 전면금지하는 취지의 법안으로, 무분별한 개인간 건기식 중고로 발생하는 국민 건강 문제와 건기식 유통 혼란 문제를 해소할 수 있을 것"이라고 설명했다.2025-05-02 11:12:25강혜경 -
 건기식 업체 1971곳 점검...표시·광고 위반 등 2곳 적발[데일리팜=이혜경 기자] 식품의약품안전처(처장 오유경)는 5월 가정의 달을 맞아 선물용으로 많이 판매되는 건강기능식품의 안전관리를 강화하기 위해 제조·유통·수입 단계와 온라인 부당광고에 대해 지자체와 함께 4월 7일부터 4월 18일까지 종합 점검을 실시했다고 밝혔다.건강기능식품 제조·판매업체 1,971곳을 점검한 결과, 표시·광고 규정을 위반한 업체와 안전 교육을 수료하지 않은 업체 총 2곳(더포레스트, 서울북부두레소비자생활협동조합)을 적발하였으며, 적발된 업체는 관할 관청에서 행정처분 등의 조치 후 6개월 이내에 다시 점검해 개선 여부를 확인할 예정이다.국내 시장 점유율이 높은 홍삼, 프로바이오틱스, 복합영양소 제품 등에 대한 기능성분·영양성분 함량, 대장균군, 중금속 등 기준·규격 적합 여부를 확인하기 위해 국내 유통 중인 건강기능식품 180건(국내 80, 수입 100)을 수거·검사했다.회수조치가 이뤄진 건강기능식품 제품 3건. 검사 결과 제품 3건(국내 1, 수입 2)이 프로바이오틱스 수 함량, 과산화물가(EPA 및 DHA 함유 유지 제품), 붕해시험(영양소·기능성복합제품)에서 부적합 판정되어 회수폐기 등을 요청했다.국내로 정식 수입 전 통관 단계에서 수입 비타민 제품 등 114건에 대한 정밀검사 결과, 1건이 프로바이오틱스 수 함량 부족으로 부적합 판정되어 수출국으로 반송하거나 폐기할 예정이다.소비자들이 온라인 쇼핑몰 등에서 건강기능식품 구매 시 주로 검색하는 키워드인 혈행건강, 관절건강, 비염 등으로 광고·판매되는 제품 게시물의 부당광고 여부를 집중 점검했다.점검 결과 위반 게시물 104건을 적발했으며, 주요 위반 내용은 ▲골다공증 예방 등 질병 예방·치료 효능의 인식 우려 광고(78건) ▲일반식품을 건강기능식품으로 인식할 우려가 있는 광고(19건) ▲기관지보호 등 인정하지 않은 기능성 거짓·과장 광고(3건) ▲체험기를 이용한 소비자 기만 광고(2건) ▲혈행개선제 등 의약품 인식 우려 광고(2건)이다.'식품 등의 표시·광고에 관한 법률' 위반 게시물은 방송통신심의위원회 등에 접속 차단을 요청하고, 관할 기관에 행정처분 등을 요청했다.식약처는 "앞으로도 특정 시기에 소비가 증가하는 건강기능식품 등에 대한 사전 점검을 실시해 식품 등 안전사고를 예방하고, 허위·과대 광고 등 불법행위를 지속적으로 점검하여 국민이 안심하고 건강기능식품을 소비할 수 있는 환경을 조성하기 위해 최선을 다할 계획"이라고 밝혔다.건강기능식품을 구매할 때는 허위과대 광고에 현혹되지 않고 제품에 표시된 건강기능식품 문구나 도안을 반드시 확인해야 한다고 강조했으며, 검사 부적합 제품은 신속히 구입처에 반품해야 한다.2025-05-02 09:25:18이혜경
건기식 업체 1971곳 점검...표시·광고 위반 등 2곳 적발[데일리팜=이혜경 기자] 식품의약품안전처(처장 오유경)는 5월 가정의 달을 맞아 선물용으로 많이 판매되는 건강기능식품의 안전관리를 강화하기 위해 제조·유통·수입 단계와 온라인 부당광고에 대해 지자체와 함께 4월 7일부터 4월 18일까지 종합 점검을 실시했다고 밝혔다.건강기능식품 제조·판매업체 1,971곳을 점검한 결과, 표시·광고 규정을 위반한 업체와 안전 교육을 수료하지 않은 업체 총 2곳(더포레스트, 서울북부두레소비자생활협동조합)을 적발하였으며, 적발된 업체는 관할 관청에서 행정처분 등의 조치 후 6개월 이내에 다시 점검해 개선 여부를 확인할 예정이다.국내 시장 점유율이 높은 홍삼, 프로바이오틱스, 복합영양소 제품 등에 대한 기능성분·영양성분 함량, 대장균군, 중금속 등 기준·규격 적합 여부를 확인하기 위해 국내 유통 중인 건강기능식품 180건(국내 80, 수입 100)을 수거·검사했다.회수조치가 이뤄진 건강기능식품 제품 3건. 검사 결과 제품 3건(국내 1, 수입 2)이 프로바이오틱스 수 함량, 과산화물가(EPA 및 DHA 함유 유지 제품), 붕해시험(영양소·기능성복합제품)에서 부적합 판정되어 회수폐기 등을 요청했다.국내로 정식 수입 전 통관 단계에서 수입 비타민 제품 등 114건에 대한 정밀검사 결과, 1건이 프로바이오틱스 수 함량 부족으로 부적합 판정되어 수출국으로 반송하거나 폐기할 예정이다.소비자들이 온라인 쇼핑몰 등에서 건강기능식품 구매 시 주로 검색하는 키워드인 혈행건강, 관절건강, 비염 등으로 광고·판매되는 제품 게시물의 부당광고 여부를 집중 점검했다.점검 결과 위반 게시물 104건을 적발했으며, 주요 위반 내용은 ▲골다공증 예방 등 질병 예방·치료 효능의 인식 우려 광고(78건) ▲일반식품을 건강기능식품으로 인식할 우려가 있는 광고(19건) ▲기관지보호 등 인정하지 않은 기능성 거짓·과장 광고(3건) ▲체험기를 이용한 소비자 기만 광고(2건) ▲혈행개선제 등 의약품 인식 우려 광고(2건)이다.'식품 등의 표시·광고에 관한 법률' 위반 게시물은 방송통신심의위원회 등에 접속 차단을 요청하고, 관할 기관에 행정처분 등을 요청했다.식약처는 "앞으로도 특정 시기에 소비가 증가하는 건강기능식품 등에 대한 사전 점검을 실시해 식품 등 안전사고를 예방하고, 허위·과대 광고 등 불법행위를 지속적으로 점검하여 국민이 안심하고 건강기능식품을 소비할 수 있는 환경을 조성하기 위해 최선을 다할 계획"이라고 밝혔다.건강기능식품을 구매할 때는 허위과대 광고에 현혹되지 않고 제품에 표시된 건강기능식품 문구나 도안을 반드시 확인해야 한다고 강조했으며, 검사 부적합 제품은 신속히 구입처에 반품해야 한다.2025-05-02 09:25:18이혜경 -
 지자체, 약국·도매 등 동물약 취급업소 일제 점검[데일리팜=강신국 기자] 지차제가 5월부터 동물약 취급업소에 대한 일제 단속에 나선다.먼저 충남도는 5월 1일부터 6월 30일까지 2개월간 동물용 의약품을 취급하는 도매업소와 약국을 대상으로 점검을 시작한다.주요 점검 내용은 ▲판매업 시설의 적합 여부 ▲관리약사의 관리 실태 ▲동물용 의약품 관리 적정 여부 ▲무허가·유효기간 경과 제품 등의 보관·판매 ▲처방 대상 동물용 의약품의 임의 판매 여부 ▲관계 규정 및 행정 지시 사항 준수 여부 등이다.점검 결과 위반 사항 발견 시 가벼운 사안은 지도 및 현장 시정조치하고 법령 위반 등 중대 사안은 확인서 징수 및 행정처분을 실시할 예정이다.또 시중에 유통되는 동물용 의약품의 성분 함량 등 품질 검증을 위해 항생물질제제 75건 및 일반화학제제 40건 등 총 115건을 수거 검사할 예정이며, 검사 결과 부적합 제품은 수거·폐기 등 규정에 따라 조치할 방침이다.조수일 충남도 동물방역위생과장은 "이번 점검을 통해 동물용 의약품의 품질을 검증하고 유통 질서를 확립하겠다"며 "동물용 의약품 소매자 보호와 약화사고 방지에 최선을 다하겠다"고 말했다.또한 전북자치도는 5월 1일부터 한 달 간 동물용의약품 도매업소와 동물병원·약국 등 853곳을 일제 점검을 한다고 30일 밝혔다.주요 점검항목은 ▲처방대상 동물용의약품의 처방전 발급 준수 여부 ▲임의판매 여부 ▲동물약국·도매업소 약사 근무실태 ▲무허가·유효기간 경과 제품 판매 여부 ▲판매업 시설 적합 여부 등이다.또한 유통 중인 의약품 품질 확인을 위해 항생치료약제 75건, 일반화학제제 40건 등 총 115건은 수거해 검사한다. 이 중 24건은 반려동물용 의약품을 포함해 진행된다.전북도는 지난해 811개 업소를 점검해 '동물용의약품 판매기록 누락', '관리약사 교육 미실시' 등의 위반사항으로 7개 업소를 적발했으며, 이들 업소의 조치사항 이행 여부도 중점적으로 확인할 계획이다.최재용 농생명축산산업국장은 "이번 점검을 통해 부적합하거나 불법 유통되는 동물용의약품을 사전 차단해 축산농가와 반려동물 보호자 모두가 안심하고 사용할 수 있는 의약품 유통환경을 조성하겠다"고 밝혔다.2025-04-30 11:23:20강신국
지자체, 약국·도매 등 동물약 취급업소 일제 점검[데일리팜=강신국 기자] 지차제가 5월부터 동물약 취급업소에 대한 일제 단속에 나선다.먼저 충남도는 5월 1일부터 6월 30일까지 2개월간 동물용 의약품을 취급하는 도매업소와 약국을 대상으로 점검을 시작한다.주요 점검 내용은 ▲판매업 시설의 적합 여부 ▲관리약사의 관리 실태 ▲동물용 의약품 관리 적정 여부 ▲무허가·유효기간 경과 제품 등의 보관·판매 ▲처방 대상 동물용 의약품의 임의 판매 여부 ▲관계 규정 및 행정 지시 사항 준수 여부 등이다.점검 결과 위반 사항 발견 시 가벼운 사안은 지도 및 현장 시정조치하고 법령 위반 등 중대 사안은 확인서 징수 및 행정처분을 실시할 예정이다.또 시중에 유통되는 동물용 의약품의 성분 함량 등 품질 검증을 위해 항생물질제제 75건 및 일반화학제제 40건 등 총 115건을 수거 검사할 예정이며, 검사 결과 부적합 제품은 수거·폐기 등 규정에 따라 조치할 방침이다.조수일 충남도 동물방역위생과장은 "이번 점검을 통해 동물용 의약품의 품질을 검증하고 유통 질서를 확립하겠다"며 "동물용 의약품 소매자 보호와 약화사고 방지에 최선을 다하겠다"고 말했다.또한 전북자치도는 5월 1일부터 한 달 간 동물용의약품 도매업소와 동물병원·약국 등 853곳을 일제 점검을 한다고 30일 밝혔다.주요 점검항목은 ▲처방대상 동물용의약품의 처방전 발급 준수 여부 ▲임의판매 여부 ▲동물약국·도매업소 약사 근무실태 ▲무허가·유효기간 경과 제품 판매 여부 ▲판매업 시설 적합 여부 등이다.또한 유통 중인 의약품 품질 확인을 위해 항생치료약제 75건, 일반화학제제 40건 등 총 115건은 수거해 검사한다. 이 중 24건은 반려동물용 의약품을 포함해 진행된다.전북도는 지난해 811개 업소를 점검해 '동물용의약품 판매기록 누락', '관리약사 교육 미실시' 등의 위반사항으로 7개 업소를 적발했으며, 이들 업소의 조치사항 이행 여부도 중점적으로 확인할 계획이다.최재용 농생명축산산업국장은 "이번 점검을 통해 부적합하거나 불법 유통되는 동물용의약품을 사전 차단해 축산농가와 반려동물 보호자 모두가 안심하고 사용할 수 있는 의약품 유통환경을 조성하겠다"고 밝혔다.2025-04-30 11:23:20강신국 -
 고려은단 멀티비타민 요오드 함량 표시 '제각각'...이유는?[데일리팜=이혜경 기자] 고려은단이 시중에 판매하고 있는 '멀티비타민 올인원' 제품을 확인한 결과, 같은 제품이더라도 요오드 함량 표시가 제각각인 것으로 나타났다.식품의약품안전처의 '건강기능식품의 기준 및 규격'을 보면 요오드 영양소의 경우 일일섭취량은 45~150μg으로 이 범위 안에서 함량을 맞춰 포장지나 라벨에 표시가 가능하다. 이때 표시된 함량의 80~150% 범위가 유지되면 '적합'한 규격으로 인정된다.최근 요오드 함량 표시 기준 초과로 논란이 되고 있는 멀티비타민 올인원 60정의 경우 제품 내 요오드 함량으로 60μg가 표시됐으며, 규격만 놓고 보면 48~90μg 함량까지만 해당 표시에 적합한 요오드 함량이다.시중에 유통 중인 고려은단의 '멀티비타민 올인원' 제품의 요오드 성분은 제품 마다 달랐다.현재 180ug는 품목변경으로 생산되지 않으며, 소비기한이 남은 품목만 유통중이다. 하지만 고려은단이 자가품질검사을 진행하는 과정에서 60μg표시 제품의 요오드 함량으로 129.7μg이 나왔고 '부적합' 결과로 회수 조치가 이뤄진 셈이다.해당 수치는 식약처 1일 섭취 권장량 150μg의 86% 수준으로 소비자 건강에 위해를 줄 만한 수준은 아니지만 검사 결과가 표시 기준 60μg(식약처 1일 섭취 권장량의 40%)보다 초과되면서 규격위반으로 회수해야 한다.따라서 같은 멀티비타민 올인원 제품이라고 하더라도 식약처 1일 섭취 권장량 150μg의 150% 범위를 초과하지 않는 범위에서 요오드 함량을 유지하면 '적합' 제품으로 판매가 가능하다는 얘기다.현재 회수 대상 제품명은 '멀티비타민 올인원' 60정으로 2025년 2월 11일에 생산된 멀티비타민 올인원 제품 중 케이스 밑면 바코드번호(8809497531729) 이후 끝 4자리로 표기된 제조번호 '1460'과 소비 기한이 2027년 02월 10일까지로 표기된 제품이다.나머지 요오드 함량으로 품목보고한 제품들은 표시기준을 초과하지 않아 시중에 유통 중이다.이런 방식으로 현재 시중에 유통되고 있는 멀티비타민 올인원의 경우 요오드 함량이 60μg, 120μg, 180μg 등 다양하게 표시되고 있다.건강기능식품의 경우 1일 섭취 허용량 기준이 명확하지 않은 상황이다.현재로서는 영양소 필요량을 충족시키는 섭취량인 '권장섭취량', 권장섭취량의 과학적 근거가 부족할 경우 건강을 유지하는데 충분한 양을 설정한 섭취량인 '충분섭취량', 인체에 유해한 영향이 나타나지 않는 최대 영양소 섭취량인 '상한섭취량'으로 볼 수 있다.식약처 관계자는 "건강기능식품의 섭취 허용량 기준을 무엇으로 보느냐에 따라서 달라질 수 있다"며 "요오드의 경우 식약처의 권장 섭취량은 150μg이지만, 한국영양학회가 5년마다 개정하는 한국인 영양소 섭취 기준을 보면 최대 2400μg까지 섭취할 수 있도록 하고 있다"고 했다.세계보건기구(WHO)에서 권장하는 성인 기준 일일 상한 섭취량은 약 1100μg이지만 한국인의 경우 김, 미역국, 다시마 같은 요오드가 풍부한 해조류 식단이 많아 섭취량이 조정된 것으로 알려졌다.그는 "고려은단 멀티비타민의 경우 식약처 권장섭취량 기준에 미치지 못하지만 제품에 표시된 60μg보다 200% 넘는 함량이 나오면서 회수조치가 이뤄진 것"이라고 했다.식약처 건강기능식품 기준 및 규격에 따른 요오드 표시 기준 및 섭취 허용량. 한편 요오드는 갑상선 호르몬의 합성에 필요, 에너지 생성에 필요, 신경발달에 필요 등의 기능성을 갖고 있어 미네랄·비타민 복합 영양제 같은 건기식에 기본적으로 포함되고 있다.요오드는 우리 몸에서 갑상선 호르몬을 만드는 데 꼭 필요한 미네랄 성분으로, 갑상선 호르몬은 대사 조절, 체온 유지, 뇌 발달, 성장 등 정말 많은 생리적 기능에 관여하는데, 요오드가 부족하면 갑상선 기능 저하증, 임신 중 결핍 등의 부작용이 생긴다.식약처 관계자는 "요오드 함량의 경우 식약처 권장섭취량인 150μg 초과할 경우의 이상증세에 대한 자료는 없다"며 "다만 최대 허용량인 2400μg을 초과할 경우 입이나 목, 복부 등의 통증을 비롯해 발열, 오심, 구토, 설사 등의 증상이 즉시 나타날 수 있다"고 설명했다.그는 "요오드는 영양소로 섭취량에 따른 개인적인 차이는 발생할 수 있다"며 "건강기능식품으로 최대 섭취량을 초과할 경우 발생하는 증상 정도만 확인 가능하다"고 덧붙였다.2025-04-25 09:12:45이혜경
고려은단 멀티비타민 요오드 함량 표시 '제각각'...이유는?[데일리팜=이혜경 기자] 고려은단이 시중에 판매하고 있는 '멀티비타민 올인원' 제품을 확인한 결과, 같은 제품이더라도 요오드 함량 표시가 제각각인 것으로 나타났다.식품의약품안전처의 '건강기능식품의 기준 및 규격'을 보면 요오드 영양소의 경우 일일섭취량은 45~150μg으로 이 범위 안에서 함량을 맞춰 포장지나 라벨에 표시가 가능하다. 이때 표시된 함량의 80~150% 범위가 유지되면 '적합'한 규격으로 인정된다.최근 요오드 함량 표시 기준 초과로 논란이 되고 있는 멀티비타민 올인원 60정의 경우 제품 내 요오드 함량으로 60μg가 표시됐으며, 규격만 놓고 보면 48~90μg 함량까지만 해당 표시에 적합한 요오드 함량이다.시중에 유통 중인 고려은단의 '멀티비타민 올인원' 제품의 요오드 성분은 제품 마다 달랐다.현재 180ug는 품목변경으로 생산되지 않으며, 소비기한이 남은 품목만 유통중이다. 하지만 고려은단이 자가품질검사을 진행하는 과정에서 60μg표시 제품의 요오드 함량으로 129.7μg이 나왔고 '부적합' 결과로 회수 조치가 이뤄진 셈이다.해당 수치는 식약처 1일 섭취 권장량 150μg의 86% 수준으로 소비자 건강에 위해를 줄 만한 수준은 아니지만 검사 결과가 표시 기준 60μg(식약처 1일 섭취 권장량의 40%)보다 초과되면서 규격위반으로 회수해야 한다.따라서 같은 멀티비타민 올인원 제품이라고 하더라도 식약처 1일 섭취 권장량 150μg의 150% 범위를 초과하지 않는 범위에서 요오드 함량을 유지하면 '적합' 제품으로 판매가 가능하다는 얘기다.현재 회수 대상 제품명은 '멀티비타민 올인원' 60정으로 2025년 2월 11일에 생산된 멀티비타민 올인원 제품 중 케이스 밑면 바코드번호(8809497531729) 이후 끝 4자리로 표기된 제조번호 '1460'과 소비 기한이 2027년 02월 10일까지로 표기된 제품이다.나머지 요오드 함량으로 품목보고한 제품들은 표시기준을 초과하지 않아 시중에 유통 중이다.이런 방식으로 현재 시중에 유통되고 있는 멀티비타민 올인원의 경우 요오드 함량이 60μg, 120μg, 180μg 등 다양하게 표시되고 있다.건강기능식품의 경우 1일 섭취 허용량 기준이 명확하지 않은 상황이다.현재로서는 영양소 필요량을 충족시키는 섭취량인 '권장섭취량', 권장섭취량의 과학적 근거가 부족할 경우 건강을 유지하는데 충분한 양을 설정한 섭취량인 '충분섭취량', 인체에 유해한 영향이 나타나지 않는 최대 영양소 섭취량인 '상한섭취량'으로 볼 수 있다.식약처 관계자는 "건강기능식품의 섭취 허용량 기준을 무엇으로 보느냐에 따라서 달라질 수 있다"며 "요오드의 경우 식약처의 권장 섭취량은 150μg이지만, 한국영양학회가 5년마다 개정하는 한국인 영양소 섭취 기준을 보면 최대 2400μg까지 섭취할 수 있도록 하고 있다"고 했다.세계보건기구(WHO)에서 권장하는 성인 기준 일일 상한 섭취량은 약 1100μg이지만 한국인의 경우 김, 미역국, 다시마 같은 요오드가 풍부한 해조류 식단이 많아 섭취량이 조정된 것으로 알려졌다.그는 "고려은단 멀티비타민의 경우 식약처 권장섭취량 기준에 미치지 못하지만 제품에 표시된 60μg보다 200% 넘는 함량이 나오면서 회수조치가 이뤄진 것"이라고 했다.식약처 건강기능식품 기준 및 규격에 따른 요오드 표시 기준 및 섭취 허용량. 한편 요오드는 갑상선 호르몬의 합성에 필요, 에너지 생성에 필요, 신경발달에 필요 등의 기능성을 갖고 있어 미네랄·비타민 복합 영양제 같은 건기식에 기본적으로 포함되고 있다.요오드는 우리 몸에서 갑상선 호르몬을 만드는 데 꼭 필요한 미네랄 성분으로, 갑상선 호르몬은 대사 조절, 체온 유지, 뇌 발달, 성장 등 정말 많은 생리적 기능에 관여하는데, 요오드가 부족하면 갑상선 기능 저하증, 임신 중 결핍 등의 부작용이 생긴다.식약처 관계자는 "요오드 함량의 경우 식약처 권장섭취량인 150μg 초과할 경우의 이상증세에 대한 자료는 없다"며 "다만 최대 허용량인 2400μg을 초과할 경우 입이나 목, 복부 등의 통증을 비롯해 발열, 오심, 구토, 설사 등의 증상이 즉시 나타날 수 있다"고 설명했다.그는 "요오드는 영양소로 섭취량에 따른 개인적인 차이는 발생할 수 있다"며 "건강기능식품으로 최대 섭취량을 초과할 경우 발생하는 증상 정도만 확인 가능하다"고 덧붙였다.2025-04-25 09:12:45이혜경
오늘의 TOP 10
- 1'메가팩토리' 약국장, 금천 홈플러스 내 600평 약국 개설
- 2'클릭' 한번에 사후통보 가능…대체조제, 숨통 트인다
- 3제약 CEO 45% "사업 전망 부정적"...약가개편 걸림돌
- 4개미들, 바이오 4.7조 순매수…삼성에피스·알테오젠 집중
- 5명인제약, 락업 해제에 주가 조정…실적·신약 체력은 탄탄
- 6닥터나우 도매금지법, 국회 처리 진퇴양난…원안 유지될까
- 7약국 혈액순환제 선택기준, 답은 '고객의 말'에 있다
- 8'김태한 카드' 꺼낸 HLB, 리보세라닙 FDA 허가 총력전
- 91%대 대체조제 얼마나 늘까?..."품절약·원거리 처방부터"
- 10씨투스 후발주자에 경쟁 과열...한국프라임, 급여 진입
-
상품명최고최저평균
-
게보린(10정)4,0003,0003,782
-
노스카나겔(20g)22,00018,00021,195
-
베나치오에프액(75ml)1,000800996
-
비코그린에스(20정)5,0004,5004,625
-
머시론정(21정)10,0008,5009,873
























![[종근당] 벤포벨에스 어른들의 피로회복제](https://cdn.platpharm.co.kr/2025/07/2507290841210004645.webp)
![[SK케미칼] 트라스트패취 피록시캄 성분](https://cdn.platpharm.co.kr/2025/10/2510020656150002375.webp)
![[신신] 새사래 상처연고 습윤밴드](https://cdn.platpharm.co.kr/2025/10/2510210339570001784.webp)
![[SK케미칼] 속편한정 복합소화제](https://cdn.platpharm.co.kr/2025/12/2512040916400005920.webp)
![[리쥬올]레티노 멜라세럼 저자극 레티놀](https://cdn.platpharm.co.kr/2025/09/2509260219360000145.webp)
![[신신] 아렉스 두번효과로 강력한](https://cdn.platpharm.co.kr/2025/10/2510230254510000664.webp)
![[리쥬올]리쥬올 PDRN 약국 1위 PDRN](https://cdn.platpharm.co.kr/2025/09/2509260220180000170.webp)
![[셀로맥스] 베베락스 온가족 안심 관장약](https://cdn.platpharm.co.kr/2025/09/2509171131320018843.webp)
![[위고비] 직거래 최저가](https://cdn.platpharm.co.kr/2025/12/2512020211090000013.webp)
![[더본메디칼] ATC인쇄리본 특가](https://cdn.platpharm.co.kr/2025/04/2504100527360001454.jpg)
![[유한양행] 미녹펜겔 탈모스팟 집중케어](https://cdn.platpharm.co.kr/2025/09/2509220824180004563.webp)
![[유한양행] 콘택콜드 걸렸구나 생각되면](https://cdn.platpharm.co.kr/2025/10/2510282252420008436.webp)
![[오펠라] 부드럽고 편안한, 둘코락스에스장용정 20정](https://i.baropharm.com/products/202511/1762260404625.png)
![[아워팜] 우리아이 맞춤설계, 바로타민 kids 엘더베리맛](https://i.baropharm.com/products/8eae7689-61be-4b71-9608-05364b05ea12.png)
![[아워팜] 에너지 바로 충전, 바로콤](https://i.baropharm.com/products/202512/1764922282624.png)
![[레킷코리아] 목 아플 때, 스트렙실 허니&레몬 트로키 12정](https://i.baropharm.com/products/202502/1739520767049.png?label=PLAN_01)
![[켄뷰] 다양한 통증에, 타이레놀정 500mg 10정](https://i.baropharm.com/products/6c6ea4f4-7ab2-44f2-a165-f062d80f525b.png)
![[아워팜] CJ웰케어, 바이오코어 1000억 유산균](https://i.baropharm.com/products/202512/1765955416559.png)
![[한독] 붙이는 통증 전문가, 케토톱 액티브 플라스타(쿨) 40매](https://i.baropharm.com/products/202503/1741829602305.png)
![[켄뷰] 오리지널 폼타입, 로게인5%폼에어로졸60g](https://i.baropharm.com/products/dc84d96e-d0b4-46bc-bcc8-d62016406fe4.png)
![[휴온스 ] 비듬을 한번에, 니조랄 2%액](https://i.baropharm.com/products/478a284d-4361-4b4a-8a00-8bab80f34319.png?label=PLAN_01)
![[아워팜] 아이들이 먼저찾는, 바로타민 kids 미네랄](https://i.baropharm.com/products/202512/1766121243228.png)
![[아워팜] 혈행건강 히어로, 혈행건강 초임계 rTG 오메가3 프리미엄](https://i.baropharm.com/products/f724f191-7052-4ad5-bc92-cda889cf13a6.png)
![[아워팜] 건강한 힘, 바로바이오틱스 kids 비피더스 50억](https://i.baropharm.com/products/202511/1763106585375.png)
