총 1,363건
-
 "제2의 콜린알포 안된다" 건약, 급여 재평가 확대 촉구[데일리팜=강혜경 기자]내일(15일) 열리는 약제급여평가위원회(이하 약평위)를 앞두고 약사단체가 급여적정성 재평가 확대·개편을 촉구하고 나섰다. 급여적정성 재평가는 환자의 안전과 건강보험 재정을 지키는 최소한의 조치로, 제2의 콜린알포세레이트 사태가 남발돼서는 안된다는 주장이다. 건강사회를위한약사회(대표 전경림, 이하 건약)는 14일 성명을 통해 "지난 11월 28일 약가제도 개선방안 발표 이후 급여 재평가 제도의 근간이 흔들리고 제약업계 편의만을 봐주는 방향으로 흐르는 현 상황에 대해 깊은 우려를 표한다"며 "재평가 축소를 위한 꼼수 개편안은 전면 백지화돼야 한다"고 촉구했다. 이들은 "급여적정성 재평가 제도의 취지는 현재의 과학적 기준으로는 효과를 입증하기 어려운 약들을 걸러내는 것"이라며 "효과 없는 약을 퇴출시켜 환자의 안전을 위협하는 요소를 제거하고, 낭비되는 건강보험 재정을 지키기 위해 시작된 제도인 만큼 정당성은 결코 훼손돼서는 안된다"고 주장했다. 특히 이들은 지난 11월 발표된 약가제도 개선방안에 '새로운 데이터가 발견되거나 전문가들이 문제를 제기한 경우'에만 재평가를 하겠다고 담긴 부분에 대해서도 지적했다. 이들은 "청구액 규모나 등재 시기와 상관없이 임상적 유용성이 불분명한 약제라면 환자의 안전과 재정 누수를 위해 예외 없이 재평가 대상에 포함돼야 한다"며 "지금은 축소를 논할 때가 아닌 확대 개편이 필요한 시점"이라고 강조했다. 그러면서 재평가 제도의 예측 가능성과 투명성 확보를 촉구했다. 재평가 대상 선정 기준을 명확히 하고 제약사가 임상적 가치를 소명할 수 있는 투명한 논의구조가 필요함에도 이번 개선안은 이러한 문제 해결은 외면한 채 단순히 평가 대상을 어떻게 정할지 논의하는 수준에 그치고 있다는 것. 건약은 "의학적 근거가 부족함에도 모호한 사회적 요구도를 핑계로 살아남은 약제들 때문에 일선 약국에서는 불필요한 민원과 행정비용 낭비로 골머리를 앓고 있다"며 "기준 없는 봐주기식 평가는 결국 현장의 혼란과 사회적 비용으로 돌아올 것"이라고 비판했다. 이어 "복지부는 고무줄 같은 사회적 요구도 기준을 걷어치우고 투명하고 과학적인 기준으로 옥석을 가려내야 할 것"이라고 주문했다. 끝으로 이들은 "복지부와 약평위는 국민의 건강권을 담보로 제약사의 이익을 대변해서는 안 될 것"이라며 "재평가 제도를 확대 개편하고 과학적 엄밀성과 투명성을 강화할 것을 촉구하는 바"라고 덧붙였다.2026-01-14 13:58:36강혜경 기자
"제2의 콜린알포 안된다" 건약, 급여 재평가 확대 촉구[데일리팜=강혜경 기자]내일(15일) 열리는 약제급여평가위원회(이하 약평위)를 앞두고 약사단체가 급여적정성 재평가 확대·개편을 촉구하고 나섰다. 급여적정성 재평가는 환자의 안전과 건강보험 재정을 지키는 최소한의 조치로, 제2의 콜린알포세레이트 사태가 남발돼서는 안된다는 주장이다. 건강사회를위한약사회(대표 전경림, 이하 건약)는 14일 성명을 통해 "지난 11월 28일 약가제도 개선방안 발표 이후 급여 재평가 제도의 근간이 흔들리고 제약업계 편의만을 봐주는 방향으로 흐르는 현 상황에 대해 깊은 우려를 표한다"며 "재평가 축소를 위한 꼼수 개편안은 전면 백지화돼야 한다"고 촉구했다. 이들은 "급여적정성 재평가 제도의 취지는 현재의 과학적 기준으로는 효과를 입증하기 어려운 약들을 걸러내는 것"이라며 "효과 없는 약을 퇴출시켜 환자의 안전을 위협하는 요소를 제거하고, 낭비되는 건강보험 재정을 지키기 위해 시작된 제도인 만큼 정당성은 결코 훼손돼서는 안된다"고 주장했다. 특히 이들은 지난 11월 발표된 약가제도 개선방안에 '새로운 데이터가 발견되거나 전문가들이 문제를 제기한 경우'에만 재평가를 하겠다고 담긴 부분에 대해서도 지적했다. 이들은 "청구액 규모나 등재 시기와 상관없이 임상적 유용성이 불분명한 약제라면 환자의 안전과 재정 누수를 위해 예외 없이 재평가 대상에 포함돼야 한다"며 "지금은 축소를 논할 때가 아닌 확대 개편이 필요한 시점"이라고 강조했다. 그러면서 재평가 제도의 예측 가능성과 투명성 확보를 촉구했다. 재평가 대상 선정 기준을 명확히 하고 제약사가 임상적 가치를 소명할 수 있는 투명한 논의구조가 필요함에도 이번 개선안은 이러한 문제 해결은 외면한 채 단순히 평가 대상을 어떻게 정할지 논의하는 수준에 그치고 있다는 것. 건약은 "의학적 근거가 부족함에도 모호한 사회적 요구도를 핑계로 살아남은 약제들 때문에 일선 약국에서는 불필요한 민원과 행정비용 낭비로 골머리를 앓고 있다"며 "기준 없는 봐주기식 평가는 결국 현장의 혼란과 사회적 비용으로 돌아올 것"이라고 비판했다. 이어 "복지부는 고무줄 같은 사회적 요구도 기준을 걷어치우고 투명하고 과학적인 기준으로 옥석을 가려내야 할 것"이라고 주문했다. 끝으로 이들은 "복지부와 약평위는 국민의 건강권을 담보로 제약사의 이익을 대변해서는 안 될 것"이라며 "재평가 제도를 확대 개편하고 과학적 엄밀성과 투명성을 강화할 것을 촉구하는 바"라고 덧붙였다.2026-01-14 13:58:36강혜경 기자 -
 생필품 배달원된 MR...판결문에 드러난 리베이트 백태[데일리팜=김지은 기자] 의약품 리베이트의 액수가 소액이라 하더라도 제재를 피할 수는 없다는 법원의 판단이 나왔다. 영업사원의 개인적 일탈에 불과하다는 제약사의 주장에도 법원은 의약품 판촉을 목적으로 한 리베이트 행위의 책임은 결국 회사에 귀속된다고 못 박았다. 서울행정법원은 최근 A제약사가 식품의약품안전처장과 대전지방식품의약품안전청장을 상대로 제기한 의약품 판매업무정지처분 등 취소 청구 소송을 모두 기각했다. 이 회사는 지난 2023년 식약처가 자사 특정 의약품에 대한 3개월의 판매업무정지처분을, 대전식약청이 같은 기간 특정 의약품들에 대한 3개월의 판매업무정지, 해당 의약품들에 대한 2700여만원의 과징금 부과 처분이 내려진데 대해 반발해 이번 소송을 제기했다. 이번 사건은 A제약사의 영업사원인 B과장이 의약품 채택·처방유도 등 판매촉진을 목적으로 지난 2016년 5월부터 9월까지 4회에 걸쳐 서울의 한 내과의원에 10만원 내지 20만원 상당 물품으로 경제적 이익을 제공한 것이 발각되면서 불거졌다. 당시 육아휴직 중이었던 B과장은 병원 간호사 등 직원으로부터 병원에 필요한 생필품 등의 내역을 문자메시지로 전송받으면 자신의 하급자인 C영업사원에게 관련 내용을 전송한 후 구매해 병원에 배송할 수 있도록 한 것으로 확인됐다. 법정에서는 B과장이 물품을 제공한 내과 간호사로부터 전송된 생필품 내역 등이 기재된 문자메시지가 리베이트 증거 자료로 공개되기도 했다. 이번 소송에서 A회사 측은 사건의 의료기관이 리베이트 관련 수사를 받거나 행정처분을 받지 않은 만큼, 회사와 해당 의료기관 간 리베이트를 주고 받은 사실이 인정되지 않는다고 주장했다. 오히려 직원인 B과장이 육아휴직 중 인센티브에 갈음해 개인적 용도로 법인카드를 유용한 것에 불과할 뿐이며, 설령 리베이트 행위를 했다 하더라도 B과장의 개인적 일탈 행위에 불과하다고도 항변했다. 이 같은 회사 측 주장을 법원은 인정하지 않았다. 정황으로 볼 때 리베이트가 분명하며, 특정 의약품 판촉을 위한 리베이트의 책임은 곧 회사에 있음을 분명히 했다. 재판부는 “B가 육아휴직 중임에도 하급자인 C에게 4개월이라는 단기간 내 여러차례 걸쳐, 또 구체적 지시를 한점, 이 사건 의료기관이 요구한 각 물품 모두 병원에서 사용하는 물건으로 볼 수 있는 점 등을 보면 B의 개인적 일탈행위에 불과하다고 볼 수 없다”고 지적했다. 이어 “회사 법인카드로 B가 특정 마트에서 물건들을 구입해 사건 의료기관 간호사의 양해 하에 해당 건물 엘리베이터 옆 공간에 배달되도록 한 후 해당 물건들을 사용하거나 가족에 나눠줬다고 주장하지만, 이를 인정할 객관적 증거는 없다”면서 “위와 같은 여러차례 메시지 내용을 비춰 보면 이를 리베이트 행위로 보지 않는 것이 오히려 상식이나 경험칙에 반하는 것” 이라고 밝혔다. 이번 재판에서 처분을 내린 식약처와 대전식약처가 재량권을 일탈, 남용한 것이라고는 회사 측 주장도 받아들여지지 않았다. 리베이트 액수 합계가 50여만원에 불과한데 비해 3개월 판매업무정지, 2700여만원의 과징금 부과 처분이 내려진 것은 지나치게 과중하다는 이유에서다. 회사 측은 “300만원 미만의 리베이트 행위에 대해 식약처에서 경고 처분을 내린 선례가 있다”며 “이번 사건의 경우 리베이트 액수가 50여만원에 불과함에도 이 사건 각 처분을 한 것은 재량권을 일탈·남용한 것”이라고 주장했다. 이에 대해 법원은 “리베이트 행위는 그 제공 액수에 불문하고 반드시 근절돼야 하고 그 액수에 많고 적음이 행정처분의 재량권 일탈·남용 여부에 결정적 영향을 미친다 할 수 없다”며 “영업사원인 B의 행위는 의약품 등의 판촉을 위한 것이라고 볼 수 밖에 없고, 이는 종국에 의약품 제조, 판매업을 목적으로 하는 회사에 책임이 귀속돼야 한다”고 강조했다. 이어 “이 사건 각 처분은 제재적 행정처분 기준에 따른 것이고, 그 기준은 그 자체로 헌법 또는 법률에 비춰 현저히 부당하다고 볼 수 없어 재량권 일탈·남용의 위법이 있다고 할 수 없다. 원고의 청구는 모두 이유 없어 기각한다”고 판시했다.2026-01-14 12:02:22김지은 기자
생필품 배달원된 MR...판결문에 드러난 리베이트 백태[데일리팜=김지은 기자] 의약품 리베이트의 액수가 소액이라 하더라도 제재를 피할 수는 없다는 법원의 판단이 나왔다. 영업사원의 개인적 일탈에 불과하다는 제약사의 주장에도 법원은 의약품 판촉을 목적으로 한 리베이트 행위의 책임은 결국 회사에 귀속된다고 못 박았다. 서울행정법원은 최근 A제약사가 식품의약품안전처장과 대전지방식품의약품안전청장을 상대로 제기한 의약품 판매업무정지처분 등 취소 청구 소송을 모두 기각했다. 이 회사는 지난 2023년 식약처가 자사 특정 의약품에 대한 3개월의 판매업무정지처분을, 대전식약청이 같은 기간 특정 의약품들에 대한 3개월의 판매업무정지, 해당 의약품들에 대한 2700여만원의 과징금 부과 처분이 내려진데 대해 반발해 이번 소송을 제기했다. 이번 사건은 A제약사의 영업사원인 B과장이 의약품 채택·처방유도 등 판매촉진을 목적으로 지난 2016년 5월부터 9월까지 4회에 걸쳐 서울의 한 내과의원에 10만원 내지 20만원 상당 물품으로 경제적 이익을 제공한 것이 발각되면서 불거졌다. 당시 육아휴직 중이었던 B과장은 병원 간호사 등 직원으로부터 병원에 필요한 생필품 등의 내역을 문자메시지로 전송받으면 자신의 하급자인 C영업사원에게 관련 내용을 전송한 후 구매해 병원에 배송할 수 있도록 한 것으로 확인됐다. 법정에서는 B과장이 물품을 제공한 내과 간호사로부터 전송된 생필품 내역 등이 기재된 문자메시지가 리베이트 증거 자료로 공개되기도 했다. 이번 소송에서 A회사 측은 사건의 의료기관이 리베이트 관련 수사를 받거나 행정처분을 받지 않은 만큼, 회사와 해당 의료기관 간 리베이트를 주고 받은 사실이 인정되지 않는다고 주장했다. 오히려 직원인 B과장이 육아휴직 중 인센티브에 갈음해 개인적 용도로 법인카드를 유용한 것에 불과할 뿐이며, 설령 리베이트 행위를 했다 하더라도 B과장의 개인적 일탈 행위에 불과하다고도 항변했다. 이 같은 회사 측 주장을 법원은 인정하지 않았다. 정황으로 볼 때 리베이트가 분명하며, 특정 의약품 판촉을 위한 리베이트의 책임은 곧 회사에 있음을 분명히 했다. 재판부는 “B가 육아휴직 중임에도 하급자인 C에게 4개월이라는 단기간 내 여러차례 걸쳐, 또 구체적 지시를 한점, 이 사건 의료기관이 요구한 각 물품 모두 병원에서 사용하는 물건으로 볼 수 있는 점 등을 보면 B의 개인적 일탈행위에 불과하다고 볼 수 없다”고 지적했다. 이어 “회사 법인카드로 B가 특정 마트에서 물건들을 구입해 사건 의료기관 간호사의 양해 하에 해당 건물 엘리베이터 옆 공간에 배달되도록 한 후 해당 물건들을 사용하거나 가족에 나눠줬다고 주장하지만, 이를 인정할 객관적 증거는 없다”면서 “위와 같은 여러차례 메시지 내용을 비춰 보면 이를 리베이트 행위로 보지 않는 것이 오히려 상식이나 경험칙에 반하는 것” 이라고 밝혔다. 이번 재판에서 처분을 내린 식약처와 대전식약처가 재량권을 일탈, 남용한 것이라고는 회사 측 주장도 받아들여지지 않았다. 리베이트 액수 합계가 50여만원에 불과한데 비해 3개월 판매업무정지, 2700여만원의 과징금 부과 처분이 내려진 것은 지나치게 과중하다는 이유에서다. 회사 측은 “300만원 미만의 리베이트 행위에 대해 식약처에서 경고 처분을 내린 선례가 있다”며 “이번 사건의 경우 리베이트 액수가 50여만원에 불과함에도 이 사건 각 처분을 한 것은 재량권을 일탈·남용한 것”이라고 주장했다. 이에 대해 법원은 “리베이트 행위는 그 제공 액수에 불문하고 반드시 근절돼야 하고 그 액수에 많고 적음이 행정처분의 재량권 일탈·남용 여부에 결정적 영향을 미친다 할 수 없다”며 “영업사원인 B의 행위는 의약품 등의 판촉을 위한 것이라고 볼 수 밖에 없고, 이는 종국에 의약품 제조, 판매업을 목적으로 하는 회사에 책임이 귀속돼야 한다”고 강조했다. 이어 “이 사건 각 처분은 제재적 행정처분 기준에 따른 것이고, 그 기준은 그 자체로 헌법 또는 법률에 비춰 현저히 부당하다고 볼 수 없어 재량권 일탈·남용의 위법이 있다고 할 수 없다. 원고의 청구는 모두 이유 없어 기각한다”고 판시했다.2026-01-14 12:02:22김지은 기자 -
 올해 급여재평가 성분 공개 임박...선정 기준도 변화[데일리팜=정흥준 기자]올해 급여재평가 성분 공개가 기존에 언급됐던 7개 성분에서 소폭 변동될 전망이다. 재평가 선정 기준 변경에 따른 영향이다. 14일 업계 관계자에 따르면 내일 약제급여평가위원회에서 2026년 급여재평가 관련 안건이 상정될 예정이다. 또 재평가 선정 기준에 대해 논의가 이뤄질 것으로 보인다. 앞으로 등재 국가수와 청구금액 규모 등의 기준은 사라지고 임상적 유용성에 대한 재평가가 필요한 성분은 대상이 될 전망이다. 정부는 작년 11월 약가제도 개편안을 발표하면서 ▲A8 국가 보건당국에서 임상 또는 급여 적정성 재평가 착수한 성분 ▲기존에 보고된 약효와 상충되는 데이터·임상 근거가 발표된 경우 ▲학회 및 전문가로부터 재평가 필요성 건의된 약제로 기준 개편을 예고한 바 있다. 기존처럼 등재국이나 청구 규모로 분류하지 않고 임상적 유용성 재검토가 필요하다고 판단되는 성분은 재평가 대상으로 지정한다는 의미다. 심평원은 기관, 학회 등의 의견을 청취하고 나아가 청구 경향 변화 등의 모니터링 역할을 더 강화할 것으로 보인다. 만약 이대로 약평위와 건정심을 거쳐 급여재평가 기준이 개정되고 나면, 성분 지정 검토를 위한 전문가자문위 등 추가적인 절차 마련도 예상된다. 또 급여재평가 결과는 급여제외 또는 선별급여로 간략화된다. 즉, 제약사의 자진 약가인하 등으로 급여를 유지하는 돌파구는 사라진다는 뜻이다. 급여 적정성을 증명하지 못하면 보험에서 퇴출되거나 환자부담금 변동 중 하나로 이어질 전망이다. 작년 건정심 소위원회에서 올해 재평가 대상으로 논의된 성분은 은행엽건조엑스, 도베실산칼슘수화물, 칼리디노게나제, 메글루민가도테레이트, 디아세레인, 아플로쿠알론, 옥틸로늄브롬화물로 총 7개다. 급여재평가 기준이 변경되기 때문에 기존 기준으로 추려졌던 7개 성분에서 일부 변동이 예상된다. 한편, 이번 약평위는 10기 위원 교체 후 첫 회의다. 삼성서울병원 최승혁, 서울성모병원 김성환, 송세현 경성대 약대 교수, 김현아 숙명여대 약대 교수 등의 위원들이 신규로 합류하며 74명으로 출범했다.2026-01-14 06:00:50정흥준 기자
올해 급여재평가 성분 공개 임박...선정 기준도 변화[데일리팜=정흥준 기자]올해 급여재평가 성분 공개가 기존에 언급됐던 7개 성분에서 소폭 변동될 전망이다. 재평가 선정 기준 변경에 따른 영향이다. 14일 업계 관계자에 따르면 내일 약제급여평가위원회에서 2026년 급여재평가 관련 안건이 상정될 예정이다. 또 재평가 선정 기준에 대해 논의가 이뤄질 것으로 보인다. 앞으로 등재 국가수와 청구금액 규모 등의 기준은 사라지고 임상적 유용성에 대한 재평가가 필요한 성분은 대상이 될 전망이다. 정부는 작년 11월 약가제도 개편안을 발표하면서 ▲A8 국가 보건당국에서 임상 또는 급여 적정성 재평가 착수한 성분 ▲기존에 보고된 약효와 상충되는 데이터·임상 근거가 발표된 경우 ▲학회 및 전문가로부터 재평가 필요성 건의된 약제로 기준 개편을 예고한 바 있다. 기존처럼 등재국이나 청구 규모로 분류하지 않고 임상적 유용성 재검토가 필요하다고 판단되는 성분은 재평가 대상으로 지정한다는 의미다. 심평원은 기관, 학회 등의 의견을 청취하고 나아가 청구 경향 변화 등의 모니터링 역할을 더 강화할 것으로 보인다. 만약 이대로 약평위와 건정심을 거쳐 급여재평가 기준이 개정되고 나면, 성분 지정 검토를 위한 전문가자문위 등 추가적인 절차 마련도 예상된다. 또 급여재평가 결과는 급여제외 또는 선별급여로 간략화된다. 즉, 제약사의 자진 약가인하 등으로 급여를 유지하는 돌파구는 사라진다는 뜻이다. 급여 적정성을 증명하지 못하면 보험에서 퇴출되거나 환자부담금 변동 중 하나로 이어질 전망이다. 작년 건정심 소위원회에서 올해 재평가 대상으로 논의된 성분은 은행엽건조엑스, 도베실산칼슘수화물, 칼리디노게나제, 메글루민가도테레이트, 디아세레인, 아플로쿠알론, 옥틸로늄브롬화물로 총 7개다. 급여재평가 기준이 변경되기 때문에 기존 기준으로 추려졌던 7개 성분에서 일부 변동이 예상된다. 한편, 이번 약평위는 10기 위원 교체 후 첫 회의다. 삼성서울병원 최승혁, 서울성모병원 김성환, 송세현 경성대 약대 교수, 김현아 숙명여대 약대 교수 등의 위원들이 신규로 합류하며 74명으로 출범했다.2026-01-14 06:00:50정흥준 기자 -
 예상청구액 2300억 키트루다 급여 확대...건보재정 경고등[데일리팜=정흥준 기자]면역항암제 키트루다(펨브롤리주맙)가 2384억이라는 역대 최대 규모 예상청구액으로 이달 급여확대가 이뤄지면서 보장성은 강화됐지만, 건강보험재정 관리 측면에서는 경고등이 들어왔다. 작년 말 복지부는 약가제도 개편에 따라 약 1조원의 재정이 절감될 것이라는 추산치를 발표한 바 있다. 증감액으로만 놓고 보자면 단일 약제의 청구액 확대가 기등재 제네릭 약가인하에 따른 재정 절감액의 20~25%를 차지하는 셈이다. 키트루다뿐만 아니라 다적응증 블록버스터 약제가 많아짐에 따라 사후관리 강화 필요성이 제기되는 이유다. 13일 업계에 따르면 한국MSD의 면역항암제 키트루다의 예상청구액은 역대 최대 규모다. 2200억대를 기록했던 팍스로비드를 웃도는 금액이다. 그만큼 건보재정에 미치는 영향이 클 것이라는 뜻이다. 키트루다는 그동안 비소세포폐암 등 4개 암종에서 보험이 적용됐지만, 올해부터 두경부암 등 9개 암종 17개 요법에서 추가로 보험 적용된다. 확대되는 보험 환자 수는 3258명에서 점차 증가해 6680명까지 늘어날 것으로 예상하고 있다. 이에 따라 예상청구액은 첫 해 1788억원에서 점차 증가해 2384억까지 증가할 것으로 보고 있다. 지난 2022년 키트루다는 비소세포폐암 1차 치료 등으로 급여 확대를 성공했는데, 당시 복지부는 1762억원의 예상청구액을 추산한 바 있다. 이후 단일약제로 연 4000억대 매출을 기록하고 있는 키트루다가 잇따라 급여확대 문턱을 넘으며 몸집을 키워가는 중이다. 비소세포폐암에 집중됐던 보장성이 여성암을 비롯해 다양한 암종에서 보장된다는 건 대상 환자 입장에서는 희소식이다. 다만, 재정 관리 부담은 그만큼 커질 수밖에 없다. 건보공단도 재정 영향을 고려해 사후 모니터링를 강화한다는 입장이다. 점차 유사 사례들이 늘어날 것으로 예상되는 상황에서 사후관리 강화 방안에 대해서도 고민 중이다. 공단 관계자는 “(급여확대 신약은)사용량 약가연동으로 사후관리를 하고 있다. 공단 외 다른 기관에서도 재정 영향에 대한 관리 방안을 가지고 있겠지만, 공단에서도 추가적인 사후관리 방안 마련에 대해서도 고민 중이다”라고 밝혔다.2026-01-13 06:00:50정흥준 기자
예상청구액 2300억 키트루다 급여 확대...건보재정 경고등[데일리팜=정흥준 기자]면역항암제 키트루다(펨브롤리주맙)가 2384억이라는 역대 최대 규모 예상청구액으로 이달 급여확대가 이뤄지면서 보장성은 강화됐지만, 건강보험재정 관리 측면에서는 경고등이 들어왔다. 작년 말 복지부는 약가제도 개편에 따라 약 1조원의 재정이 절감될 것이라는 추산치를 발표한 바 있다. 증감액으로만 놓고 보자면 단일 약제의 청구액 확대가 기등재 제네릭 약가인하에 따른 재정 절감액의 20~25%를 차지하는 셈이다. 키트루다뿐만 아니라 다적응증 블록버스터 약제가 많아짐에 따라 사후관리 강화 필요성이 제기되는 이유다. 13일 업계에 따르면 한국MSD의 면역항암제 키트루다의 예상청구액은 역대 최대 규모다. 2200억대를 기록했던 팍스로비드를 웃도는 금액이다. 그만큼 건보재정에 미치는 영향이 클 것이라는 뜻이다. 키트루다는 그동안 비소세포폐암 등 4개 암종에서 보험이 적용됐지만, 올해부터 두경부암 등 9개 암종 17개 요법에서 추가로 보험 적용된다. 확대되는 보험 환자 수는 3258명에서 점차 증가해 6680명까지 늘어날 것으로 예상하고 있다. 이에 따라 예상청구액은 첫 해 1788억원에서 점차 증가해 2384억까지 증가할 것으로 보고 있다. 지난 2022년 키트루다는 비소세포폐암 1차 치료 등으로 급여 확대를 성공했는데, 당시 복지부는 1762억원의 예상청구액을 추산한 바 있다. 이후 단일약제로 연 4000억대 매출을 기록하고 있는 키트루다가 잇따라 급여확대 문턱을 넘으며 몸집을 키워가는 중이다. 비소세포폐암에 집중됐던 보장성이 여성암을 비롯해 다양한 암종에서 보장된다는 건 대상 환자 입장에서는 희소식이다. 다만, 재정 관리 부담은 그만큼 커질 수밖에 없다. 건보공단도 재정 영향을 고려해 사후 모니터링를 강화한다는 입장이다. 점차 유사 사례들이 늘어날 것으로 예상되는 상황에서 사후관리 강화 방안에 대해서도 고민 중이다. 공단 관계자는 “(급여확대 신약은)사용량 약가연동으로 사후관리를 하고 있다. 공단 외 다른 기관에서도 재정 영향에 대한 관리 방안을 가지고 있겠지만, 공단에서도 추가적인 사후관리 방안 마련에 대해서도 고민 중이다”라고 밝혔다.2026-01-13 06:00:50정흥준 기자 -
 심평원, 마약류DUR 연착륙·비대면진료 본사업 전환 채비[데일리팜=이정환 기자]건강보험심사평가원이 지난해 국회 통과로 정부 공포된 '마약류 DUR(의약품안전사용서비스) 의무화' 연착륙을 위해 올해 1분기 관련 약사법 개정을 지원하고 2분기엔 시행령 등 하위법령 개정에 나선다. 비대면진료 제도화 의료법이 올해 12월 24일 시행을 앞둔 만큼 시범사업 모형을 개선하고 세부 기준도 마련한다. 대상환자, 지역 제한, 처방 제한 등 입법안을 토대로 현행 시범사업의 본사업 전환 때 수가 기준을 신설하고 청구·심사 연계방향 개편 등을 추진한다. 약가제도의 경우 혁신형 제약기업이 개발한 신약과 식품의약품안전처 신속심사(GIFT) 허가, 국내 임상시험 수행 조건을 모두 충족한 의약품에 대해 약가 우대를 적용한다. 12일 보건복지부는 심평원으로부터 소관 공공기관 업무보고를 받았다. 마약류 DUR 의무화…"본회의 미상정 약사법 통과 지원" 심평원은 환자의 보다 안전한 의료환경 구축을 위해 DUR 의무화 법 개정을 적극 추진했다. 이에 마약류 처방 의사의 DUR 확인 의무화 법안이 국회를 통과해 정부 공포됐다. 다만 약사법 개정안의 본회의 상정 보류로 약사 마약류 DUR 의무화는 국회 통과와 정부 공포가 지연되고 있다는 게 심평원 설명이다. 심평원은 과태료 부과기준 등 하위법령을 정비하고 필요사항을 검토해 오는 12월 시행될 마약류 DUR 의무화 시행을 준비한다. 이를 위해 올해 1분기 약사법 개정안 국회 통과를 지원하고 2분기엔 시행령 등 하위법령 개정에 나선다. 올해 12월엔 처방 면허번호, 환자정보 등 마약류 통합정보를 연계한다. 나아가 심평원은 전체 의약품 DUR 의무화로 의약품 안전 사용 선순환 구조를 구축할 방침이다. 의료AI·제약·바이오헬스 강국 실현…"혁신 신약 약가우대 지속" 혁신적 제약 육성을 위한 건강보험 약제 등재 제도를 개선한다. 혁신형 제약사가 만든 신약과 식약처 GIFT 허가, 국내 임상시험 수행을 모두 만족한 약은 약가를 우대한다. 임상적 유용성, 즉 약효가 대체약과 유사한 경우 앞으로는 우대를 통해 '대체약제 최고가'와 '대체약제 가중평균가에 53.55%를 적용한 가격' 중 낮은 금액을 적용한다. 신약은 '혁신성' 평가 요소를 신설하고 혁신성 인정 땐 경제성평가 임계값(ICER값)을 유연 적용해 평가한다. 비대면진료 확대 제도 지원…"본사업 전환 채비" 심평원은 비대면진료 제도화 의료법이 지난해 12월 정부 공포, 올해 12월 시행이 결정되면서 본사업 전환을 추진하고 세부 규정 마련 지원이 필요하다고 밝혔다. 비대면진료 법안 취지에 맞춰 시범사업 내용을 개선하고 관련 법안 시행·적용에 대비해 비대면진료 수가·기준 개발을 지속한다. 비대면진료 제도화 내용을 반영해 시범사업 모형 개선을 검토하고 본 사업 전환 때 수가·기준 신설, 청구·심사 연계방향 개편을 추진한다. 의약품 처방제한 사항, EMR 시스템 반영을 위한 API 개발 등 관련 시스템을 오는 12월까지 구축한다. 비급여 관리 체계 도입·운영 심평원은 시장 자율영역으로 간주돼 가격·진료기준·적정사용 등 관리가 미흡한 비급여 진료의 과잉 팽창과 과도한 보상을 관리하기 위한 체계도 만든다. 총 5개 항목을 관리급여로 검토해 도수치료, 경피적 경막외강, 신경성형술, 방사선 온열치료·온열치료계획을 선정한다. 심평원은 선별급여 지정 및 실시 등에 관한 기준 고시를 개정해 관리급여 별도 평가기준 신설·운영 규정을 마련한다. 관리급여 항목은 3개 대상항목별 수가·급여기준 등을 검토하고 관련 위원회 평가·심의를 거쳐 올해 상반기 내 급여로 전환한다.2026-01-12 16:02:05이정환 기자
심평원, 마약류DUR 연착륙·비대면진료 본사업 전환 채비[데일리팜=이정환 기자]건강보험심사평가원이 지난해 국회 통과로 정부 공포된 '마약류 DUR(의약품안전사용서비스) 의무화' 연착륙을 위해 올해 1분기 관련 약사법 개정을 지원하고 2분기엔 시행령 등 하위법령 개정에 나선다. 비대면진료 제도화 의료법이 올해 12월 24일 시행을 앞둔 만큼 시범사업 모형을 개선하고 세부 기준도 마련한다. 대상환자, 지역 제한, 처방 제한 등 입법안을 토대로 현행 시범사업의 본사업 전환 때 수가 기준을 신설하고 청구·심사 연계방향 개편 등을 추진한다. 약가제도의 경우 혁신형 제약기업이 개발한 신약과 식품의약품안전처 신속심사(GIFT) 허가, 국내 임상시험 수행 조건을 모두 충족한 의약품에 대해 약가 우대를 적용한다. 12일 보건복지부는 심평원으로부터 소관 공공기관 업무보고를 받았다. 마약류 DUR 의무화…"본회의 미상정 약사법 통과 지원" 심평원은 환자의 보다 안전한 의료환경 구축을 위해 DUR 의무화 법 개정을 적극 추진했다. 이에 마약류 처방 의사의 DUR 확인 의무화 법안이 국회를 통과해 정부 공포됐다. 다만 약사법 개정안의 본회의 상정 보류로 약사 마약류 DUR 의무화는 국회 통과와 정부 공포가 지연되고 있다는 게 심평원 설명이다. 심평원은 과태료 부과기준 등 하위법령을 정비하고 필요사항을 검토해 오는 12월 시행될 마약류 DUR 의무화 시행을 준비한다. 이를 위해 올해 1분기 약사법 개정안 국회 통과를 지원하고 2분기엔 시행령 등 하위법령 개정에 나선다. 올해 12월엔 처방 면허번호, 환자정보 등 마약류 통합정보를 연계한다. 나아가 심평원은 전체 의약품 DUR 의무화로 의약품 안전 사용 선순환 구조를 구축할 방침이다. 의료AI·제약·바이오헬스 강국 실현…"혁신 신약 약가우대 지속" 혁신적 제약 육성을 위한 건강보험 약제 등재 제도를 개선한다. 혁신형 제약사가 만든 신약과 식약처 GIFT 허가, 국내 임상시험 수행을 모두 만족한 약은 약가를 우대한다. 임상적 유용성, 즉 약효가 대체약과 유사한 경우 앞으로는 우대를 통해 '대체약제 최고가'와 '대체약제 가중평균가에 53.55%를 적용한 가격' 중 낮은 금액을 적용한다. 신약은 '혁신성' 평가 요소를 신설하고 혁신성 인정 땐 경제성평가 임계값(ICER값)을 유연 적용해 평가한다. 비대면진료 확대 제도 지원…"본사업 전환 채비" 심평원은 비대면진료 제도화 의료법이 지난해 12월 정부 공포, 올해 12월 시행이 결정되면서 본사업 전환을 추진하고 세부 규정 마련 지원이 필요하다고 밝혔다. 비대면진료 법안 취지에 맞춰 시범사업 내용을 개선하고 관련 법안 시행·적용에 대비해 비대면진료 수가·기준 개발을 지속한다. 비대면진료 제도화 내용을 반영해 시범사업 모형 개선을 검토하고 본 사업 전환 때 수가·기준 신설, 청구·심사 연계방향 개편을 추진한다. 의약품 처방제한 사항, EMR 시스템 반영을 위한 API 개발 등 관련 시스템을 오는 12월까지 구축한다. 비급여 관리 체계 도입·운영 심평원은 시장 자율영역으로 간주돼 가격·진료기준·적정사용 등 관리가 미흡한 비급여 진료의 과잉 팽창과 과도한 보상을 관리하기 위한 체계도 만든다. 총 5개 항목을 관리급여로 검토해 도수치료, 경피적 경막외강, 신경성형술, 방사선 온열치료·온열치료계획을 선정한다. 심평원은 선별급여 지정 및 실시 등에 관한 기준 고시를 개정해 관리급여 별도 평가기준 신설·운영 규정을 마련한다. 관리급여 항목은 3개 대상항목별 수가·급여기준 등을 검토하고 관련 위원회 평가·심의를 거쳐 올해 상반기 내 급여로 전환한다.2026-01-12 16:02:05이정환 기자 -
 데이터 변환 10분내 뚝딱…PIT3000→PM+20 전환 속도전[데일리팜=강혜경 기자] 약학정보원(원장 유상준, 이하 약정원)이 오는 6월 약국 청구소프트웨어(SW) PIT3000 운영 종료를 앞두고 PM+20으로의 전환에 속도를 낼 전망이다. 운영 종료를 5개월 가량 앞두고 본격적인 속도전에 돌입하는 것이다. 약정원은 5~6월에 청구SW 전환이 집중되는 것을 사전에 막기 위해 순차적으로 청구SW 전환을 추진하는데, 가칭 '변환 선도 분회'를 선정해 우선 전환에 나선다는 계획이다. 개별 약국 차원의 접근에 앞서 권역별 단위인 분회를 통해 우선 전환을 하겠다는 의중으로 읽힌다. 유상준 약학정보원장이 회원으로 속해 있는 서울 강동구약사회는 선도 반회를 자처해 약정원과의 협업에 나선다는 방침이다. 10일 강동구약사회 정기총회에서 이조미 부회장은 "PIT3000 운영 종료가 예고된 6월에 전환 신청이 몰릴 것을 대비하기 위해 미리 순차적으로 변경을 하고자 한다. 이미 PM+20이 완성 단계로, 전환 가능한 상황"이라며 "약정원과 협의해 시범적으로 전환할 수 있도록 할 방침"이라고 말했다. 전체 청구SW 점유율의 절반 가량인 1만 여곳의 6월 전환이 집중되는 경우 업무 차질 등이 빚어질 수 있는 부분을 고려해, 회원 약국을 대상으로 사용 청구프로그램은 물론 연계 A/S업체 등에 대해 설문조사를 실시, 우선 전환해 나간다는 설명이다. 현재 전국 단위 사용 약국 중 전환에 참여한 약국은 약 200여곳 수준인 것으로 알려졌다. 유상준 약학정보원장은 제반 설명을 통해 "누적됐던 오류들이 상당부분 개선됐다. 특히 데이터 변환 속도가 매우 빨라졌다"며 "과거 1~2시간에서 현재는 10분 내로 시간이 줄어들었다"고 밝혔다. IT를 잘 사용하는 약국에서는 프로그램 전환 이후 ATC, 바코드, 봉투 등도 바로 사용할 수 있도록 세팅을 하고 있다는 것. 유 원장은 "문제가 있으면 약정원 차원에서 밀착 마크해 해결할 수 있도록 도움을 드릴 계획"이라며 "큰 걱정 없이 프로그램을 전환할 수 있도록 노력하겠다"고 말했다.2026-01-12 12:00:31강혜경 기자
데이터 변환 10분내 뚝딱…PIT3000→PM+20 전환 속도전[데일리팜=강혜경 기자] 약학정보원(원장 유상준, 이하 약정원)이 오는 6월 약국 청구소프트웨어(SW) PIT3000 운영 종료를 앞두고 PM+20으로의 전환에 속도를 낼 전망이다. 운영 종료를 5개월 가량 앞두고 본격적인 속도전에 돌입하는 것이다. 약정원은 5~6월에 청구SW 전환이 집중되는 것을 사전에 막기 위해 순차적으로 청구SW 전환을 추진하는데, 가칭 '변환 선도 분회'를 선정해 우선 전환에 나선다는 계획이다. 개별 약국 차원의 접근에 앞서 권역별 단위인 분회를 통해 우선 전환을 하겠다는 의중으로 읽힌다. 유상준 약학정보원장이 회원으로 속해 있는 서울 강동구약사회는 선도 반회를 자처해 약정원과의 협업에 나선다는 방침이다. 10일 강동구약사회 정기총회에서 이조미 부회장은 "PIT3000 운영 종료가 예고된 6월에 전환 신청이 몰릴 것을 대비하기 위해 미리 순차적으로 변경을 하고자 한다. 이미 PM+20이 완성 단계로, 전환 가능한 상황"이라며 "약정원과 협의해 시범적으로 전환할 수 있도록 할 방침"이라고 말했다. 전체 청구SW 점유율의 절반 가량인 1만 여곳의 6월 전환이 집중되는 경우 업무 차질 등이 빚어질 수 있는 부분을 고려해, 회원 약국을 대상으로 사용 청구프로그램은 물론 연계 A/S업체 등에 대해 설문조사를 실시, 우선 전환해 나간다는 설명이다. 현재 전국 단위 사용 약국 중 전환에 참여한 약국은 약 200여곳 수준인 것으로 알려졌다. 유상준 약학정보원장은 제반 설명을 통해 "누적됐던 오류들이 상당부분 개선됐다. 특히 데이터 변환 속도가 매우 빨라졌다"며 "과거 1~2시간에서 현재는 10분 내로 시간이 줄어들었다"고 밝혔다. IT를 잘 사용하는 약국에서는 프로그램 전환 이후 ATC, 바코드, 봉투 등도 바로 사용할 수 있도록 세팅을 하고 있다는 것. 유 원장은 "문제가 있으면 약정원 차원에서 밀착 마크해 해결할 수 있도록 도움을 드릴 계획"이라며 "큰 걱정 없이 프로그램을 전환할 수 있도록 노력하겠다"고 말했다.2026-01-12 12:00:31강혜경 기자 -
 카나프·리센스 IPO 시동…헬스케어기업, 릴레이 상장 도전[데일리팜=차지현 기자] 올해에도 바이오·헬스케어 기업의 기업공개(IPO) 도전 열기가 이어질 전망이다. 의료기기·디지털 헬스케어 기업부터 신약개발 바이오텍까지 다양한 분야 기업이 상장 채비에 나서면서 시장의 관심도 높아지는 분위기다. 12일 금융감독원에 따르면 의료기기 기업 리센스메디컬은 9일 IPO를 위한 증권신고서를 제출했다. 한국거래소로부터 코스닥 상장을 위한 예비심사 승인을 받은 지 7영업일 만이다. 리센스메디컬은 지난달 29일 상장 예비심사 승인을 획득한 바 있다. 리센스메디컬은 정밀 냉각 기술을 상업화한 의료기기 기업이다. 극저온 냉매 제어 기술을 기반으로 다양한 의료 분야에 냉각 솔루션을 공급 중이다. 의료용 저온기, 냉동 수술기(TargetCool), 안구 냉각 마취기기(OcuCool), 분사식 주사기(TargetCool+), 동물 전용 냉각 의료기기 (VetEase) 등을 주요 제품으로 뒀다. 지난해 매출 63억원을 기록했다. 이 회사는 공모 주식 140만주를 포함해 총 1085만298주를 상장할 예정이다. 희망 공모가액은 9000~1만1000원으로 책정했다. 이에 기반한 예상 공모금액은 약 126억~154억원이다. 상장 후 시가총액은 약 2100억~2600억원 수준이다. 상장 주관사는 KB증권과 한국투자증권이다. 이에 앞서 신약개발 바이오텍 카나프테라퓨틱스도 지난 5일 IPO 증권신고서를 제출했다. 카나프테라퓨틱스는 거래소 코스닥 상장 예비심사를 통과한 지 10영업일 만에 신고서를 제출했다. 앞서 회사는 지난해 8월 거래소 전문 평가기관 두 곳으로부터 각각 A·BBB 등급을 획득, 기술특례상장을 위한 기술성 평가를 통과한 바 있다. 카나프테라퓨틱스는 2019년 2월 설립된 바이오 기업이다. 인간 유전체 기반 약물 개발 플랫폼을 활용해 항암제를 개발하고 있다. 특히 종양 미세환경(TME)을 표적하는 혁신적 기전과 면역 활성 조절 기술을 기반으로 한 면역항암제와 자체 항체약물접합체(ADC) 기술을 활용한 ADC 치료제 등 파이프라인을 지속해서 확장 중이다. 이 회사는 지난 2023년 230억원 규모 시리즈C 투자를 포함해 약 581억원의 누적 투자금을 확보했다. 또 카나프테라퓨틱스는 롯데바이오로직스, GC녹십자, 오스코텍, 동아에스티, 유한양행 등 국내 유수 기업과 공동 연구개발과 기술이전 계약을 체결했다. 이를 기반으로 지난 2024년 43억원의 매출을 올렸다. 카나프테라퓨틱스는 이번 IPO를 통해 총 200만주를 공모할 계획이다. 희망 공모가는 1만6000~2만원으로 이를 기준으로 한 예상 공모금액은 320억~400억원, 상장 후 시가총액은 약 2100억~2600억원 수준이다. 공모를 통해 조달된 자금은 기존 파이프라인 임상 진행, 신규 파이프라인 확대, 연구개발(R&D) 강화 등에 활용할 예정이다. 나노의약품 개발 전문 기업 인벤테라와 이동형 원격 환자 모니터링(aRPM) 기업 메쥬 등도 상장 출격을 대기 중이다. 인벤테라와 메쥬는 각각 지난달 24일과 18일 코스닥 상장을 위한 예비심사를 통과했다. 인벤테라는 나노-MRI 조영제를 기반으로 근골격계·림프계·췌담관 질환 타깃 신약 파이프라인을 개발 중인 업체다. 현재 인벤테라는 리드 파이프라인인 근골격계 나노-MRI 조영제 'INV-002' 국내 임상 3상을 진행 중이다. 올 초까지 3상 투약을 마무리한 뒤 품목허가 신청을 추진할 계획이다. 메쥬도는 aRPM 기술을 앞세운 의료기기 업체다. 생체계측과 인공지능(AI) 기반 생체신호 처리 기술을 바탕으로 제품 설계부터 생산까지 자체 수행하는 기술력을 보유했다. 국내 최초로 이동형 원격 환자 모니터링 상용 레퍼런스를 구축해 의료 현장 중심의 실사용 경험을 축적해 왔다. 상급종합병원을 포함한 전국 600여개 병·의원에 aRPM 솔루션 '하이카디'(HiCardi)를 공급 중이다. 예비심사 청구서를 제출하고 심사 결과를 기다리는 곳도 있다. 아이엠바이오로직스, 유빅스테라퓨틱스, 레몬헬스케어, 넥스트젠바이오 등이 해당한다. 아이엠바이오로직스는 2020년 HK이노엔(전 CJ헬스케어) 바이오부문장 출신 하경식 대표가 창업한 항체 기반 신약개발 바이오 기업으로 지난해 10월 거래소에 코스닥시장 상장 예심 청구서를 제출했다. 앞서 회사는 지난 8월 거래소 지정 전문 평가기관으로부터 각각 A 등급을 획득, 기술특례 상장을 위한 기술성 평가를 통과, 기술특례 상장을 위한 기본 요건을 갖췄다. 이 회사는 창업 4년 만에 1조원대 기술수출 계약을 체결했다. 아이엠바이오로직스는 2024년 6월 자가면역질환 이중항체 신약 후보물질 'IMB-101'을 미국 네비게이터 메디신에 1조3000억원 규모로 기술수출했다. 이어 2개월 뒤 IMB-101에 대해 중국 화동제약과 4309억원 규모 계약을 맺으며 연이은 기술수출 성과를 거뒀다. 해당 계약은 아이엠바이오로직스가 개발을 주도하고 HK이노엔과 와이바이오로직스가 각각 핵심 기술을 제공한 3자 공동개발 구조로 체결됐다. 유빅스테라퓨틱스도 지난해 11월 예비심사 청구서를 접수하며 IPO 절차에 착수했다. 이 회사는 표적 단백질 분해제(TPD) 플랫폼을 기반으로 신약을 개발하는 바이오텍이다. 자체 TPD 플랫폼 '디그래듀서'(Degraducer)를 앞세워 항암·면역질환 파이프라인을 구축해 왔다. 지난해 거래소 지정 전문평가기관 이크레더블과 한국평가데이터에서 각각 A·A등급을 획득, 코스닥 상장을 위한 기술성평가 심사를 통과했다. 레몬헬스케어는 코스닥 입성에 재도전한다. 이 회사는 지난해 11월 예비심사 청구서를 제출했다. 2021년 코스닥 상장 예비심사를 자진 철회하며 고배를 마신 뒤 두 번째 도전에 나섰다. 레몬헬스케어는 이번 상장을 통해 공모 주식 200만주를 포함해 총 1335만1559주를 상장할 예정이다. 상장 주관사는 KB증권이다. 레몬헬스케어는 2017년 IT 컨설팅 기업 데이타뱅크시스템즈에서 인적 분할돼 설립된 디지털 헬스케어 기업이다. 모바일 기반 실손보험 청구 앱 '청구의 신'을 중심으로 병원 예약·결제·보험 청구를 통합한 '레몬케어', 알림톡 기반 병원 안내 서비스 '레몬톡톡' 등 의료 마이데이터 서비스를 운영하고 있다. 작년 매출은 149억원으로 집계됐다. 자가면역질환과 섬유증 치료제 개발에 주력하는 넥스트젠바이오도 지난달 상장예비심사 신청서를 접수하면서 코스닥 상장 절차에 들어갔다. 이 회사는 자가면역질환 치료제 후보물질 'NXC736', 특발성폐섬유증 치료제 후보물질 'NXC680' 등을 보유했다. 이 회사는 공모 주식 110만주를 포함해 총 1071만6533주를 상장할 예정이다. 다만 금융당국의 상장 문턱이 한층 높아지고 있는 점은 부담 요소로 거론된다. 금융당국은 지난해 초 기관투자자 의무보유 확약 확대와 상장폐지 요건 강화를 골자로 한 IPO 제도 개편안을 내놓은 이후 상장 심사 전반에 걸쳐 보다 엄격한 기준을 적용하고 있다. 특히 기술성평가 과정에서 기술력과 함께 사업성·시장성을 동시에 요구하는 기조가 뚜렷해진 분위기다.2026-01-12 12:00:19차지현 기자
카나프·리센스 IPO 시동…헬스케어기업, 릴레이 상장 도전[데일리팜=차지현 기자] 올해에도 바이오·헬스케어 기업의 기업공개(IPO) 도전 열기가 이어질 전망이다. 의료기기·디지털 헬스케어 기업부터 신약개발 바이오텍까지 다양한 분야 기업이 상장 채비에 나서면서 시장의 관심도 높아지는 분위기다. 12일 금융감독원에 따르면 의료기기 기업 리센스메디컬은 9일 IPO를 위한 증권신고서를 제출했다. 한국거래소로부터 코스닥 상장을 위한 예비심사 승인을 받은 지 7영업일 만이다. 리센스메디컬은 지난달 29일 상장 예비심사 승인을 획득한 바 있다. 리센스메디컬은 정밀 냉각 기술을 상업화한 의료기기 기업이다. 극저온 냉매 제어 기술을 기반으로 다양한 의료 분야에 냉각 솔루션을 공급 중이다. 의료용 저온기, 냉동 수술기(TargetCool), 안구 냉각 마취기기(OcuCool), 분사식 주사기(TargetCool+), 동물 전용 냉각 의료기기 (VetEase) 등을 주요 제품으로 뒀다. 지난해 매출 63억원을 기록했다. 이 회사는 공모 주식 140만주를 포함해 총 1085만298주를 상장할 예정이다. 희망 공모가액은 9000~1만1000원으로 책정했다. 이에 기반한 예상 공모금액은 약 126억~154억원이다. 상장 후 시가총액은 약 2100억~2600억원 수준이다. 상장 주관사는 KB증권과 한국투자증권이다. 이에 앞서 신약개발 바이오텍 카나프테라퓨틱스도 지난 5일 IPO 증권신고서를 제출했다. 카나프테라퓨틱스는 거래소 코스닥 상장 예비심사를 통과한 지 10영업일 만에 신고서를 제출했다. 앞서 회사는 지난해 8월 거래소 전문 평가기관 두 곳으로부터 각각 A·BBB 등급을 획득, 기술특례상장을 위한 기술성 평가를 통과한 바 있다. 카나프테라퓨틱스는 2019년 2월 설립된 바이오 기업이다. 인간 유전체 기반 약물 개발 플랫폼을 활용해 항암제를 개발하고 있다. 특히 종양 미세환경(TME)을 표적하는 혁신적 기전과 면역 활성 조절 기술을 기반으로 한 면역항암제와 자체 항체약물접합체(ADC) 기술을 활용한 ADC 치료제 등 파이프라인을 지속해서 확장 중이다. 이 회사는 지난 2023년 230억원 규모 시리즈C 투자를 포함해 약 581억원의 누적 투자금을 확보했다. 또 카나프테라퓨틱스는 롯데바이오로직스, GC녹십자, 오스코텍, 동아에스티, 유한양행 등 국내 유수 기업과 공동 연구개발과 기술이전 계약을 체결했다. 이를 기반으로 지난 2024년 43억원의 매출을 올렸다. 카나프테라퓨틱스는 이번 IPO를 통해 총 200만주를 공모할 계획이다. 희망 공모가는 1만6000~2만원으로 이를 기준으로 한 예상 공모금액은 320억~400억원, 상장 후 시가총액은 약 2100억~2600억원 수준이다. 공모를 통해 조달된 자금은 기존 파이프라인 임상 진행, 신규 파이프라인 확대, 연구개발(R&D) 강화 등에 활용할 예정이다. 나노의약품 개발 전문 기업 인벤테라와 이동형 원격 환자 모니터링(aRPM) 기업 메쥬 등도 상장 출격을 대기 중이다. 인벤테라와 메쥬는 각각 지난달 24일과 18일 코스닥 상장을 위한 예비심사를 통과했다. 인벤테라는 나노-MRI 조영제를 기반으로 근골격계·림프계·췌담관 질환 타깃 신약 파이프라인을 개발 중인 업체다. 현재 인벤테라는 리드 파이프라인인 근골격계 나노-MRI 조영제 'INV-002' 국내 임상 3상을 진행 중이다. 올 초까지 3상 투약을 마무리한 뒤 품목허가 신청을 추진할 계획이다. 메쥬도는 aRPM 기술을 앞세운 의료기기 업체다. 생체계측과 인공지능(AI) 기반 생체신호 처리 기술을 바탕으로 제품 설계부터 생산까지 자체 수행하는 기술력을 보유했다. 국내 최초로 이동형 원격 환자 모니터링 상용 레퍼런스를 구축해 의료 현장 중심의 실사용 경험을 축적해 왔다. 상급종합병원을 포함한 전국 600여개 병·의원에 aRPM 솔루션 '하이카디'(HiCardi)를 공급 중이다. 예비심사 청구서를 제출하고 심사 결과를 기다리는 곳도 있다. 아이엠바이오로직스, 유빅스테라퓨틱스, 레몬헬스케어, 넥스트젠바이오 등이 해당한다. 아이엠바이오로직스는 2020년 HK이노엔(전 CJ헬스케어) 바이오부문장 출신 하경식 대표가 창업한 항체 기반 신약개발 바이오 기업으로 지난해 10월 거래소에 코스닥시장 상장 예심 청구서를 제출했다. 앞서 회사는 지난 8월 거래소 지정 전문 평가기관으로부터 각각 A 등급을 획득, 기술특례 상장을 위한 기술성 평가를 통과, 기술특례 상장을 위한 기본 요건을 갖췄다. 이 회사는 창업 4년 만에 1조원대 기술수출 계약을 체결했다. 아이엠바이오로직스는 2024년 6월 자가면역질환 이중항체 신약 후보물질 'IMB-101'을 미국 네비게이터 메디신에 1조3000억원 규모로 기술수출했다. 이어 2개월 뒤 IMB-101에 대해 중국 화동제약과 4309억원 규모 계약을 맺으며 연이은 기술수출 성과를 거뒀다. 해당 계약은 아이엠바이오로직스가 개발을 주도하고 HK이노엔과 와이바이오로직스가 각각 핵심 기술을 제공한 3자 공동개발 구조로 체결됐다. 유빅스테라퓨틱스도 지난해 11월 예비심사 청구서를 접수하며 IPO 절차에 착수했다. 이 회사는 표적 단백질 분해제(TPD) 플랫폼을 기반으로 신약을 개발하는 바이오텍이다. 자체 TPD 플랫폼 '디그래듀서'(Degraducer)를 앞세워 항암·면역질환 파이프라인을 구축해 왔다. 지난해 거래소 지정 전문평가기관 이크레더블과 한국평가데이터에서 각각 A·A등급을 획득, 코스닥 상장을 위한 기술성평가 심사를 통과했다. 레몬헬스케어는 코스닥 입성에 재도전한다. 이 회사는 지난해 11월 예비심사 청구서를 제출했다. 2021년 코스닥 상장 예비심사를 자진 철회하며 고배를 마신 뒤 두 번째 도전에 나섰다. 레몬헬스케어는 이번 상장을 통해 공모 주식 200만주를 포함해 총 1335만1559주를 상장할 예정이다. 상장 주관사는 KB증권이다. 레몬헬스케어는 2017년 IT 컨설팅 기업 데이타뱅크시스템즈에서 인적 분할돼 설립된 디지털 헬스케어 기업이다. 모바일 기반 실손보험 청구 앱 '청구의 신'을 중심으로 병원 예약·결제·보험 청구를 통합한 '레몬케어', 알림톡 기반 병원 안내 서비스 '레몬톡톡' 등 의료 마이데이터 서비스를 운영하고 있다. 작년 매출은 149억원으로 집계됐다. 자가면역질환과 섬유증 치료제 개발에 주력하는 넥스트젠바이오도 지난달 상장예비심사 신청서를 접수하면서 코스닥 상장 절차에 들어갔다. 이 회사는 자가면역질환 치료제 후보물질 'NXC736', 특발성폐섬유증 치료제 후보물질 'NXC680' 등을 보유했다. 이 회사는 공모 주식 110만주를 포함해 총 1071만6533주를 상장할 예정이다. 다만 금융당국의 상장 문턱이 한층 높아지고 있는 점은 부담 요소로 거론된다. 금융당국은 지난해 초 기관투자자 의무보유 확약 확대와 상장폐지 요건 강화를 골자로 한 IPO 제도 개편안을 내놓은 이후 상장 심사 전반에 걸쳐 보다 엄격한 기준을 적용하고 있다. 특히 기술성평가 과정에서 기술력과 함께 사업성·시장성을 동시에 요구하는 기조가 뚜렷해진 분위기다.2026-01-12 12:00:19차지현 기자 -
 제미글로·엔트레스토 분쟁 종결 임박...미등재특허 관건[데일리팜=김진구 기자] 연 1500억원 규모의 당뇨병 치료제 '제미글로(제미글립틴)' 시리즈를 둘러싼 특허 분쟁이 대법원 판결을 앞두고 있다. 2심에서 제네릭사의 무효 도전과 회피 도전의 판결이 엇갈린 가운데, 대법원 판결에 따라 제네릭 발매 시점이 9년 앞당겨질 수 있다는 분석이다. 5년 넘게 결론을 내지 못했던 심부전 치료제 '엔트레스토(사쿠비트릴·발사르탄)' 분쟁이 최종 결론을 맞이할지도 관심이다. 1·2심에 이어 특허도전 업체들이 승소할 경우 연 800억원 규모 시장에서 제네릭 빗장이 풀릴 전망이다. 제미글로 특허분쟁 대법원행…2심선 무효·회피 도전 판결 엇갈려 12일 제약업계에 따르면 DPP-4 억제제 계열 당뇨병 치료제 제미글로·제미메트를 둘러싼 특허분쟁이 대법원 판결을 기다리고 있다. 업계에선 이르면 연내 최종 판결이 나올 것으로 전망한다. 분쟁은 두 갈래로 나뉘어 진행 중이다. 제네릭사들은 동일한 용도특허에 소극적 권리범위확인(회피) 심판과 무효 심판을 각각 청구했다. 1심에선 회피·무효 도전 모두 제네릭사가 승리 심결을 받았다. 2심에선 판결이 엇갈렸다. 특허법원은 제네릭사의 회피 도전에 대해선 LG화학의 손을 들어줬다. 반면 무효 도전에 대해선 지난해 말 1심에 이어 제네릭사의 손을 들어주는 판결을 내렸다. 특허법원으로부터 패소한 양 측이 각각 대법원에 상고장을 제출했다. 대법원 판결에 따라 제미글로 제네릭 조기 발매 시점이 9년여 앞당겨질 수 있다는 분석이다. 제네릭사들이 도전장을 낸 제미글로 용도특허의 경우 2039년 10월 만료된다. 제네릭사들은 대법원에서 최종 승소한 뒤, 제미글로 물질특허가 만료되는 2030년 1월 이후 제품을 발매한다는 계획이다. 반면 LG화학이 최종 승소하면 제네릭 발매 시점을 2039년 이후로 늦출 수 있다. 제미글로 시리즈의 연간 처방액은 1500억원 규모로 DPP-4 억제제 시장에서 선두를 달리고 있다. LG화학 입장에선 당뇨병 치료제 시장에서의 영향력을 9년 더 유지할 수 있게 되는 셈이다. 장기 미결론 대형 특허분쟁, 엔트레스토만 남아…대법원 판결 임박 5년 넘게 결론을 맺지 못하고 있는 엔트레스토 특허 분쟁이 연내 마무리될지도 관심을 모은다. 제네릭사가 최종 승소할 경우 연 800억원 규모로 성장한 엔트레스토 제네릭 빗장이 풀린다. 현재 장기간 미결론 상태로 남은 특허분쟁은 사실상 엔트레스토가 유일하다. 지난해의 경우 대법원이 펠루비(펠루비프로펜), 케이캡(테고프라잔), 듀카브(피마사르탄+암로디핀) 관련 최종 판결을 내리며 장기 분쟁의 마침표를 찍은 바 있다. 제네릭사들은 2021년 1월 이후로 엔트레스토 결정형특허, 염·수화물특허, 용도특허 2건, 제제특허 2건 등에 전방위로 심판을 청구했다. 1심에선 제네릭사들이 모두 승리했다. 노바티스는 1심 패배 후 결정형특허와 용도특허, 염·수화물특허 등 3건을 추려 항소했다. 이 가운데 용도특허의 경우 지난해 11월 특허법원으로부터 패소 판결을 받았다. 노바티스는 재차 대법원에 상고했으나, 올해 4월 심리불속행 기각 판결을 받았다. 이로써 남은 특허 분쟁은 2건으로 좁혀졌다. 이 가운데 결정형특허의 경우 노바티스가 2심 패소했다. 노바티스는 즉시 대법원에 상고했다. 염·수화물특허의 경우 2심 재판부의 판결 선고를 기다리고 있다. 특허법원이 어떤 판결을 내리든 대법원행이 유력하게 전망된다. 트라젠타·자디앙 미등재특허 분쟁도 지속…제네릭사 '특허 리스크' 해소될까 베링거인겔하임의 트라젠타와 자디앙을 둘러싼 미등재특허 분쟁도 올해 이어질 것으로 보인다. 제네릭사 입장에선 물질특허 만료 이후 제품 발매를 강행했다. 다만 미등재특허에 의한 리스크가 완전히 해소되지 않은 상황이다. 미등재특허 관련 분쟁에서 제네릭사가 최종 패소할 경우 베링거인겔하임은 특허침해와 이에 따른 손해배상을 청구할 수 있다. 트라젠타·자디앙 미등재특허 분쟁의 경우 몇몇 사건에서 최종 결론이 났다. 다만 워낙 많은 미등재특허를 두고 분쟁이 동시다발로 전개되고 있다는 점에서 최종 판단이 나올 때까지 긴장감이 유지될 것으로 전망된다. 당뇨약 중심 대규모 특허 도전 일단락…'틈새시장 공략'으로 무게 이동 전망 지난 몇 년간 당뇨병 치료제를 중심으로 전개됐던 대규모 특허 도전과 제네릭 우판권(우선판매품목허가) 경쟁이 올해 들어 소강 국면에 접어들 전망이다. 대신 틈새시장을 겨냥한 신규 특허 도전은 더욱 확산할 것으로 예상된다. 2022년 이후 국내 당뇨병 치료제 시장에서는 DPP-4 억제제와 SGLT-2 억제제를 중심으로 대형 품목의 물질특허가 연이어 만료된 바 있다. DPP-4 억제제 계열에서는 2022년 3월 가브스를 시작으로 같은 해 10월 테넬리아, 2023년 9월 자누비아, 2024년 6월 트라젠타까지 주요 제품의 물질특허가 차례로 만료됐다. SGLT-2 억제제 계열에서도 2023년 4월 포시가에 이어 2025년 10월 자디앙의 물질특허가 만료되며 대형 특허 사이클이 사실상 마무리 수순에 들어갔다. 올해 1월엔 셀트리온제약의 네시나(알로글립틴)와 네시나메트 특허가 만료되지만, 신규 특허 도전 가능성은 높지 않을 것으로 예상된다. 지난 몇 년간 다수 제네릭이 출시되면서 당뇨병 치료제 시장이 단기간에 포화 상태에 이르렀기 때문이다. 더구나 알로글립틴 성분 당뇨병 치료제의 경우 처방 규모도 크지 않다는 점에서 추가 진입에 따른 기대 효과가 크지 않다는 분석이다. 우판권 경쟁 역시 예년과는 다른 흐름을 보일 것으로 전망된다. 올해 7월 자디앙·자디앙듀오의 우판권이 만료되지만, 후발 제품의 진입 움직임은 제한적일 것이란 전망이 나온다. 그동안은 대형 당뇨병 치료제의 제네릭 우판권 만료 시점 이후 후발 제품의 진입이 뒤따르는 양상이 반복됐지만, 자디앙의 경우 이미 제네릭이 대거 진입해 시장을 선점한 상태다. 후발주자 입장에선 포화 상태의 시장에 뛰어드는 실익이 크지 않다. 이런 이유로 지난해에 이어 틈새시장을 공략하기 위한 특허 도전이 더욱 확대될 것으로 예상된다. 이미 올해 들어 부광약품의 양극성장애 치료제 '라투다(루라시돈)'를 겨냥한 제네릭사의 특허심판이 청구된 상태다. 라투다의 발매 첫 1년(2024년 4분기~2025년 3분기) 매출이 100억원 내외에 그친다. 지난해의 경우 13개 오리지널 제품이 신규 특허도전 타깃이 됐는데, 이 가운데 ▲현대약품 ‘디엠듀오’ ▲SK케미칼 ‘온젠티스’ ▲다이이찌산쿄 ‘탈리제’ ▲에자이 ‘에퀴피나’ ▲노바티스 ‘자카비’ ▲아스텔라스 ‘엑스탄디’ ▲얀센 ‘서튜러’ ▲산텐 ‘아이커비스점안액’·‘타프콤점안액’ ▲로슈 ‘조플루자’ 등 9개의 2024년 기준 생산·수입 실적이 100억원 안팎으로 집계됐다.2026-01-12 06:00:56김진구 기자
제미글로·엔트레스토 분쟁 종결 임박...미등재특허 관건[데일리팜=김진구 기자] 연 1500억원 규모의 당뇨병 치료제 '제미글로(제미글립틴)' 시리즈를 둘러싼 특허 분쟁이 대법원 판결을 앞두고 있다. 2심에서 제네릭사의 무효 도전과 회피 도전의 판결이 엇갈린 가운데, 대법원 판결에 따라 제네릭 발매 시점이 9년 앞당겨질 수 있다는 분석이다. 5년 넘게 결론을 내지 못했던 심부전 치료제 '엔트레스토(사쿠비트릴·발사르탄)' 분쟁이 최종 결론을 맞이할지도 관심이다. 1·2심에 이어 특허도전 업체들이 승소할 경우 연 800억원 규모 시장에서 제네릭 빗장이 풀릴 전망이다. 제미글로 특허분쟁 대법원행…2심선 무효·회피 도전 판결 엇갈려 12일 제약업계에 따르면 DPP-4 억제제 계열 당뇨병 치료제 제미글로·제미메트를 둘러싼 특허분쟁이 대법원 판결을 기다리고 있다. 업계에선 이르면 연내 최종 판결이 나올 것으로 전망한다. 분쟁은 두 갈래로 나뉘어 진행 중이다. 제네릭사들은 동일한 용도특허에 소극적 권리범위확인(회피) 심판과 무효 심판을 각각 청구했다. 1심에선 회피·무효 도전 모두 제네릭사가 승리 심결을 받았다. 2심에선 판결이 엇갈렸다. 특허법원은 제네릭사의 회피 도전에 대해선 LG화학의 손을 들어줬다. 반면 무효 도전에 대해선 지난해 말 1심에 이어 제네릭사의 손을 들어주는 판결을 내렸다. 특허법원으로부터 패소한 양 측이 각각 대법원에 상고장을 제출했다. 대법원 판결에 따라 제미글로 제네릭 조기 발매 시점이 9년여 앞당겨질 수 있다는 분석이다. 제네릭사들이 도전장을 낸 제미글로 용도특허의 경우 2039년 10월 만료된다. 제네릭사들은 대법원에서 최종 승소한 뒤, 제미글로 물질특허가 만료되는 2030년 1월 이후 제품을 발매한다는 계획이다. 반면 LG화학이 최종 승소하면 제네릭 발매 시점을 2039년 이후로 늦출 수 있다. 제미글로 시리즈의 연간 처방액은 1500억원 규모로 DPP-4 억제제 시장에서 선두를 달리고 있다. LG화학 입장에선 당뇨병 치료제 시장에서의 영향력을 9년 더 유지할 수 있게 되는 셈이다. 장기 미결론 대형 특허분쟁, 엔트레스토만 남아…대법원 판결 임박 5년 넘게 결론을 맺지 못하고 있는 엔트레스토 특허 분쟁이 연내 마무리될지도 관심을 모은다. 제네릭사가 최종 승소할 경우 연 800억원 규모로 성장한 엔트레스토 제네릭 빗장이 풀린다. 현재 장기간 미결론 상태로 남은 특허분쟁은 사실상 엔트레스토가 유일하다. 지난해의 경우 대법원이 펠루비(펠루비프로펜), 케이캡(테고프라잔), 듀카브(피마사르탄+암로디핀) 관련 최종 판결을 내리며 장기 분쟁의 마침표를 찍은 바 있다. 제네릭사들은 2021년 1월 이후로 엔트레스토 결정형특허, 염·수화물특허, 용도특허 2건, 제제특허 2건 등에 전방위로 심판을 청구했다. 1심에선 제네릭사들이 모두 승리했다. 노바티스는 1심 패배 후 결정형특허와 용도특허, 염·수화물특허 등 3건을 추려 항소했다. 이 가운데 용도특허의 경우 지난해 11월 특허법원으로부터 패소 판결을 받았다. 노바티스는 재차 대법원에 상고했으나, 올해 4월 심리불속행 기각 판결을 받았다. 이로써 남은 특허 분쟁은 2건으로 좁혀졌다. 이 가운데 결정형특허의 경우 노바티스가 2심 패소했다. 노바티스는 즉시 대법원에 상고했다. 염·수화물특허의 경우 2심 재판부의 판결 선고를 기다리고 있다. 특허법원이 어떤 판결을 내리든 대법원행이 유력하게 전망된다. 트라젠타·자디앙 미등재특허 분쟁도 지속…제네릭사 '특허 리스크' 해소될까 베링거인겔하임의 트라젠타와 자디앙을 둘러싼 미등재특허 분쟁도 올해 이어질 것으로 보인다. 제네릭사 입장에선 물질특허 만료 이후 제품 발매를 강행했다. 다만 미등재특허에 의한 리스크가 완전히 해소되지 않은 상황이다. 미등재특허 관련 분쟁에서 제네릭사가 최종 패소할 경우 베링거인겔하임은 특허침해와 이에 따른 손해배상을 청구할 수 있다. 트라젠타·자디앙 미등재특허 분쟁의 경우 몇몇 사건에서 최종 결론이 났다. 다만 워낙 많은 미등재특허를 두고 분쟁이 동시다발로 전개되고 있다는 점에서 최종 판단이 나올 때까지 긴장감이 유지될 것으로 전망된다. 당뇨약 중심 대규모 특허 도전 일단락…'틈새시장 공략'으로 무게 이동 전망 지난 몇 년간 당뇨병 치료제를 중심으로 전개됐던 대규모 특허 도전과 제네릭 우판권(우선판매품목허가) 경쟁이 올해 들어 소강 국면에 접어들 전망이다. 대신 틈새시장을 겨냥한 신규 특허 도전은 더욱 확산할 것으로 예상된다. 2022년 이후 국내 당뇨병 치료제 시장에서는 DPP-4 억제제와 SGLT-2 억제제를 중심으로 대형 품목의 물질특허가 연이어 만료된 바 있다. DPP-4 억제제 계열에서는 2022년 3월 가브스를 시작으로 같은 해 10월 테넬리아, 2023년 9월 자누비아, 2024년 6월 트라젠타까지 주요 제품의 물질특허가 차례로 만료됐다. SGLT-2 억제제 계열에서도 2023년 4월 포시가에 이어 2025년 10월 자디앙의 물질특허가 만료되며 대형 특허 사이클이 사실상 마무리 수순에 들어갔다. 올해 1월엔 셀트리온제약의 네시나(알로글립틴)와 네시나메트 특허가 만료되지만, 신규 특허 도전 가능성은 높지 않을 것으로 예상된다. 지난 몇 년간 다수 제네릭이 출시되면서 당뇨병 치료제 시장이 단기간에 포화 상태에 이르렀기 때문이다. 더구나 알로글립틴 성분 당뇨병 치료제의 경우 처방 규모도 크지 않다는 점에서 추가 진입에 따른 기대 효과가 크지 않다는 분석이다. 우판권 경쟁 역시 예년과는 다른 흐름을 보일 것으로 전망된다. 올해 7월 자디앙·자디앙듀오의 우판권이 만료되지만, 후발 제품의 진입 움직임은 제한적일 것이란 전망이 나온다. 그동안은 대형 당뇨병 치료제의 제네릭 우판권 만료 시점 이후 후발 제품의 진입이 뒤따르는 양상이 반복됐지만, 자디앙의 경우 이미 제네릭이 대거 진입해 시장을 선점한 상태다. 후발주자 입장에선 포화 상태의 시장에 뛰어드는 실익이 크지 않다. 이런 이유로 지난해에 이어 틈새시장을 공략하기 위한 특허 도전이 더욱 확대될 것으로 예상된다. 이미 올해 들어 부광약품의 양극성장애 치료제 '라투다(루라시돈)'를 겨냥한 제네릭사의 특허심판이 청구된 상태다. 라투다의 발매 첫 1년(2024년 4분기~2025년 3분기) 매출이 100억원 내외에 그친다. 지난해의 경우 13개 오리지널 제품이 신규 특허도전 타깃이 됐는데, 이 가운데 ▲현대약품 ‘디엠듀오’ ▲SK케미칼 ‘온젠티스’ ▲다이이찌산쿄 ‘탈리제’ ▲에자이 ‘에퀴피나’ ▲노바티스 ‘자카비’ ▲아스텔라스 ‘엑스탄디’ ▲얀센 ‘서튜러’ ▲산텐 ‘아이커비스점안액’·‘타프콤점안액’ ▲로슈 ‘조플루자’ 등 9개의 2024년 기준 생산·수입 실적이 100억원 안팎으로 집계됐다.2026-01-12 06:00:56김진구 기자 -
![[서울 강동] "약사직능 위협 한약사·기형적 약국, 원칙준수"](https://vod.dailypharm.com/new_dailypharm/editor/content/2026/01/10/7b7581de-72be-435f-ab70-c5f5aa949861.png) [서울 강동] "약사직능 위협 한약사·기형적 약국, 원칙준수"[데일리팜=강혜경 기자] 강동구약사회(회장 신민경)가 한약사 문제, 기형적 약국 등 난립하는 현안과 관련해 회원들과 함께 해결해 나가자는 데 뜻을 모았다. 원칙을 준수하며 제도와 법이 마련될 때까지 각자의 자리에서 최선을 다하겠다는 것이다. 구약사회는 10일 강동경희대병원 별관 4층 차후영홀에서 제47회 정기총회를 열고 올해 사업계획과 예산 등을 심의했다. 총회에 앞서 박근희 의장은 "정기총회는 지난 1년을 결산하는 자리를 넘어 약사회가 나아갈 100년의 길을 모색하는 중차대한 자리"라며 "심도있고 건설적인 논의를 통해 약사회가 더욱 발전할 수 있는 토대를 만들어 주시기를 부탁드리며, 한 해 동안 헌신하고 봉사해 준 회원들께 감사드린다"고 개회사를 전했다. 신민경 회장은 한약사 문제와 창고형·마트형 약국 같은 기형적 약국 확산에 대해 지적했다. 또 수급불안정 의약품과 비대면 진료 플랫폼 업체의 도매상 운영 금지법안이 국회 본회의 문턱에서 멈춰선 현실 등을 지적하며 "보건의료는 편의와 속도가 아닌 안전과 책임의 문제"라며 "침묵은 아무것도 바꾸지 못한다. 회원들과 함께 원칙이 지켜질 수 있도록 최선을 다하겠다"고 강조했다. 리병도 서울시약사회 부회장 역시 "약국과 약사의 본질을 고민해야 할 때"라며 "속도가 아닌 원칙과 방향이 바로설 수 있도록 서울시약사회가 대한약사회와 함께 노력해 나갈 것"이라고 말했다. 이수희 강동구청장은 축사에서 "국민보건향상을 위해 늘 힘써주는 약사회원님들께 감사드린다"며 "3월 시행되는 통합돌봄에 약사님들이 적극 참여해 큰 역할을 해주시기를 당부드린다"고 밝혔다. 전주혜 전 국민의힘 의원도 "대체조제 사후통보 간소화가 시행된다는 점에서는 환영하는 부분"이라며 "약사와 한약사간 업무를 정확히 하는 법 규정이 이뤄질 수 있도록 노력하겠다"고 약속했다. 조동탁 강동구의회 의장도 "어려운 경기 속에서 약국 역시 피해가 크다. 특히 온라인과 생활용품점 등에 시장을 뺐기고 있다"며 "올해는 약사사회가 더 발전하시기를 바란다"는 말로 축사를 갈음했다. 약사회는 구청에 '희망온돌 나눔 성금' 300만원을 기탁했으며, 한약사 문제 해결을 촉구했다. 구체적으로 ▲약사, 한약사 면허범위 바로세워 국민건강 보장하라! ▲약사는 약국, 한약사는 한약국 정부는 즉각 분리하라! ▲면허범위 무시한 한약사 불법행위 정부는 즉각 처벌하라! ▲정부의 무원칙, 무대응, 무책임으로 국민안전 무너진다! ▲한약사 문제 방치 30년 정부는 해결책을 마련하라! 등의 구호를 외쳤다. 2025년도 감사 및 세입·세출 결산, 2026년도 위원회 사업계획, 세입·세출 예산 등은 원안대로 승인됐다. 구약사회는 올해 돌봄통합에서 약사의 역할을 확대하는 한편 의약품 정보 진위 팩트체크 카드뉴스를 새롭게 제공하기로 했다. 또 순차적으로 약국 청구소프트웨어 프로그램을 변경할 수 있도록 안내한다는 계획이다. 아울러 반회 활성화를 통한 회원간 교류 확대, 동호회 활성화 등을 중점 추진하기로 했다. 분회비 41만원은 동결됐으며, 올해 예산으로는 1억5375만원이 책정됐다. 한편 이날 총회에는 리병도 서울시약사회 부회장, 박근희 강동구약사회 총회의장, 이수희 강동구청장, 조동탁 강동구의회의장, 전주혜 전 국민의힘 의원, 이종태 시의원, 박춘선 시의원, 김영철 시의원, 최정수 보건소장 등이 참석했다. [총회 수상자] ◆서울시약사회장 표창: 송혁중(큰사랑약국), 임은주(마리온누리약국) ◆강동구청장 표창: 이은아 ◆강동구약사회장 표창장: 안영희(온정약국), 노경균(동명약국), 강민경(아산자성약국), 장지연(강동365약국) ◆강동구약사회장 감사패: 장진호(일동제약), 정상훈(쥴릭파마코리아) ◆강동구약사회장 공로패: 윤복순(보은약국), 정언약국(황혜익), 김명희(고려약국)2026-01-10 19:51:55강혜경 기자
[서울 강동] "약사직능 위협 한약사·기형적 약국, 원칙준수"[데일리팜=강혜경 기자] 강동구약사회(회장 신민경)가 한약사 문제, 기형적 약국 등 난립하는 현안과 관련해 회원들과 함께 해결해 나가자는 데 뜻을 모았다. 원칙을 준수하며 제도와 법이 마련될 때까지 각자의 자리에서 최선을 다하겠다는 것이다. 구약사회는 10일 강동경희대병원 별관 4층 차후영홀에서 제47회 정기총회를 열고 올해 사업계획과 예산 등을 심의했다. 총회에 앞서 박근희 의장은 "정기총회는 지난 1년을 결산하는 자리를 넘어 약사회가 나아갈 100년의 길을 모색하는 중차대한 자리"라며 "심도있고 건설적인 논의를 통해 약사회가 더욱 발전할 수 있는 토대를 만들어 주시기를 부탁드리며, 한 해 동안 헌신하고 봉사해 준 회원들께 감사드린다"고 개회사를 전했다. 신민경 회장은 한약사 문제와 창고형·마트형 약국 같은 기형적 약국 확산에 대해 지적했다. 또 수급불안정 의약품과 비대면 진료 플랫폼 업체의 도매상 운영 금지법안이 국회 본회의 문턱에서 멈춰선 현실 등을 지적하며 "보건의료는 편의와 속도가 아닌 안전과 책임의 문제"라며 "침묵은 아무것도 바꾸지 못한다. 회원들과 함께 원칙이 지켜질 수 있도록 최선을 다하겠다"고 강조했다. 리병도 서울시약사회 부회장 역시 "약국과 약사의 본질을 고민해야 할 때"라며 "속도가 아닌 원칙과 방향이 바로설 수 있도록 서울시약사회가 대한약사회와 함께 노력해 나갈 것"이라고 말했다. 이수희 강동구청장은 축사에서 "국민보건향상을 위해 늘 힘써주는 약사회원님들께 감사드린다"며 "3월 시행되는 통합돌봄에 약사님들이 적극 참여해 큰 역할을 해주시기를 당부드린다"고 밝혔다. 전주혜 전 국민의힘 의원도 "대체조제 사후통보 간소화가 시행된다는 점에서는 환영하는 부분"이라며 "약사와 한약사간 업무를 정확히 하는 법 규정이 이뤄질 수 있도록 노력하겠다"고 약속했다. 조동탁 강동구의회 의장도 "어려운 경기 속에서 약국 역시 피해가 크다. 특히 온라인과 생활용품점 등에 시장을 뺐기고 있다"며 "올해는 약사사회가 더 발전하시기를 바란다"는 말로 축사를 갈음했다. 약사회는 구청에 '희망온돌 나눔 성금' 300만원을 기탁했으며, 한약사 문제 해결을 촉구했다. 구체적으로 ▲약사, 한약사 면허범위 바로세워 국민건강 보장하라! ▲약사는 약국, 한약사는 한약국 정부는 즉각 분리하라! ▲면허범위 무시한 한약사 불법행위 정부는 즉각 처벌하라! ▲정부의 무원칙, 무대응, 무책임으로 국민안전 무너진다! ▲한약사 문제 방치 30년 정부는 해결책을 마련하라! 등의 구호를 외쳤다. 2025년도 감사 및 세입·세출 결산, 2026년도 위원회 사업계획, 세입·세출 예산 등은 원안대로 승인됐다. 구약사회는 올해 돌봄통합에서 약사의 역할을 확대하는 한편 의약품 정보 진위 팩트체크 카드뉴스를 새롭게 제공하기로 했다. 또 순차적으로 약국 청구소프트웨어 프로그램을 변경할 수 있도록 안내한다는 계획이다. 아울러 반회 활성화를 통한 회원간 교류 확대, 동호회 활성화 등을 중점 추진하기로 했다. 분회비 41만원은 동결됐으며, 올해 예산으로는 1억5375만원이 책정됐다. 한편 이날 총회에는 리병도 서울시약사회 부회장, 박근희 강동구약사회 총회의장, 이수희 강동구청장, 조동탁 강동구의회의장, 전주혜 전 국민의힘 의원, 이종태 시의원, 박춘선 시의원, 김영철 시의원, 최정수 보건소장 등이 참석했다. [총회 수상자] ◆서울시약사회장 표창: 송혁중(큰사랑약국), 임은주(마리온누리약국) ◆강동구청장 표창: 이은아 ◆강동구약사회장 표창장: 안영희(온정약국), 노경균(동명약국), 강민경(아산자성약국), 장지연(강동365약국) ◆강동구약사회장 감사패: 장진호(일동제약), 정상훈(쥴릭파마코리아) ◆강동구약사회장 공로패: 윤복순(보은약국), 정언약국(황혜익), 김명희(고려약국)2026-01-10 19:51:55강혜경 기자 -
 네트워크·창고형·H&B…'1약사 1약국' 경계 허물어지나[데일리팜=김지은 기자] 문전약국을 중심으로 불거졌던 ‘네트워크 약국’ 논란이 최근 대규모 기형적 약국의 잇따른 개설까지 맞물리며 확산되고 있다. 약사사회 안팎에서는 약국 운영을 둘러싼 ‘1인 1개소’ 원칙의 경계가 점차 흐려지고 있다는 우려도 나온다. 경찰과 검찰은 지난해 한 명의 약사가 여러 문전약국 운영에 관여한 사건에 대해 무혐의 취지의 불송치·불기소 결정을 내린 바 있다. 수사기관은 해당 사안이 약사법상 금지된 ‘면허대여’에 해당하려면 명의 대여나 개설 주체의 위장 등 명백한 위법성이 입증돼야 한다는 점을 강조했다. 단순 자본 투자나 운영 관여만으로는 면허대여로 보기 어렵다는 판단이다. 유사한 사례는 사법부 판단에서도 찾을 수 있다. 한진그룹이 개입된 인하대병원 문전약국 면허대여 사건과 관련, 유죄였던 1심 판결이 2심에서 무죄로 뒤집힌 후 대법원에서 최종 확정된 바 있다. 당시 법원은 약사 명의만 빌려 운영하는 일반 면대약국과는 달리 개설 약사가 복약지도, 판매 등 약국 실질 운영을 했다며 면대가 아닌 ‘차명’으로 봐야한다는 판단을 해 논란이 되기도 했다. 최근 특정 주체의 개입이 의심되는 대형 마트형, 창고형약국을 넘어 H&B 스토어 입점 약국이 줄을 이으면서 약사사회에서는 법의 기준을 교묘히 이용한 새로운 형태의 약국 운영 방식이 확산되고 있는 것 아니냐는 문제의식이 커지고 있다. 겉으로는 개별 약사가 개설·운영하는 약국의 외형을 갖추고 있지만, 실질적으로는 외부 자본이나 특정 조직이 약국 경영 전반에 깊숙이 관여하는 구조가 늘고 있다는 것이다. 유사 형태 마트·창고형약국에 특정 법인·체인 개입 형도…‘운영 관여’ 논란 이 같은 논란은 최근 대규모 약국의 우후죽순 개설되는 상황과 맞물리며 더욱 증폭되는 분위기다. 최근에는 약국이 H&B 스토어에 전전대 계약을 맺고 입점하는 모델도 등장하고 있다. 특정 법인과 관련되는 형태인데, 개설 약사가 약국 개설, 운영의 전반을 책임지는 기존 방식과 달리 이 같은 모델의 약국은 개설과 운영 과정 상당 부분을 H&B스토어 측이 담당하거나 개입돼 있는 것으로 알려졌다. 약국가에 따르면 특정 체인 업체 가입을 통한 H&B(헬스앤뷰티) 결합형 대형 약국의 경우도 체인이 개설 약국으로부터 가맹비 명목의 마케팅 비용을 청구하고, 대신 광고·홍보·마케팅 전반을 수행하는 구조가 형성되고 있는 것으로 알려졌다. 형식상 약국의 개설자와 운영 책임자는 약사 개인이지만, 실제로는 체인이 마케팅 전략과 소비자 유입 구조를 좌우하면서 개별 약국 경영에 상당한 영향력을 행사하고 있다는 지적이다. 지역 약사회 관계자는 “이런 모델들은 법적으로는 개설에 관여하지 않았지만, 실질적으로는 개설, 운영에 특정 법인이나 체인이 깊숙이 개입하고 관여하는 형태로 볼 수 있다”고 말했다. 이 관계자는 “최근 마트, 창고형약국의 경우는 입지 선정, 인테리어, 상품 구성, 마케팅까지 이미 일정한 모듈화가 이뤄진 상태”라며 “자본이나 운영 방식 측면에서 사실상 법인 약국과 유사한 형태로 진화하고 있는 것으로 보인다”고 지적했다. ‘합법과 탈법 사이’…흐려지는 ‘1인 1개소’ 원칙? 약사들이 우려하는 지점은 바로 이 대목이다. 현행 약사법이 개설과 운영을 엄격히 구분하고 있는 틈새를 활용해 대자본이나 특정 법인, 체인 조직이 약국 운영에 실질적으로 관여하면서도 법적 책임에서는 한 발 비켜서는 구조가 고착화될 수 있다는 것이다. 네트워크 약국 무혐의 사례나 차명약국 무죄를 판단과 같이 수사기관, 사법부가 약국의 ‘명의 대여’ 여부를 엄격하게 해석하는 상황에서 이런 형태의 약국 운영이 제재 없이 확산될 경우 1인 1개소 약국 운영 원칙 자체가 형해화될 수 있다는 지적도 제기된다. 지역의 한 약사는 “결국 약사들이 가장 경계해 온 사실상 법인약국이 다른 이름과 방식으로 등장하고 있는 것”이라며 “법의 문구는 지켰지만 취지는 무력화되는 상황”이라고 우려했다. 전문가들은 이런 흐름이 단순 개별 약국이나 특정 모델의 문제가 아닌 약국 제도 전반에 영향을 미칠 수 있다고 지적한다. 개설과 운영, 자본과 전문성의 경계를 어디까지 허용할 것인지에 대한 사회적·입법적 합의가 부재한 상태에서 시장은 이미 한발 앞서 움직이고 있다는 우려에서다. 이런 현상이 더 확산되고 나아가 법망을 교묘히 피한 대자본 개입 약국이 확산되기 위해서는 법적으로 경계선을 더 명확히 그어야 한다는 말도 나온다. 지역 약사회 한 관계자는 “현행 약사법 상 1인 1개소 원칙은 명문화돼 있지만 약국 운영 관여 등에 대해서는 명확한 원칙이 없다보니 경계가 흐려지고 있다”며 “아예 개설 제한을 강화하거나 운영 개입을 처벌하는 별도 조항 마련 같은 형태의 근본적 입법 명문화가 필요할 것으로 보인다”고 했다.2026-01-10 06:00:58김지은 기자
네트워크·창고형·H&B…'1약사 1약국' 경계 허물어지나[데일리팜=김지은 기자] 문전약국을 중심으로 불거졌던 ‘네트워크 약국’ 논란이 최근 대규모 기형적 약국의 잇따른 개설까지 맞물리며 확산되고 있다. 약사사회 안팎에서는 약국 운영을 둘러싼 ‘1인 1개소’ 원칙의 경계가 점차 흐려지고 있다는 우려도 나온다. 경찰과 검찰은 지난해 한 명의 약사가 여러 문전약국 운영에 관여한 사건에 대해 무혐의 취지의 불송치·불기소 결정을 내린 바 있다. 수사기관은 해당 사안이 약사법상 금지된 ‘면허대여’에 해당하려면 명의 대여나 개설 주체의 위장 등 명백한 위법성이 입증돼야 한다는 점을 강조했다. 단순 자본 투자나 운영 관여만으로는 면허대여로 보기 어렵다는 판단이다. 유사한 사례는 사법부 판단에서도 찾을 수 있다. 한진그룹이 개입된 인하대병원 문전약국 면허대여 사건과 관련, 유죄였던 1심 판결이 2심에서 무죄로 뒤집힌 후 대법원에서 최종 확정된 바 있다. 당시 법원은 약사 명의만 빌려 운영하는 일반 면대약국과는 달리 개설 약사가 복약지도, 판매 등 약국 실질 운영을 했다며 면대가 아닌 ‘차명’으로 봐야한다는 판단을 해 논란이 되기도 했다. 최근 특정 주체의 개입이 의심되는 대형 마트형, 창고형약국을 넘어 H&B 스토어 입점 약국이 줄을 이으면서 약사사회에서는 법의 기준을 교묘히 이용한 새로운 형태의 약국 운영 방식이 확산되고 있는 것 아니냐는 문제의식이 커지고 있다. 겉으로는 개별 약사가 개설·운영하는 약국의 외형을 갖추고 있지만, 실질적으로는 외부 자본이나 특정 조직이 약국 경영 전반에 깊숙이 관여하는 구조가 늘고 있다는 것이다. 유사 형태 마트·창고형약국에 특정 법인·체인 개입 형도…‘운영 관여’ 논란 이 같은 논란은 최근 대규모 약국의 우후죽순 개설되는 상황과 맞물리며 더욱 증폭되는 분위기다. 최근에는 약국이 H&B 스토어에 전전대 계약을 맺고 입점하는 모델도 등장하고 있다. 특정 법인과 관련되는 형태인데, 개설 약사가 약국 개설, 운영의 전반을 책임지는 기존 방식과 달리 이 같은 모델의 약국은 개설과 운영 과정 상당 부분을 H&B스토어 측이 담당하거나 개입돼 있는 것으로 알려졌다. 약국가에 따르면 특정 체인 업체 가입을 통한 H&B(헬스앤뷰티) 결합형 대형 약국의 경우도 체인이 개설 약국으로부터 가맹비 명목의 마케팅 비용을 청구하고, 대신 광고·홍보·마케팅 전반을 수행하는 구조가 형성되고 있는 것으로 알려졌다. 형식상 약국의 개설자와 운영 책임자는 약사 개인이지만, 실제로는 체인이 마케팅 전략과 소비자 유입 구조를 좌우하면서 개별 약국 경영에 상당한 영향력을 행사하고 있다는 지적이다. 지역 약사회 관계자는 “이런 모델들은 법적으로는 개설에 관여하지 않았지만, 실질적으로는 개설, 운영에 특정 법인이나 체인이 깊숙이 개입하고 관여하는 형태로 볼 수 있다”고 말했다. 이 관계자는 “최근 마트, 창고형약국의 경우는 입지 선정, 인테리어, 상품 구성, 마케팅까지 이미 일정한 모듈화가 이뤄진 상태”라며 “자본이나 운영 방식 측면에서 사실상 법인 약국과 유사한 형태로 진화하고 있는 것으로 보인다”고 지적했다. ‘합법과 탈법 사이’…흐려지는 ‘1인 1개소’ 원칙? 약사들이 우려하는 지점은 바로 이 대목이다. 현행 약사법이 개설과 운영을 엄격히 구분하고 있는 틈새를 활용해 대자본이나 특정 법인, 체인 조직이 약국 운영에 실질적으로 관여하면서도 법적 책임에서는 한 발 비켜서는 구조가 고착화될 수 있다는 것이다. 네트워크 약국 무혐의 사례나 차명약국 무죄를 판단과 같이 수사기관, 사법부가 약국의 ‘명의 대여’ 여부를 엄격하게 해석하는 상황에서 이런 형태의 약국 운영이 제재 없이 확산될 경우 1인 1개소 약국 운영 원칙 자체가 형해화될 수 있다는 지적도 제기된다. 지역의 한 약사는 “결국 약사들이 가장 경계해 온 사실상 법인약국이 다른 이름과 방식으로 등장하고 있는 것”이라며 “법의 문구는 지켰지만 취지는 무력화되는 상황”이라고 우려했다. 전문가들은 이런 흐름이 단순 개별 약국이나 특정 모델의 문제가 아닌 약국 제도 전반에 영향을 미칠 수 있다고 지적한다. 개설과 운영, 자본과 전문성의 경계를 어디까지 허용할 것인지에 대한 사회적·입법적 합의가 부재한 상태에서 시장은 이미 한발 앞서 움직이고 있다는 우려에서다. 이런 현상이 더 확산되고 나아가 법망을 교묘히 피한 대자본 개입 약국이 확산되기 위해서는 법적으로 경계선을 더 명확히 그어야 한다는 말도 나온다. 지역 약사회 한 관계자는 “현행 약사법 상 1인 1개소 원칙은 명문화돼 있지만 약국 운영 관여 등에 대해서는 명확한 원칙이 없다보니 경계가 흐려지고 있다”며 “아예 개설 제한을 강화하거나 운영 개입을 처벌하는 별도 조항 마련 같은 형태의 근본적 입법 명문화가 필요할 것으로 보인다”고 했다.2026-01-10 06:00:58김지은 기자 -
 '2세 경영' 우정바이오, 오픈이노 확대…재무 건전성 숙제[데일리팜=차지현 기자] 비임상 임상시험 수탁사업(CRO) 전문 기업 우정바이오가 차세대 비임상 기술 도입과 오픈이노베이션 등 신성장동력 발굴을 위한 전방위 행보에 나서고 있다. 오너 2세 체제 출범 이후 중장기 성장 전략 실행에 나선 것으로 풀이된다. 다만 주가 부양과 재무 안정성 확보는 향후 풀어야 할 과제다. 엑셀라·갤럭스 등 글로벌 파트너십 확대… 차세대 비임상 플랫폼 도약 9일 바이오 업계에 따르면 우정바이오는 최근 차세대 인공지능(AI)과 오간온어칩(Organ-on-a-Chip) 기반 신약개발 플랫폼 기업 엑셀라 바이오시스템즈와 전략적 파트너십을 체결했다. 이번 협력은 양사 기술과 연구 역량을 결합해 인체 모사 중심 비임상 연구 솔루션을 공동으로 개발하는 것을 목표로 한다. 인체 모사 중심 비임상 연구란 사람 장기의 생리적 특성을 반영한 실험 모델을 통해 임상 결과 예측력을 높이려는 차세대 비임상 접근법이다. 엑셀라는 AI 기반 오간온어칩 플랫폼과 컴퓨터 비전 기반 이미지 분석 파이프라인, 고도화된 데이터 분석 역량을 제공한다. 우정바이오는 중개연구와 비임상 연구 전반에 걸친 풍부한 경험과 연구 인프라를 접목할 계획이다. 이를 통해 양사는 연구 효율성과 데이터 품질·재현성을 높이고 신약개발 전반에서 예측 기반 비임상 연구 접근을 강화한다는 구상이다. 우정바이오의 이 같은 오픈이노베이션 행보는 이번이 처음이 아니다. 우정바이오는 최근 들어 국내외 바이오텍, AI 신약개발 기업과 협업을 잇달아 추진하며 신약개발 전주기 비임상 파트너로 역할 확대에 속도를 내는 모습이다. 우정바이오는 지난해 11월 단백질 구조기반 신약개발 기업 마스터메디텍과 손잡고 진행성 간세포암(HCC) 타깃 신약 후보물질 개발 협력에 나섰다. 마스터메디텍은 단백질 구조 정보를 기반으로 신약 후보물질을 설계·개발하는 구조기반 신약개발(SBDD) 전문 바이오벤처로 항암제와 대사질환 치료제 등 다수의 초기 파이프라인을 보유 중이다. 우정바이오는 해당 프로젝트에서 비임상 데이터를 신속히 확보하고 적응증 확장과 기술이전 가능성까지 염두에 둔 중개연구를 지원한다. 이에 앞서 지난해 9월에는 AI 기반 신약개발 플랫폼 기업 갤럭스와 전략적 업무협약을 체결했다. 갤럭스는 AI와 물리화학적 원리를 결합한 자체 플랫폼을 통해 신약 후보물질을 설계하는 기업이다. 양사는 AI로 설계한 신약 후보물질을 비임상 단계에서 신속하게 검증하는 협력 모델을 구축해 신약개발 효율과 성공 가능성을 높인다는 구상이다. 산업·스타트업 행사 참여도 적극적이다. 지난달에는 글로벌 스타트업 페스티벌 컴업(COMEUP) 2025에 참가해 신규 오픈이노베이션 파트너 발굴과 글로벌 협업 네트워크 확장에 나섰다. 컴업은 중소벤처기업부가 주관하는 국내 최대 규모 글로벌 스타트업 행사로 아시아·유럽·북미 등 전 세계 스타트업과 글로벌 벤처캐피탈(VC), 대기업, 연구기관이 한자리에 모이는 오픈이노베이션 플랫폼이다. 우정바이오는 해당 행사에서 공유동물실(Vivashare)과 개방형 연구 인프라(LAB CLOUD)를 활용한 비임상 협업 모델을 제시했다. 우정바이오는 1989년 설립된 비임상 CRO와 감염관리 전문 기업이다. 실험용 무균동물(SPF) 공급을 출발점으로 성장해 왔다. 이후 비임상 CRO 서비스와 병원·연구시설 감염관리(E&C) 사업으로 사업 영역을 확장했고 2017년 4월 한화엠지아이기업인수목적회사(SPAC)와 합병을 통해 코스닥 시장에 상장했다. 상장 이후 사명을 우정바이오로 변경했다. 작년부터는 사업 전반에서 변화가 본격화하고 있다. 기존 비임상 CRO와 감염관리 중심 사업에서 나아가 오픈이노베이션과 AI·차세대 비임상 기술을 결합한 플랫폼 전략을 전면에 내세우며 사업 모델 확장에 나섰다. AI 신약개발 기업과 협업, 인큐베이팅·액셀러레이팅 기능 강화, 차세대 비임상 연구 인프라 구축 등을 통해 플랫폼형 비임상 파트너로 전환을 꾀하고 있다. 이 같은 변화는 창업주 천병년 회장 작고 이후 오너 2세 체제로 전환되면서 가속화하는 분위기다. 우정바이오는 지난해 5월 16일 천병년 회장 별세 이후 같은 달 22일 천희정 대표를 신임 대표이사로 선임했다. 천희정 대표는 천병년 회장의 장녀로 2019년 회사에 입사한 뒤 홍보팀장, 전략기획실장, 미래전략기획실장 등을 거치며 중장기 전략 수립과 플랫폼 사업을 주도해 온 인물이다. 천희정 대표 체제 출범 이후 오픈이노베이션과 AI·차세대 비임상 기술을 축으로 한 사업 전환이 보다 속도감 있게 추진되고 있다는 평가다. 부채비율 265%·CB 풋옵션 압박…유동성 관리 및 주가 관리 '빨간 불' 사업 전반에서 변화가 본격화하고 있지만 주가 부양과 재무 안정성 확보는 여전히 과제로 남아 있다. 작년 9월 말 우정바이오 연결기준 부채비율은 265.4%로 2024년 12월 말 부채비율 222.4% 대비 43.0%포인트 상승하며 재무 부담이 가중된 상태다. 대규모 신약 클러스터 인프라 구축과 차세대 기술 투자를 지속하면서 부채 규모가 커진 결과로 해석된다. 단기 유동성 압박도 부담 요인이다. 현재 우정바이오의 제8회차 전환사채(CB) 미상환 잔액은 35억원이다. 회사는 지난해 10월 매도청구권(콜옵션)을 행사해 15억원 규모 CB를 만기 이전에 취득하며 일부 부담을 줄였지만 여전히 상당 규모의 CB가 남아 있다. 8일 종가 기준 우정바이오 주가는 1923원으로 해당 CB 전환가액 2515원보다 약 23.5% 낮다. 투자자가 주식 전환 대신 현금 상환을 요구할 가능성이 큰 상황인 셈이다. 특이 이 CB는 지난해 11월부터 매 3개월마다 조기상환청구(풋옵션) 행사가 가능한 구조다. 주가가 전환가액을 하회하는 상황이 지속될 경우 당장 내달 말로 예정된 조기상환 청구일에 투자자 상환 요구가 집중될 수 있다는 분석이다. 문제는 우정바이오의 가용 현금이 넉넉하지 않다는 점이다. 지난해 9월 말 우정바이오의 현금 및 현금성 자산은 약 22억원으로 잔여 CB 원금(35억원)을 상환하기에도 빠듯한 수준이다. 여기에 1년 이내에 만기가 도래하는 단기차입금 규모만 약 164억원에 달해 보유 현금과 상환 예정 부채 간 격차가 큰 상황이다. 추가적인 자금 조달 방안이나 주가 부양을 통한 자본 구조 개선 필요성이 제기되는 이유다. 시가총액 방어 역시 중요한 관리 지표로 떠오르고 있다. 금융당국은 기관투자자 의무보유 확약 확대와 상장폐지 요건 강화를 골자로 한 기업공개(IPO)와 상장폐지 제도 개선 방안을 추진 중이다. 이에 따르면 상장 유지 기준이 3년에 걸쳐 단계적으로 상향된다. 코스닥 시가총액 요건은 올해 150억원, 2027년 200억원을 거쳐 2028년 300억원까지 대폭 높아진 전망이다. 8일 종가 기준 우정바이오의 시가총액은 324억원으로 300억원을 웃돌고 있다. 다만 지난 5일까지만 해도 시가총액이 300억원을 하회하는 구간이 이어지는 등 기준선 인근에서 등락을 반복 중이다. 강화되는 규제 가이드라인에 안정적으로 안착하기 위해 주가 변동성을 낮추고 시가총액을 일정 수준 이상으로 유지하는 게 필수적이라는 지적이다.2026-01-10 06:00:44차지현 기자
'2세 경영' 우정바이오, 오픈이노 확대…재무 건전성 숙제[데일리팜=차지현 기자] 비임상 임상시험 수탁사업(CRO) 전문 기업 우정바이오가 차세대 비임상 기술 도입과 오픈이노베이션 등 신성장동력 발굴을 위한 전방위 행보에 나서고 있다. 오너 2세 체제 출범 이후 중장기 성장 전략 실행에 나선 것으로 풀이된다. 다만 주가 부양과 재무 안정성 확보는 향후 풀어야 할 과제다. 엑셀라·갤럭스 등 글로벌 파트너십 확대… 차세대 비임상 플랫폼 도약 9일 바이오 업계에 따르면 우정바이오는 최근 차세대 인공지능(AI)과 오간온어칩(Organ-on-a-Chip) 기반 신약개발 플랫폼 기업 엑셀라 바이오시스템즈와 전략적 파트너십을 체결했다. 이번 협력은 양사 기술과 연구 역량을 결합해 인체 모사 중심 비임상 연구 솔루션을 공동으로 개발하는 것을 목표로 한다. 인체 모사 중심 비임상 연구란 사람 장기의 생리적 특성을 반영한 실험 모델을 통해 임상 결과 예측력을 높이려는 차세대 비임상 접근법이다. 엑셀라는 AI 기반 오간온어칩 플랫폼과 컴퓨터 비전 기반 이미지 분석 파이프라인, 고도화된 데이터 분석 역량을 제공한다. 우정바이오는 중개연구와 비임상 연구 전반에 걸친 풍부한 경험과 연구 인프라를 접목할 계획이다. 이를 통해 양사는 연구 효율성과 데이터 품질·재현성을 높이고 신약개발 전반에서 예측 기반 비임상 연구 접근을 강화한다는 구상이다. 우정바이오의 이 같은 오픈이노베이션 행보는 이번이 처음이 아니다. 우정바이오는 최근 들어 국내외 바이오텍, AI 신약개발 기업과 협업을 잇달아 추진하며 신약개발 전주기 비임상 파트너로 역할 확대에 속도를 내는 모습이다. 우정바이오는 지난해 11월 단백질 구조기반 신약개발 기업 마스터메디텍과 손잡고 진행성 간세포암(HCC) 타깃 신약 후보물질 개발 협력에 나섰다. 마스터메디텍은 단백질 구조 정보를 기반으로 신약 후보물질을 설계·개발하는 구조기반 신약개발(SBDD) 전문 바이오벤처로 항암제와 대사질환 치료제 등 다수의 초기 파이프라인을 보유 중이다. 우정바이오는 해당 프로젝트에서 비임상 데이터를 신속히 확보하고 적응증 확장과 기술이전 가능성까지 염두에 둔 중개연구를 지원한다. 이에 앞서 지난해 9월에는 AI 기반 신약개발 플랫폼 기업 갤럭스와 전략적 업무협약을 체결했다. 갤럭스는 AI와 물리화학적 원리를 결합한 자체 플랫폼을 통해 신약 후보물질을 설계하는 기업이다. 양사는 AI로 설계한 신약 후보물질을 비임상 단계에서 신속하게 검증하는 협력 모델을 구축해 신약개발 효율과 성공 가능성을 높인다는 구상이다. 산업·스타트업 행사 참여도 적극적이다. 지난달에는 글로벌 스타트업 페스티벌 컴업(COMEUP) 2025에 참가해 신규 오픈이노베이션 파트너 발굴과 글로벌 협업 네트워크 확장에 나섰다. 컴업은 중소벤처기업부가 주관하는 국내 최대 규모 글로벌 스타트업 행사로 아시아·유럽·북미 등 전 세계 스타트업과 글로벌 벤처캐피탈(VC), 대기업, 연구기관이 한자리에 모이는 오픈이노베이션 플랫폼이다. 우정바이오는 해당 행사에서 공유동물실(Vivashare)과 개방형 연구 인프라(LAB CLOUD)를 활용한 비임상 협업 모델을 제시했다. 우정바이오는 1989년 설립된 비임상 CRO와 감염관리 전문 기업이다. 실험용 무균동물(SPF) 공급을 출발점으로 성장해 왔다. 이후 비임상 CRO 서비스와 병원·연구시설 감염관리(E&C) 사업으로 사업 영역을 확장했고 2017년 4월 한화엠지아이기업인수목적회사(SPAC)와 합병을 통해 코스닥 시장에 상장했다. 상장 이후 사명을 우정바이오로 변경했다. 작년부터는 사업 전반에서 변화가 본격화하고 있다. 기존 비임상 CRO와 감염관리 중심 사업에서 나아가 오픈이노베이션과 AI·차세대 비임상 기술을 결합한 플랫폼 전략을 전면에 내세우며 사업 모델 확장에 나섰다. AI 신약개발 기업과 협업, 인큐베이팅·액셀러레이팅 기능 강화, 차세대 비임상 연구 인프라 구축 등을 통해 플랫폼형 비임상 파트너로 전환을 꾀하고 있다. 이 같은 변화는 창업주 천병년 회장 작고 이후 오너 2세 체제로 전환되면서 가속화하는 분위기다. 우정바이오는 지난해 5월 16일 천병년 회장 별세 이후 같은 달 22일 천희정 대표를 신임 대표이사로 선임했다. 천희정 대표는 천병년 회장의 장녀로 2019년 회사에 입사한 뒤 홍보팀장, 전략기획실장, 미래전략기획실장 등을 거치며 중장기 전략 수립과 플랫폼 사업을 주도해 온 인물이다. 천희정 대표 체제 출범 이후 오픈이노베이션과 AI·차세대 비임상 기술을 축으로 한 사업 전환이 보다 속도감 있게 추진되고 있다는 평가다. 부채비율 265%·CB 풋옵션 압박…유동성 관리 및 주가 관리 '빨간 불' 사업 전반에서 변화가 본격화하고 있지만 주가 부양과 재무 안정성 확보는 여전히 과제로 남아 있다. 작년 9월 말 우정바이오 연결기준 부채비율은 265.4%로 2024년 12월 말 부채비율 222.4% 대비 43.0%포인트 상승하며 재무 부담이 가중된 상태다. 대규모 신약 클러스터 인프라 구축과 차세대 기술 투자를 지속하면서 부채 규모가 커진 결과로 해석된다. 단기 유동성 압박도 부담 요인이다. 현재 우정바이오의 제8회차 전환사채(CB) 미상환 잔액은 35억원이다. 회사는 지난해 10월 매도청구권(콜옵션)을 행사해 15억원 규모 CB를 만기 이전에 취득하며 일부 부담을 줄였지만 여전히 상당 규모의 CB가 남아 있다. 8일 종가 기준 우정바이오 주가는 1923원으로 해당 CB 전환가액 2515원보다 약 23.5% 낮다. 투자자가 주식 전환 대신 현금 상환을 요구할 가능성이 큰 상황인 셈이다. 특이 이 CB는 지난해 11월부터 매 3개월마다 조기상환청구(풋옵션) 행사가 가능한 구조다. 주가가 전환가액을 하회하는 상황이 지속될 경우 당장 내달 말로 예정된 조기상환 청구일에 투자자 상환 요구가 집중될 수 있다는 분석이다. 문제는 우정바이오의 가용 현금이 넉넉하지 않다는 점이다. 지난해 9월 말 우정바이오의 현금 및 현금성 자산은 약 22억원으로 잔여 CB 원금(35억원)을 상환하기에도 빠듯한 수준이다. 여기에 1년 이내에 만기가 도래하는 단기차입금 규모만 약 164억원에 달해 보유 현금과 상환 예정 부채 간 격차가 큰 상황이다. 추가적인 자금 조달 방안이나 주가 부양을 통한 자본 구조 개선 필요성이 제기되는 이유다. 시가총액 방어 역시 중요한 관리 지표로 떠오르고 있다. 금융당국은 기관투자자 의무보유 확약 확대와 상장폐지 요건 강화를 골자로 한 기업공개(IPO)와 상장폐지 제도 개선 방안을 추진 중이다. 이에 따르면 상장 유지 기준이 3년에 걸쳐 단계적으로 상향된다. 코스닥 시가총액 요건은 올해 150억원, 2027년 200억원을 거쳐 2028년 300억원까지 대폭 높아진 전망이다. 8일 종가 기준 우정바이오의 시가총액은 324억원으로 300억원을 웃돌고 있다. 다만 지난 5일까지만 해도 시가총액이 300억원을 하회하는 구간이 이어지는 등 기준선 인근에서 등락을 반복 중이다. 강화되는 규제 가이드라인에 안정적으로 안착하기 위해 주가 변동성을 낮추고 시가총액을 일정 수준 이상으로 유지하는 게 필수적이라는 지적이다.2026-01-10 06:00:44차지현 기자 -
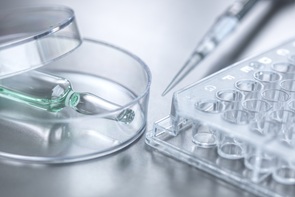 '코스닥 직행 티켓'…비상장 바이오텍 신약 기술수출 약진[데일리팜=차지현 기자] 최근 국내 바이오 업계에서 비상장 기업의 기술수출 약진이 두드러진다. 특히 상당수 기업이 기업공개(IPO)를 앞두고 계약을 성사시키거나 예비심사 청구 직전 성과를 공개하고 있다는 점이 눈에 띈다. 금융당국이 상장 심사 과정에서 기술의 사업화 가능성과 외부 검증 이력을 더욱 중시하는 기조로 전환하면서 이 같은 흐름이 가속화하고 있다는 분석이 나온다. 비상장 바이오사 아보메드·아델, IPO 앞두고 기술수출 성과 공개 9일 바이오 업계에 따르면 희귀·난치성 질환 치료제 개발 바이오 기업 아보메드는 지난 5일 벨기에 소재 상장 제약사 하이로리스(Hyloris Pharmaceuticals SA)와 희귀질환 신약 후보물질 'ARBM-101'의 유럽 지역 권리에 대한 기술수출 계약을 체결했다. 하이로리스는 기존 의약품의 제형 개선·적응증 확장·투여 방식 변경 등을 통해 의료적·상업적 가치를 높이는 데 특화한 업체다. 이번 계약은 윌슨병, 철 과부하(유전성 혈색소 침착증 포함), 원발성 담즙성 담관염(PBC) 등 희귀·난치성 간과 대사질환을 치료 적응증으로 포함한다. 개발 단계에 따른 경상 기술료(마일스톤)를 포함한 총 계약 규모는 최대 1억6000만달러(2300억원)다. 반환 의무가 없는 선급금(업프론트) 규모는 공개하지 않았다. 아보메드는 신약개발과 콤플렉스 제네릭(고난도 복제의약품) 사업을 주력으로 영위하는 업체다. ARBM-101은 체내에 축적된 금속 이온을 선택적으로 결합·배출하는 신규 기전의 저분자 펩타이드 기반 치료제다. 기존 치료제가 구리 배출을 요로에 의존해 부작용 위험이 컸던 것과 달리, 이 물질은 장(腸)을 통한 배출을 유도해 효능과 안전성을 동시에 개선하는 것이 특징이다. 아보메드는 연내 ARBM-101 임상 1상 개시 후 해당 결과를 토대로 후속 글로벌 기술수출을 타진할 계획이다. 이에 앞서 지난달 15일에는 신경퇴행성 질환 신약개발 바이오 기업 아델이 알츠하이머병 치료제 후보물질 'ADEL-Y01'에 대해 글로벌 제약사 사노피와 기술수출 계약을 맺었다. 이 계약은 업프론트 8000만달러(1176억원)을 포함해 최대 10억4000만달러(1조5288억원 규모다. 총 계약 규모 대비 선급금 비중은 약 7.7% 수준이다. 아델은 2016년 울산의대 서울아산병원에서 스핀오프한 업체다. ADEL-Y01은 타우 단백질 가운데 병적 변형 형태인 아세틸화 타우(acK280)를 선택적으로 표적하는 인간화 단일클론 항체다. 기존 알츠하이머 치료제들이 아밀로이드 베타나 전체 타우 단백질을 광범위하게 겨냥한 것과 달리 독성 타우 단백질이 뭉치고 퍼지는 현상만 선택적으로 막으면서, 정상적인 타우 단백질의 기능은 그대로 유지하는 것이 특징이다. ADEL-Y01은 현재 미국 식품의약국(FDA)으로부터 임상시험계획(IND) 승인을 받아 다국가 임상 1상을 진행 중이다. 아델은 후보물질 발굴부터 비임상 연구까지 전 과정을 자체 플랫폼으로 수행했으며, 2020년부터는 오스코텍과 공동 연구개발을 진행해왔다. 최근 기술수출 성과를 낸 아보메드와 아델은 모두 비상장사로 IPO를 추진하고 있다는 공통점이 있다. 아보메드는 올해 상장 전 투자(Pre-IPO) 유치를 완료해 내년 코스닥에 입성하겠다는 목표를 제시했다. 아델 역시 올해 IPO를 재추진할 예정이다. 아델은 지난해 기술성평가에서 BBB·BBB 등급을 받아 상장 요건을 충족하지 못하며 고배를 마신 바 있다. 두 기업 모두 IPO를 앞둔 시점에 기술수출 성과를 공개한 셈이다. 상장 문턱 높아진 바이오…국내 비상장 바이오 줄줄이 기술수출 이 같은 흐름은 일부 기업에 그치지 않는다. 국내 바이오 업계에서 IPO를 앞두고 기술수출 성과를 공개하는 사례가 잇따르고 있다. 최근 2년간 기술수출 성과를 낸 소바젠, 큐어버스, 아이엠바이오로직스, 넥스아이, 진에딧 등이 모두 상장 절차를 준비 중이다. 한국과학기술원(KAIST) 교원 창업기업 소바젠은 지난해 9월 이탈리아 안젤리니 파마와 난치성 뇌전증 신약 후보물질 'SVG105' 관련 기술수출 계약을 맺었다. 계약에 따라 소바젠은 한국, 중국, 대만을 제외한 SVG105 전 세계 개발과 상업화에 대한 독점적 권리를 안젤리니 파마에 이전한다. 계약 규모는 총 5억5000만달러(7500억원)로 업프론트와 마일스톤으로 구성됐다. 소바젠은 올해 하반기 코스닥 입성을 목표로 IPO를 추진 중으로 NH투자증권을 상장 주관사로 선정했다. 또 다른 KAIST 교원 창업기업 큐어버스도 지난 2024년 10월 안젤리니 파마에 경구용 치매 치료제 후보물질 'CV-01'을 이전하는 쾌거를 거뒀다. 계약 규모는 3억7000만달러(5037억원)다. 큐어버스 역시 미래에셋증권을 상장 주관사로 결정, IPO 준비에 착수한 상태다. 항체 신약개발 바이오 기업 아이엠바이오로직스도 IPO를 앞두고 두 건의 기술수출 계약을 연이어 체결했다. 아이엠바이오로직스는 2020년 HK이노엔(전 CJ헬스케어) 바이오부문장 출신 하경식 대표가 창업한 항체 기반 신약개발 바이오 기업으로 지난해 10월 거래소에 코스닥시장 상장 예심 청구서를 제출했다. 앞서 회사는 지난 8월 거래소 지정 전문 평가기관으로부터 각각 A 등급을 획득, 기술특례 상장을 위한 기술성 평가를 통과, 기술특례 상장을 위한 기본 요건을 갖췄다. 아이엠바이오로직스는 2024년 6월 자가면역질환 이중항체 신약 후보물질 'IMB-101'을 미국 네비게이터 메디신에 1조3000억원 규모로 기술수출했다. 이어 2개월 뒤 IMB-101에 대해 중국 화동제약과 4309억원 규모 계약을 맺으며 연이은 기술수출 성과를 거뒀다. 해당 계약은 아이엠바이오로직스가 개발을 주도하고 HK이노엔과 와이바이오로직스가 각각 핵심 기술을 제공한 3자 공동개발 구조로 체결됐다. 로슈 제넨텍과 최대 6억2900만달러(8400억원) 규모 기술수출 계약을 따낸 진에딧도 코스닥 입성을 준비 중이다. 진에딧은 2016년 미국 UC버클리대 바이오공학 박사인 이근우 대표와 박효민 수석부사장이 공동 설립한 캘리포니아 소재 바이오 기업이다. 이 회사는 당초 미국 나스닥 상장을 검토했으나 코스닥 상장으로 방향을 선회, 관련 절차를 밟고 있다. 현재 400억원 규모의 시리즈C 투자 유치를 진행 중으로 투자 마무리 이후 IPO 절차를 본격화한다는 계획이다. 기술수출 성과를 낸 바이오 기업을 중심으로 상장에 성공한 사례도 속속 나오고 있다. 항체약물접합체(ADC) 전문 바이오 기업 에임드바이오도 잇단 기술수출 성과를 발판 삼아 IPO에 성공했다. 에임드바이오는 삼성서울병원 소속 교수가 창업한 신약개발 바이오 기업으로 지난달 4일 기술특례로 코스닥 시장에 데뷔했다. 이 회사는 자체개발 신약개발 플랫폼을 기반으로 설립 후 비교적 단기간에 괄목할 만한 기술이전 성과를 냈다. 에임드바이오는 지난 2024년 말 미국 바이오헤븐에 FGFR3 표적 항암 후보물질 'AMB302'를 기술이전했고 지난해 6월 SK플라즈마와 ROR1 표적 항암 후보물질 'AMB303'에 대해 공동개발·기술이전 계약을 맺었다. 또 지난해 10월 글로벌 제약사 베링거인겔하임과 차세대 ADC 후보물질에 대해 최대 1조4000억원 규모 추가 기술이전 계약을 체결하면서 3종의 전임상 단계 ADC 자산을 모두 이전하는 쾌거를 이뤘다. 리보핵산(RNA) 치환효소 플랫폼 보유 기업 알지노믹스는 지난해 5월 일라이릴리 대상 1조9000억원 규모 기술수출 성과를 확보했다. 해당 계약은 후보물질 도출부터 선급금·연구비·마일스톤·로열티까지 단계별로 발생하는 플랫폼 딜 형태로 알지노믹스는 릴리와 다중 옵션 구조 기술수출 계약을 체결했다. 이 같은 성과에 기반해 알지노믹스는 지난달 18일 기술특례 제도를 통해 코스닥 시장에 입성했다. 작년 2월과 5월 각각 증시에 입성한 오름테라퓨틱과 인투셀도 상장 전 기술수출 성과를 공개했다. 오름테라퓨틱은 2023년 11월 글로벌 빅파마 브리스톨마이어스스큅에 급성골수성백혈병 신약 후보물질 'ORM-6151'에 대한 전체 권리를 양도했다. 이어 2024년 7월 미국 버텍스파마슈티컬스에 자체개발 표적단백질분해제(TPD) 플랫폼 기술수출 계약을 맺었다. 인투셀의 경우 지난 2023년 12월 삼성바이오에피스와 공동연구 계약을 맺었고 2024년 10월 에이비엘바이오에 ADC 플랫폼 기술을 이전했다. 다만 에이비엘바이오 계약은 작년 8월 신규 특허 확보와 제3자 특허 침해 가능성을 이유로 계약 해지 통보를 받았다. 업계에서는 이 같은 변화가 기술특례상장 제도 전반의 심사 기조 변화와 맞닿아 있다고 보고 있다. 최근 금융당국은 신약개발 업체의 상장 요건으로 이전보다 까다로운 기준을 제시하고 있다. 예를 들어 기술성평가 시 상장예비기업의 사업성 항목을 보기 위해 ▲빅파마 또는 나스닥 상장사 대상 기술수출 이력 ▲기술수출 이력이 없을 경우 임상 2상 단계 데이터 등을 요구하고 있다. 물론 기술수출 이력이 있다고 해서 상장이 자동으로 보장되는 것은 아니다. 같은 기술수출이라도 기술이전 상대방의 규모와 신뢰도, 계약 조건의 실질성, 업프론트 비중, 파이프라인 수 등에 따라 심사에서 평가 수준이 크게 달라질 수 있다는 지적이다. 업계 관계자는 "기술수출 이력이 상장 심사에서 중요한 참고 자료로 활용되고 있는 것은 사실"이라면서도 "기술수출이 있다고 해서 상장이 보장되는 것은 아니고, 결국 심사의 출발선에 올라서는 수준에 가깝다"고 했다.2026-01-09 12:14:36차지현 기자
'코스닥 직행 티켓'…비상장 바이오텍 신약 기술수출 약진[데일리팜=차지현 기자] 최근 국내 바이오 업계에서 비상장 기업의 기술수출 약진이 두드러진다. 특히 상당수 기업이 기업공개(IPO)를 앞두고 계약을 성사시키거나 예비심사 청구 직전 성과를 공개하고 있다는 점이 눈에 띈다. 금융당국이 상장 심사 과정에서 기술의 사업화 가능성과 외부 검증 이력을 더욱 중시하는 기조로 전환하면서 이 같은 흐름이 가속화하고 있다는 분석이 나온다. 비상장 바이오사 아보메드·아델, IPO 앞두고 기술수출 성과 공개 9일 바이오 업계에 따르면 희귀·난치성 질환 치료제 개발 바이오 기업 아보메드는 지난 5일 벨기에 소재 상장 제약사 하이로리스(Hyloris Pharmaceuticals SA)와 희귀질환 신약 후보물질 'ARBM-101'의 유럽 지역 권리에 대한 기술수출 계약을 체결했다. 하이로리스는 기존 의약품의 제형 개선·적응증 확장·투여 방식 변경 등을 통해 의료적·상업적 가치를 높이는 데 특화한 업체다. 이번 계약은 윌슨병, 철 과부하(유전성 혈색소 침착증 포함), 원발성 담즙성 담관염(PBC) 등 희귀·난치성 간과 대사질환을 치료 적응증으로 포함한다. 개발 단계에 따른 경상 기술료(마일스톤)를 포함한 총 계약 규모는 최대 1억6000만달러(2300억원)다. 반환 의무가 없는 선급금(업프론트) 규모는 공개하지 않았다. 아보메드는 신약개발과 콤플렉스 제네릭(고난도 복제의약품) 사업을 주력으로 영위하는 업체다. ARBM-101은 체내에 축적된 금속 이온을 선택적으로 결합·배출하는 신규 기전의 저분자 펩타이드 기반 치료제다. 기존 치료제가 구리 배출을 요로에 의존해 부작용 위험이 컸던 것과 달리, 이 물질은 장(腸)을 통한 배출을 유도해 효능과 안전성을 동시에 개선하는 것이 특징이다. 아보메드는 연내 ARBM-101 임상 1상 개시 후 해당 결과를 토대로 후속 글로벌 기술수출을 타진할 계획이다. 이에 앞서 지난달 15일에는 신경퇴행성 질환 신약개발 바이오 기업 아델이 알츠하이머병 치료제 후보물질 'ADEL-Y01'에 대해 글로벌 제약사 사노피와 기술수출 계약을 맺었다. 이 계약은 업프론트 8000만달러(1176억원)을 포함해 최대 10억4000만달러(1조5288억원 규모다. 총 계약 규모 대비 선급금 비중은 약 7.7% 수준이다. 아델은 2016년 울산의대 서울아산병원에서 스핀오프한 업체다. ADEL-Y01은 타우 단백질 가운데 병적 변형 형태인 아세틸화 타우(acK280)를 선택적으로 표적하는 인간화 단일클론 항체다. 기존 알츠하이머 치료제들이 아밀로이드 베타나 전체 타우 단백질을 광범위하게 겨냥한 것과 달리 독성 타우 단백질이 뭉치고 퍼지는 현상만 선택적으로 막으면서, 정상적인 타우 단백질의 기능은 그대로 유지하는 것이 특징이다. ADEL-Y01은 현재 미국 식품의약국(FDA)으로부터 임상시험계획(IND) 승인을 받아 다국가 임상 1상을 진행 중이다. 아델은 후보물질 발굴부터 비임상 연구까지 전 과정을 자체 플랫폼으로 수행했으며, 2020년부터는 오스코텍과 공동 연구개발을 진행해왔다. 최근 기술수출 성과를 낸 아보메드와 아델은 모두 비상장사로 IPO를 추진하고 있다는 공통점이 있다. 아보메드는 올해 상장 전 투자(Pre-IPO) 유치를 완료해 내년 코스닥에 입성하겠다는 목표를 제시했다. 아델 역시 올해 IPO를 재추진할 예정이다. 아델은 지난해 기술성평가에서 BBB·BBB 등급을 받아 상장 요건을 충족하지 못하며 고배를 마신 바 있다. 두 기업 모두 IPO를 앞둔 시점에 기술수출 성과를 공개한 셈이다. 상장 문턱 높아진 바이오…국내 비상장 바이오 줄줄이 기술수출 이 같은 흐름은 일부 기업에 그치지 않는다. 국내 바이오 업계에서 IPO를 앞두고 기술수출 성과를 공개하는 사례가 잇따르고 있다. 최근 2년간 기술수출 성과를 낸 소바젠, 큐어버스, 아이엠바이오로직스, 넥스아이, 진에딧 등이 모두 상장 절차를 준비 중이다. 한국과학기술원(KAIST) 교원 창업기업 소바젠은 지난해 9월 이탈리아 안젤리니 파마와 난치성 뇌전증 신약 후보물질 'SVG105' 관련 기술수출 계약을 맺었다. 계약에 따라 소바젠은 한국, 중국, 대만을 제외한 SVG105 전 세계 개발과 상업화에 대한 독점적 권리를 안젤리니 파마에 이전한다. 계약 규모는 총 5억5000만달러(7500억원)로 업프론트와 마일스톤으로 구성됐다. 소바젠은 올해 하반기 코스닥 입성을 목표로 IPO를 추진 중으로 NH투자증권을 상장 주관사로 선정했다. 또 다른 KAIST 교원 창업기업 큐어버스도 지난 2024년 10월 안젤리니 파마에 경구용 치매 치료제 후보물질 'CV-01'을 이전하는 쾌거를 거뒀다. 계약 규모는 3억7000만달러(5037억원)다. 큐어버스 역시 미래에셋증권을 상장 주관사로 결정, IPO 준비에 착수한 상태다. 항체 신약개발 바이오 기업 아이엠바이오로직스도 IPO를 앞두고 두 건의 기술수출 계약을 연이어 체결했다. 아이엠바이오로직스는 2020년 HK이노엔(전 CJ헬스케어) 바이오부문장 출신 하경식 대표가 창업한 항체 기반 신약개발 바이오 기업으로 지난해 10월 거래소에 코스닥시장 상장 예심 청구서를 제출했다. 앞서 회사는 지난 8월 거래소 지정 전문 평가기관으로부터 각각 A 등급을 획득, 기술특례 상장을 위한 기술성 평가를 통과, 기술특례 상장을 위한 기본 요건을 갖췄다. 아이엠바이오로직스는 2024년 6월 자가면역질환 이중항체 신약 후보물질 'IMB-101'을 미국 네비게이터 메디신에 1조3000억원 규모로 기술수출했다. 이어 2개월 뒤 IMB-101에 대해 중국 화동제약과 4309억원 규모 계약을 맺으며 연이은 기술수출 성과를 거뒀다. 해당 계약은 아이엠바이오로직스가 개발을 주도하고 HK이노엔과 와이바이오로직스가 각각 핵심 기술을 제공한 3자 공동개발 구조로 체결됐다. 로슈 제넨텍과 최대 6억2900만달러(8400억원) 규모 기술수출 계약을 따낸 진에딧도 코스닥 입성을 준비 중이다. 진에딧은 2016년 미국 UC버클리대 바이오공학 박사인 이근우 대표와 박효민 수석부사장이 공동 설립한 캘리포니아 소재 바이오 기업이다. 이 회사는 당초 미국 나스닥 상장을 검토했으나 코스닥 상장으로 방향을 선회, 관련 절차를 밟고 있다. 현재 400억원 규모의 시리즈C 투자 유치를 진행 중으로 투자 마무리 이후 IPO 절차를 본격화한다는 계획이다. 기술수출 성과를 낸 바이오 기업을 중심으로 상장에 성공한 사례도 속속 나오고 있다. 항체약물접합체(ADC) 전문 바이오 기업 에임드바이오도 잇단 기술수출 성과를 발판 삼아 IPO에 성공했다. 에임드바이오는 삼성서울병원 소속 교수가 창업한 신약개발 바이오 기업으로 지난달 4일 기술특례로 코스닥 시장에 데뷔했다. 이 회사는 자체개발 신약개발 플랫폼을 기반으로 설립 후 비교적 단기간에 괄목할 만한 기술이전 성과를 냈다. 에임드바이오는 지난 2024년 말 미국 바이오헤븐에 FGFR3 표적 항암 후보물질 'AMB302'를 기술이전했고 지난해 6월 SK플라즈마와 ROR1 표적 항암 후보물질 'AMB303'에 대해 공동개발·기술이전 계약을 맺었다. 또 지난해 10월 글로벌 제약사 베링거인겔하임과 차세대 ADC 후보물질에 대해 최대 1조4000억원 규모 추가 기술이전 계약을 체결하면서 3종의 전임상 단계 ADC 자산을 모두 이전하는 쾌거를 이뤘다. 리보핵산(RNA) 치환효소 플랫폼 보유 기업 알지노믹스는 지난해 5월 일라이릴리 대상 1조9000억원 규모 기술수출 성과를 확보했다. 해당 계약은 후보물질 도출부터 선급금·연구비·마일스톤·로열티까지 단계별로 발생하는 플랫폼 딜 형태로 알지노믹스는 릴리와 다중 옵션 구조 기술수출 계약을 체결했다. 이 같은 성과에 기반해 알지노믹스는 지난달 18일 기술특례 제도를 통해 코스닥 시장에 입성했다. 작년 2월과 5월 각각 증시에 입성한 오름테라퓨틱과 인투셀도 상장 전 기술수출 성과를 공개했다. 오름테라퓨틱은 2023년 11월 글로벌 빅파마 브리스톨마이어스스큅에 급성골수성백혈병 신약 후보물질 'ORM-6151'에 대한 전체 권리를 양도했다. 이어 2024년 7월 미국 버텍스파마슈티컬스에 자체개발 표적단백질분해제(TPD) 플랫폼 기술수출 계약을 맺었다. 인투셀의 경우 지난 2023년 12월 삼성바이오에피스와 공동연구 계약을 맺었고 2024년 10월 에이비엘바이오에 ADC 플랫폼 기술을 이전했다. 다만 에이비엘바이오 계약은 작년 8월 신규 특허 확보와 제3자 특허 침해 가능성을 이유로 계약 해지 통보를 받았다. 업계에서는 이 같은 변화가 기술특례상장 제도 전반의 심사 기조 변화와 맞닿아 있다고 보고 있다. 최근 금융당국은 신약개발 업체의 상장 요건으로 이전보다 까다로운 기준을 제시하고 있다. 예를 들어 기술성평가 시 상장예비기업의 사업성 항목을 보기 위해 ▲빅파마 또는 나스닥 상장사 대상 기술수출 이력 ▲기술수출 이력이 없을 경우 임상 2상 단계 데이터 등을 요구하고 있다. 물론 기술수출 이력이 있다고 해서 상장이 자동으로 보장되는 것은 아니다. 같은 기술수출이라도 기술이전 상대방의 규모와 신뢰도, 계약 조건의 실질성, 업프론트 비중, 파이프라인 수 등에 따라 심사에서 평가 수준이 크게 달라질 수 있다는 지적이다. 업계 관계자는 "기술수출 이력이 상장 심사에서 중요한 참고 자료로 활용되고 있는 것은 사실"이라면서도 "기술수출이 있다고 해서 상장이 보장되는 것은 아니고, 결국 심사의 출발선에 올라서는 수준에 가깝다"고 했다.2026-01-09 12:14:36차지현 기자 -
![[칼럼] 작년 글로벌 제약 특허 주요 사건과 올해 전망](https://vod.dailypharm.com/new_dailypharm/news/thumbnail/2026/01/09/48d433cb-84c4-4696-b0f2-dd9570b1d37c.jpg) [칼럼] 작년 글로벌 제약 특허 주요 사건과 올해 전망2026년 새해가 시작됐다. 지난해에도 글로벌 제약 특허 분야에서는 제약·바이오 기업의 사업 전략에 직접적인 영향을 미칠 만한 주요 판결과 제도 변화가 잇따랐다. 그중 우리나라 기업들이 특히 주목할 필요가 있는 사건들을 중심으로 살펴본다. 먼저 미국에서는 암젠 대 사노피 판결의 연장선상에 놓일 만한 의미 있는 판단이 나왔다. 2025년 12월 2일, 미국 연방항소법원(CAFC)은 화이자의 자회사 시젠(Seagen)이 일본 다이이찌산쿄(Daiichi Sankyo)를 상대로 제기한 특허침해 소송에서 1심 판결을 뒤집고, 시젠의 특허를 무효로 판단했다. 이 사건은 항암제 엔허투(Enhertu)와 관련된 소송으로, 엔허투는 2024년 기준 약 37억 5천만 달러의 매출을 기록한 블록버스터 의약품이다. 문제 된 특허(U.S. Patent 10808039)는 항체-약물 접합체(ADC)에 관한 것으로, 청구항 제1항을 간략히 표현하면 ‘항체–링커–펩타이드–약물’ 구조의 ADC를 포괄적으로 청구하고 있었다. CAFC는 이 특허가 두 가지 측면에서 요건을 충족하지 못했다고 판단했다. 첫 번째는 명세서 기재요건(Written Description) 불비다. 해당 청구항에서 펩타이드 부분(Ww)은 글리신(Gly)과 페닐알라닌(Phe)으로 구성된 테트라펩타이드를 의미하며, 이론적으로 81가지 조합이 가능하다. 그러나 특허 명세서에는 Gly·Phe로 구성된 테트라펩타이드가 단 하나도 특정되지 않은 채, 아미노산이 2개부터 12개까지 연결된 약 47만 개 이상의 펩타이드가 가능하다는 수준의 일반적 기재만 존재했다. 법원은 ‘81’이라는 수가 ‘47만’이라는 범위에 비해 극히 제한적이며, 명세서가 Gly·Phe 테트라펩타이드라는 특정 아종(subgenus)을 충분히 개시하지 못했다고 판단했다. 두 번째는 실시가능성(Enablement) 요건 불비다. 청구항에서 약물 부분은 임의의 약물로 정의돼 있어, 결과적으로 ‘세포 내에서 절단 가능한 모든 ADC’를 포괄하게 된다. 하지만 명세서에는 이를 가능하게 하는 공통의 구조적 특징이나 원리가 제시돼 있지 않았다. 이로 인해 연구자가 발명을 실시하기 위해서는 개별 접합체를 하나씩 시험해야 하는 과도한 실험이 요구된다고 봤다. 이는 암젠 대 사노피 판결에서 문제 삼았던 논리와 궤를 같이한다. 그 결과 해당 특허는 모든 청구항이 무효로 판단됐다. 최근 미국 특허 판례를 보면 ‘개시한 것’과 ‘청구한 것’ 사이의 간극이 큰 특허는 과거보다 훨씬 쉽게 무효되는 경향이 뚜렷하다. 청구항이 반드시 실시예에 한정될 필요는 없지만, 개시 범위를 현저히 넘어서는 과도한 확장은 리스크로 작용한다. 특히 개별 특허의 사업적 가치가 큰 제약·바이오 분야에서는, 청구항 수가 다소 늘어나더라도 넓은 범위부터 좁은 범위까지 단계적으로 구성하는 전략이 상대적으로 유리해 보인다. 2025년에는 유럽에서도 주목할 만한 사건이 있었다. 유럽 바이오시밀러 업계에 큰 파장을 일으킨 아일리아(애플리버셉트) 특허 분쟁이다. 독일 뮌헨 지역법원은 2025년 10월, 리제네론·바이엘의 아일리아 바이오시밀러인 포미콘(Formycon)의 FYB203이 리제네론의 조성물 특허(EP 2364691)를 침해했다며, 유럽 20개국을 대상으로 한 다국가 특허침해 금지명령(Cross-border Injunction)을 내렸다. 주목할 점은 이 판결이 유럽통합특허법원(UPC)이 아닌 독일 지방법원에서 내려졌다는 점이다. 해당 특허는 이미 UPC 관할에서 옵트아웃(opt-out)된 상태였지만, 유럽사법재판소(CJEU)가 2025년 2월 25일 선고한 C-339/22 판결 취지에 따라, 피고가 소재한 EU 회원국 법원이 국경을 넘는 관할권을 인정한 것이다. 이제 유럽에서 다국가 특허소송을 검토할 때는 UPC와 함께 CJEU 체제까지 동시에 고려하는 것이 필요해졌다. UPC는 참여국 전체에서 특허를 일괄 무효로 만들 수 있는 반면, CJEU 체제에서는 중앙 무효 판단이 불가능하다. 아일리아 사례에서 보듯, 이는 기업 입장에서 중요한 전략적 판단 요소가 된다. UPC 출범 이후 유럽 특허소송은 CJEU, 개별국 법원, UPC가 얽힌 복합적인 전략 구도로 전개되고 있다. 이밖에도 미국에서는 제약사 테바(Teva)가 연방거래위원회(FTC)의 압박 속에 2025년 12월, 부적절하게 등록된 200건이 넘는 특허를 오렌지북에서 삭제하는 디리스팅(de-listing)을 단행했다. 유럽에서는 데이터 독점기간 단축과 볼라 예외(Bolar exemption) 확대를 골자로 한 제약 패키지법(Pharma Package)이 EU 의회를 통과했다. 2026년 역시 변화의 속도는 늦춰지지 않을 전망이다. 2026년부터 2028년까지 주요 블록버스터 의약품의 특허 만료가 본격화되는 특허절벽이 가시화되고 있으며, AI를 활용한 발명이 빠르게 늘어날 것으로 예상된다. 미국 인플레이션 감축법(IRA)의 영향으로 의약품 포트폴리오가 저분자 화합물에서 바이오의약품으로 이동하는 흐름도 점차 뚜렷해지고 있다. 변화는 늘 반복돼 왔다. 다만 그 변화의 방향과 속도는 점점 더 복잡해지고 있다. 2026년이 우리 제약·바이오 기업들에게 또 하나의 도전이자 기회의 해가 되기를 기대해본다.2026-01-09 12:12:50데일리팜
[칼럼] 작년 글로벌 제약 특허 주요 사건과 올해 전망2026년 새해가 시작됐다. 지난해에도 글로벌 제약 특허 분야에서는 제약·바이오 기업의 사업 전략에 직접적인 영향을 미칠 만한 주요 판결과 제도 변화가 잇따랐다. 그중 우리나라 기업들이 특히 주목할 필요가 있는 사건들을 중심으로 살펴본다. 먼저 미국에서는 암젠 대 사노피 판결의 연장선상에 놓일 만한 의미 있는 판단이 나왔다. 2025년 12월 2일, 미국 연방항소법원(CAFC)은 화이자의 자회사 시젠(Seagen)이 일본 다이이찌산쿄(Daiichi Sankyo)를 상대로 제기한 특허침해 소송에서 1심 판결을 뒤집고, 시젠의 특허를 무효로 판단했다. 이 사건은 항암제 엔허투(Enhertu)와 관련된 소송으로, 엔허투는 2024년 기준 약 37억 5천만 달러의 매출을 기록한 블록버스터 의약품이다. 문제 된 특허(U.S. Patent 10808039)는 항체-약물 접합체(ADC)에 관한 것으로, 청구항 제1항을 간략히 표현하면 ‘항체–링커–펩타이드–약물’ 구조의 ADC를 포괄적으로 청구하고 있었다. CAFC는 이 특허가 두 가지 측면에서 요건을 충족하지 못했다고 판단했다. 첫 번째는 명세서 기재요건(Written Description) 불비다. 해당 청구항에서 펩타이드 부분(Ww)은 글리신(Gly)과 페닐알라닌(Phe)으로 구성된 테트라펩타이드를 의미하며, 이론적으로 81가지 조합이 가능하다. 그러나 특허 명세서에는 Gly·Phe로 구성된 테트라펩타이드가 단 하나도 특정되지 않은 채, 아미노산이 2개부터 12개까지 연결된 약 47만 개 이상의 펩타이드가 가능하다는 수준의 일반적 기재만 존재했다. 법원은 ‘81’이라는 수가 ‘47만’이라는 범위에 비해 극히 제한적이며, 명세서가 Gly·Phe 테트라펩타이드라는 특정 아종(subgenus)을 충분히 개시하지 못했다고 판단했다. 두 번째는 실시가능성(Enablement) 요건 불비다. 청구항에서 약물 부분은 임의의 약물로 정의돼 있어, 결과적으로 ‘세포 내에서 절단 가능한 모든 ADC’를 포괄하게 된다. 하지만 명세서에는 이를 가능하게 하는 공통의 구조적 특징이나 원리가 제시돼 있지 않았다. 이로 인해 연구자가 발명을 실시하기 위해서는 개별 접합체를 하나씩 시험해야 하는 과도한 실험이 요구된다고 봤다. 이는 암젠 대 사노피 판결에서 문제 삼았던 논리와 궤를 같이한다. 그 결과 해당 특허는 모든 청구항이 무효로 판단됐다. 최근 미국 특허 판례를 보면 ‘개시한 것’과 ‘청구한 것’ 사이의 간극이 큰 특허는 과거보다 훨씬 쉽게 무효되는 경향이 뚜렷하다. 청구항이 반드시 실시예에 한정될 필요는 없지만, 개시 범위를 현저히 넘어서는 과도한 확장은 리스크로 작용한다. 특히 개별 특허의 사업적 가치가 큰 제약·바이오 분야에서는, 청구항 수가 다소 늘어나더라도 넓은 범위부터 좁은 범위까지 단계적으로 구성하는 전략이 상대적으로 유리해 보인다. 2025년에는 유럽에서도 주목할 만한 사건이 있었다. 유럽 바이오시밀러 업계에 큰 파장을 일으킨 아일리아(애플리버셉트) 특허 분쟁이다. 독일 뮌헨 지역법원은 2025년 10월, 리제네론·바이엘의 아일리아 바이오시밀러인 포미콘(Formycon)의 FYB203이 리제네론의 조성물 특허(EP 2364691)를 침해했다며, 유럽 20개국을 대상으로 한 다국가 특허침해 금지명령(Cross-border Injunction)을 내렸다. 주목할 점은 이 판결이 유럽통합특허법원(UPC)이 아닌 독일 지방법원에서 내려졌다는 점이다. 해당 특허는 이미 UPC 관할에서 옵트아웃(opt-out)된 상태였지만, 유럽사법재판소(CJEU)가 2025년 2월 25일 선고한 C-339/22 판결 취지에 따라, 피고가 소재한 EU 회원국 법원이 국경을 넘는 관할권을 인정한 것이다. 이제 유럽에서 다국가 특허소송을 검토할 때는 UPC와 함께 CJEU 체제까지 동시에 고려하는 것이 필요해졌다. UPC는 참여국 전체에서 특허를 일괄 무효로 만들 수 있는 반면, CJEU 체제에서는 중앙 무효 판단이 불가능하다. 아일리아 사례에서 보듯, 이는 기업 입장에서 중요한 전략적 판단 요소가 된다. UPC 출범 이후 유럽 특허소송은 CJEU, 개별국 법원, UPC가 얽힌 복합적인 전략 구도로 전개되고 있다. 이밖에도 미국에서는 제약사 테바(Teva)가 연방거래위원회(FTC)의 압박 속에 2025년 12월, 부적절하게 등록된 200건이 넘는 특허를 오렌지북에서 삭제하는 디리스팅(de-listing)을 단행했다. 유럽에서는 데이터 독점기간 단축과 볼라 예외(Bolar exemption) 확대를 골자로 한 제약 패키지법(Pharma Package)이 EU 의회를 통과했다. 2026년 역시 변화의 속도는 늦춰지지 않을 전망이다. 2026년부터 2028년까지 주요 블록버스터 의약품의 특허 만료가 본격화되는 특허절벽이 가시화되고 있으며, AI를 활용한 발명이 빠르게 늘어날 것으로 예상된다. 미국 인플레이션 감축법(IRA)의 영향으로 의약품 포트폴리오가 저분자 화합물에서 바이오의약품으로 이동하는 흐름도 점차 뚜렷해지고 있다. 변화는 늘 반복돼 왔다. 다만 그 변화의 방향과 속도는 점점 더 복잡해지고 있다. 2026년이 우리 제약·바이오 기업들에게 또 하나의 도전이자 기회의 해가 되기를 기대해본다.2026-01-09 12:12:50데일리팜 -
 에버엑스, CES 2026 CTA 수상…글로벌 헬스케어 가시화[데일리팜=황병우 기자]에버엑스(EverEx)는 세계 최대 기술 박람회 CES2026에서 CTA(Consumer Technology Association)가 주최한 'CTA Foundation Pitch Competition'에서 최종 수상 기업으로 선정됐다고 9일 밝혔다. CTA Foundation Pitch Competition은 CES 주관사인 CTA가 직접 운영하는 공식 프로그램으로, 전 세계 유망 기업들이 대거 참여하는 높은 경쟁률의 글로벌 피치 무대다. 기술 혁신성뿐 아니라 사업 확장성, 사회적 임팩트, 접근성, 실제 시장 적용 가능성을 종합적으로 평가해 소수의 기업만을 최종 수상 기업으로 선정한다. 이번 선정은 에버엑스의 AI 기반 맞춤형 디지털 재활 솔루션과 보험 청구가 가능한 원격치료 모니터링(RTM) 사업 모델이 기술 시연을 넘어 의료 현장에서 검증 가능한 디지털 헬스 솔루션이라는 점에서 글로벌 심사위원단의 높은 평가를 받은 결과다 또 회사는 CES 2026에 미국 은퇴자연합(AARP)의 AgeTech Collaborative(ATC) 파트너 기업 자격으로 공식 부스를 운영하는 등 고령층 및 만성 근골격계 질환자를 위한 디지털 헬스 솔루션을 글로벌 시장에 선보였다. 전시 기간 동안 미국 및 글로벌 의료기관, 헬스케어 기업, 의료기기 기업들과의 협력 논의와 파트너십 성과를 도출하며 사업 확장 가능성을 구체화했다. 아울러 에버엑스는 이번 CES 2026에서 모라케어 (MORA Care) 제품으로 'CES Innovation Awards Digital Health' 부문에도 선정되며, 디지털 헬스 분야에서의 기술 혁신성과 근골격계 질환 예방/관리 적용 가능성을 추가로 입증했다. 이와 함께 에버엑스는 CES 현장에서 ‘IP R&D 성과 글로벌 확산 우수기업’으로도 선정됐다. 이번 수상은 한국특허전략개발원장이 에버엑스 부스를 직접 방문해 상을 수여한 것으로, AI 동작분석 및 데이터 기반 재활 기술을 중심으로 한 지식재산(IP) 전략과 글로벌 사업 확장 성과를 공식적으로 인정받았다. 윤찬 에버엑스 대표이사는 "CES 주관사 CTA가 직접 주최한 Pitch Competition 수상은 글로벌 무대에서 에버엑스의 기술력과 사업성이 함께 검증된 결과"라며 "앞으로도 실제 의료 현장에서 가치를 만드는 디지털 재활 솔루션으로 글로벌 시장을 확대해 나가겠다"고 밝혔다.2026-01-09 10:43:19황병우 기자
에버엑스, CES 2026 CTA 수상…글로벌 헬스케어 가시화[데일리팜=황병우 기자]에버엑스(EverEx)는 세계 최대 기술 박람회 CES2026에서 CTA(Consumer Technology Association)가 주최한 'CTA Foundation Pitch Competition'에서 최종 수상 기업으로 선정됐다고 9일 밝혔다. CTA Foundation Pitch Competition은 CES 주관사인 CTA가 직접 운영하는 공식 프로그램으로, 전 세계 유망 기업들이 대거 참여하는 높은 경쟁률의 글로벌 피치 무대다. 기술 혁신성뿐 아니라 사업 확장성, 사회적 임팩트, 접근성, 실제 시장 적용 가능성을 종합적으로 평가해 소수의 기업만을 최종 수상 기업으로 선정한다. 이번 선정은 에버엑스의 AI 기반 맞춤형 디지털 재활 솔루션과 보험 청구가 가능한 원격치료 모니터링(RTM) 사업 모델이 기술 시연을 넘어 의료 현장에서 검증 가능한 디지털 헬스 솔루션이라는 점에서 글로벌 심사위원단의 높은 평가를 받은 결과다 또 회사는 CES 2026에 미국 은퇴자연합(AARP)의 AgeTech Collaborative(ATC) 파트너 기업 자격으로 공식 부스를 운영하는 등 고령층 및 만성 근골격계 질환자를 위한 디지털 헬스 솔루션을 글로벌 시장에 선보였다. 전시 기간 동안 미국 및 글로벌 의료기관, 헬스케어 기업, 의료기기 기업들과의 협력 논의와 파트너십 성과를 도출하며 사업 확장 가능성을 구체화했다. 아울러 에버엑스는 이번 CES 2026에서 모라케어 (MORA Care) 제품으로 'CES Innovation Awards Digital Health' 부문에도 선정되며, 디지털 헬스 분야에서의 기술 혁신성과 근골격계 질환 예방/관리 적용 가능성을 추가로 입증했다. 이와 함께 에버엑스는 CES 현장에서 ‘IP R&D 성과 글로벌 확산 우수기업’으로도 선정됐다. 이번 수상은 한국특허전략개발원장이 에버엑스 부스를 직접 방문해 상을 수여한 것으로, AI 동작분석 및 데이터 기반 재활 기술을 중심으로 한 지식재산(IP) 전략과 글로벌 사업 확장 성과를 공식적으로 인정받았다. 윤찬 에버엑스 대표이사는 "CES 주관사 CTA가 직접 주최한 Pitch Competition 수상은 글로벌 무대에서 에버엑스의 기술력과 사업성이 함께 검증된 결과"라며 "앞으로도 실제 의료 현장에서 가치를 만드는 디지털 재활 솔루션으로 글로벌 시장을 확대해 나가겠다"고 밝혔다.2026-01-09 10:43:19황병우 기자 -
 의협 "의대증원 추진 문제 있다"...감사원에 감사청구[데일리팜=강신국 기자] 의사단체가 복지부의 의대정원 추진 과정에 문제가 있다며 감사원에 공익감사를 청구했다. 대한의사협회(회장 김택우)는 9일 지난해 11월 감사원이 지적한 의대 정원 증원 추진 과정의 위법·부당성에도 불구하고, 복지부가 이를 전혀 시정하지 않은 채 2027년도 정원 결정을 강행하고 있다며 공익감사 청구 배경을 설명했다. 의협에 따르면 보건의료기본법 제23조의2에 따르면 보건의료인력 수급 추계 시에는 반드시 '지역 단위 수급 추계'와 '전문과목 및 진료과목별 수급 추계'를 분석하고 반영해야 하지만 수급추계위원회는 이러한 세부 분석을 생략하거나 형식적으로 처리한 채, 전체 총량 중심의 수치만을 발표했고 이는 명백한 직무유기이자 법치주의 훼손이라는 것이다. 의협은 "보건의료정책심의위원회(보정심)가 불충분한 추계를 토대로 또다시 졸속 의결을 시도하고 있다"며 "현재 보정심은 앞서 언급한 수급추계위의 부실한 결과를 면밀히 검증하기는커녕, 시간에 쫓겨 기계적으로 인용해 2027년 정원을 확정하려는 데 이는 충분한 논의와 과학적 근거에 기반하라는 감사원의 지적 사항을 정면으로 위배하는 것으로 감사원의 권위를 묵살하는 행정 폭거"라고 주장했다. 아울러 "보정심의 인적 구성 또한 감사원의 시정 요구를 외면하고 있다"며 "정부는 제5기 보정심을 출범시키면서, 정부 중심의 위원 구성을 쇄신하지 않았다. 편향된 인적 구성 위에서, 부실한 데이터를 근거로, 시간에 쫓겨 내리는 결정은 원천 무효일 수밖에 없다"고 지적했다. 의협은 "잘못된 진단 위에서 올바른 처방이 나올 수 없듯이, 위법하고 부실한 추계 위에서 수립된 의대 증원 정책은 실패할 수밖에 없다"며 "이번 공익감사 청구를 통해 정부의 감사 결과 미이행과 습관적 위법 행정에 대해 엄중한 책임을 묻겠다. 감사원은 정부가 자신들의 지적 사항조차 이행하지 않는 작금의 사태를 직시하고, 즉각적이고 철저한 감사를 실시해야 한다"고 촉구했다.2026-01-09 09:49:05강신국 기자
의협 "의대증원 추진 문제 있다"...감사원에 감사청구[데일리팜=강신국 기자] 의사단체가 복지부의 의대정원 추진 과정에 문제가 있다며 감사원에 공익감사를 청구했다. 대한의사협회(회장 김택우)는 9일 지난해 11월 감사원이 지적한 의대 정원 증원 추진 과정의 위법·부당성에도 불구하고, 복지부가 이를 전혀 시정하지 않은 채 2027년도 정원 결정을 강행하고 있다며 공익감사 청구 배경을 설명했다. 의협에 따르면 보건의료기본법 제23조의2에 따르면 보건의료인력 수급 추계 시에는 반드시 '지역 단위 수급 추계'와 '전문과목 및 진료과목별 수급 추계'를 분석하고 반영해야 하지만 수급추계위원회는 이러한 세부 분석을 생략하거나 형식적으로 처리한 채, 전체 총량 중심의 수치만을 발표했고 이는 명백한 직무유기이자 법치주의 훼손이라는 것이다. 의협은 "보건의료정책심의위원회(보정심)가 불충분한 추계를 토대로 또다시 졸속 의결을 시도하고 있다"며 "현재 보정심은 앞서 언급한 수급추계위의 부실한 결과를 면밀히 검증하기는커녕, 시간에 쫓겨 기계적으로 인용해 2027년 정원을 확정하려는 데 이는 충분한 논의와 과학적 근거에 기반하라는 감사원의 지적 사항을 정면으로 위배하는 것으로 감사원의 권위를 묵살하는 행정 폭거"라고 주장했다. 아울러 "보정심의 인적 구성 또한 감사원의 시정 요구를 외면하고 있다"며 "정부는 제5기 보정심을 출범시키면서, 정부 중심의 위원 구성을 쇄신하지 않았다. 편향된 인적 구성 위에서, 부실한 데이터를 근거로, 시간에 쫓겨 내리는 결정은 원천 무효일 수밖에 없다"고 지적했다. 의협은 "잘못된 진단 위에서 올바른 처방이 나올 수 없듯이, 위법하고 부실한 추계 위에서 수립된 의대 증원 정책은 실패할 수밖에 없다"며 "이번 공익감사 청구를 통해 정부의 감사 결과 미이행과 습관적 위법 행정에 대해 엄중한 책임을 묻겠다. 감사원은 정부가 자신들의 지적 사항조차 이행하지 않는 작금의 사태를 직시하고, 즉각적이고 철저한 감사를 실시해야 한다"고 촉구했다.2026-01-09 09:49:05강신국 기자 -
 끝없는 재평가 수난과 소송전...제약사들의 복잡한 병오년[데일리팜=천승현 기자] 올해 제약사들은 정부 규제 후유증으로 혹독한 시험대에 오를 전망이다. 알포세레이트(콜린제제)의 임상재평가가 막바지로 향하면서 생존 여부와 막대한 환수에 대한 윤곽이 조금씩 드러날 것으로 예상된다. 제약사 수십곳이 연루된 애엽 추출물의 급여재평가도 초미의 관심사다. GMP 적합판정 취소와 보툴리눔독소제제 허가취소 처분에 대한 소송전 결과에 따라 제약업계 전반에 막대한 영향을 미칠 예정이다. 콜린제제 임상재평가 종료 임박...임상 실패시 대규모 환수·집단 소송 불가피 9일 업계에 따르면 올해부터 콜린제제의 임상재평가가 순차적으로 종료될 예정이다. 콜린제제의 임상재평가는 종근당과 대웅바이오의 주도로 진행 중이다. 종근당이 퇴행성 경도인지장애와 혈관성 경도인지장애 임상시험을 각각 수행하고, 대웅바이오가 치매 환자 대상 임상시험을 진행하는 방식이다. 종근당이 진행하는 경도인지장애 환자 대상 임상시험의 경우 종료시한이 3년 9개월로 설정됐다. 대웅바이오의 알츠하이머 환자 대상 임상시험의 경우 4년 6개월 이내에 마무리해야 한다. 당초 종근당의 혈관성 경도인지장애의 재평가 임상시험은 올해 3월 종료가 예정됐는데 내년 6월로 결과보고서 제출기한이 연장됐다. 퇴행성 경도인지장애 재평가 임상의 경우 2027년 3월로 종료 시기가 연장됐다. 대웅바이오의 알츠하이머 임상시험은 2027년 10월이 종료 기한으로 지정됐다. 콜린제제의 임상재평가 결과는 국내 제약업계 전반에 걸쳐 막대한 후폭풍을 가져올 수 있다. 만약 임상재평가가 실패로 결론나면 연간 6000억원 규모의 처방액 손실과 함께 초유의 수천억원 규모 환수 리스크가 현실화하기 때문이다. 지난 2020년 12월 보건복지부는 국민건강보험공단에 콜린제제를 보유한 업체들에 '임상시험에 실패할 경우 처방액을 반환하라‘는 내용의 요양급여계약을 명령했다. 협상 명령 8개월만에 제약사들은 콜린제제의 재평가 임상 실패로 최종적으로 적응증이 삭제될 경우 임상시험 계획서를 승인받은 날부터 삭제일까지 처방액의 20%를 건보공단에 돌려주겠다고 합의했다. 의약품 조사기관 유비스트에 따르면 지난 2024년 콜린제제의 외래 처방시장 규모는 6123억원이다. 만약 콜린제제 임상시험 계획 승인 이후 5년간 진행한 임상시험이 실패할 경우 제약사들의 환수 금액은 5000억원 이상으로 추산된다. 제약사들은 콜린제제의 임상재평가가 끝나지 않았는데도 이미 임상 실패를 가정한 부채를 인식한 상황이다. 종근당, 대웅바이오, 한미약품, 알리코제약, 동구바이오제약, 국제약품, 동광약품, 경동제약, 제뉴파마, 동국제약, 환인제약 등이 콜린제제를 판매 중인 주요 업체들이 많게는 수백억원 규모의 환수 금액 추정치를 미리 부채 항목 등에 반영했다. 제약사들은 환수를 저지하기 위해 전방위 소송전을 전개하고 있지만 좀처럼 승기를 잡지 못하는 상황이다. 복지부의 환수협상 명령 이후 제약사들은 협상 명령이 무효라는 행정소송을 일제히 제기했다. 제약사들은 1차 협상 명령과 2차 협상 명령에 대해 각각 2개 그룹으로 나눠 총 4건의 소송을 청구했는데 지난해 대법원까지 모두 패소했다. 제약사들은 지난 2024년 콜린제제 환수협상 계약은 무효라는 내용의 행정소송을 추가로 제기했다. 법무법인 세종이 종근당 등 24곳의 사건을 맡았고 법무법인 광장이 대웅바이오 등 13곳의 소송을 대리했다. 종근당 등은 지난해 9월 패소했고 대웅바이오 등은 작년 12월 기각 판결을 받았다. 콜린제제의 임상재평가는 임상시험이 종료되는 적응증별로 퇴출 여부가 결정될 가능성이 크다. 뇌질환 치료제 아세틸엘카르니틴은 적응증별로 임상재평가 결론이 도출됐다. 지난 2013년 식약처는 아세틸엘카르니틴제제에 대한 임상재평가를 지시했다. 재평가 임상은 적응증에 따라 ’일차적 퇴행성 질환‘과 ’뇌혈관 질환에 의한 이차적 퇴행성 질환‘ 2개 그룹으로 나눠 진행됐다. 임상시험 결과 지난 2019년 7월 일차적 퇴행성 질환을 입증하지 못해 해당 적응증이 삭제됐다. 2021년 8월에는 ‘뇌혈관 질환에 의한 이차적 퇴행성 질환’도 유효성을 입증하지 못한 것으로 결론났다. 아세틸엘카르니틴은 임상재평가 실패로 인한 처방액 환수 조항이 없어 시장 퇴출에서 마무리됐다. 제약사들은 콜린제제의 임상실패시 보건당국이 환수금액을 청구하더라도 또 다시 소송전이 펼쳐질 수 밖에 없다. 제약사들은 콜린제제의 허가가 유효한 상황에서 재평가 임상시험 실패로 막대한 금액을 부담하는 것은 납득하기 어렵다는 인식이 팽배하다. 제약사들은 올해 콜린제제의 급여축소에 따른 손실도 대비해야 하는 처지다. 복지부는 2020년 8월 콜린제제의 새로운 급여 기준 내용을 담은 ‘요양급여의 적용기준 및 방법에 관한 세부사항’ 일부 개정고시를 발령했다. 치매 진단을 받지 않은 환자가 콜린제제를 사용할 경우 약값 부담률을 30%에서 80%로 올리는 내용이다. 제약사들은 콜린제제 급여 축소의 부당함을 따지는 취소 소송을 제기했지만 지난해 최종 패소했다. 업계에서는 처방 현장에서 환자들의 콜린제제 약값 부담 2.7배 상승하면 처방 기피 현상이 발생할 수 있다는 우려가 커지는 실정이다. 실제로 콜린제제의 급여 축소는 지난해 9월 21일부터 적용됐는데 작년 10월 처방시장 규모는 333억원으로 전년동기보다 37.3% 감소했고 전월 대비 33.9% 축소됐다. 제약사들은 콜린제제의 약값이 저렴한 수준이어서 급여 축소 이후에도 기존에 만족도가 높은 의료진과 환자들을 중심으로 급격한 처방 중단으로 이어지지 않을 것으로 기대하는 모습이다. 애엽 추출물 첫 1천억대 급여재평가 탈락 가능성...제네릭 동등성 재평가도 영향 촉각 제약사들은 올해 애엽 추출물 위염치료제의 생존에 큰 관심을 기울인다. 40여개 업체가 애엽 추출물을 파는데다 제네릭의 동등성 재평가 성패에도 영향을 미친다. 애엽 성분 의약품은 쑥을 기반으로 만드는 천연물의약품이다. 동아에스티의 ‘스티렌’이 오리지널 제품으로 급성위염과 만성위염의 위점막 병변, 출혈, 발적, 부종 등의 개선에 사용된다. 건강보험심사평가원은 지난해 8월 약제급여평가위원회에서 심의한 결과 애엽 추출물에 대해 임상적 유용성 근거가 없다는 이유로 급여 적정성이 없다는 결론을 내렸다. 제약사들은 급여 재평가 결과를 수용할 수 없다며 이의신청을 제기했고 심평원은 ‘비용효과성 충족시 급여적정성 있음’이라는 결론을 내렸다. 애엽 추출물의 약가 인하에 합의한 제품에 대해 비용 효과성이 인정된다는 판단으로 급여 잔류를 결정했다. 하지만 지난해 12월 건강보험정책심의위원회는 애엽 추출물의 급여재평가 결론을 보류했다. 추가 검토 필요성이 제기됐다는 이유에서다. 당초 이달부터 애엽 추출물 성분 의약품 74종의 보험상한가가 평균 14.3% 인하되는 절충안이 예고됐지만 건정심에서는 이 안건을 다루지 않았다. 애엽 추출물은 지난 2024년 1298억원의 외래 처방시장을 형성했다. 급여 삭제시 연간 1000억원 이상의 수익이 증발하는 셈이다. 지난 2021년부터 급여재평가 결과 빌베리건조엑스, 스트렙토키나제·스트렙토도르나제, 옥시라세탐, 아세틸엘카르니틴, 이토프리드 등이 전 제품 급여 삭제가 결정됐는데 모두 연간 처방액이 1000억원 미만이었다. 애엽추출물은 용량과 제조법에 따라 총 4종류가 있는데 평균 약가는 107원, 124원, 186원, 205원이다. 4종류의 애엽추출물이 비슷하게 처방됐다고 가정하면 지난해에만 총 8억개 이상이 처방됐다는 계산이 나온다. 국민 1인당 15개 이상 처방받는 '국민 위염약'이 퇴출 기로에 놓인 셈이다. 만약 애엽추출물이 약가인하를 조건으로 급여목록에 잔류하더라도 제약사들은 대규모 손실이 예고됐다. 당초 약가 인하 대상 애엽 추출물 74개 품목은 지난해 4분기부터 올해 3분기까지 최근 1년 간 총 1066억원의 처방금액을 합작했다. 약가인하 제품들의 인하율을 적용하면 연간 152억원의 손실이 발생하는 것으로 추산됐다. 애엽에탄올연조엑스 성분 제네릭 제품들은 급여재평가를 통과하더라도 시장 잔류를 위한 또 다른 시험대에 오른다. 제약사 50여곳은 지난 6월 말 식품의약품안전처에 애엽 성분 위염치료제의 임상시험 계획서를 제출했다. 오리지널 의약품 스티렌과 스티렌투엑스를 각각 대조약으로 위염치료제 효능을 비교하는 내용의 임상시험이다. 식약처의 동등성 재평가 지시에 따른 임상시험 수행 계획이다. 제약사들은 동등성 재평가 대상 애엽 추출물 의약품을 스티렌과 스티렌투엑스와 각각 비교 임상시험하는 방식으로 동등성을 입증할 계획이다. 생약제제 특성상 유효 성분의 혈중농도를 비교하는 생물학적동등성시험으로 동등성을 입증하기 어렵다는 이유에서다. 스티렌과 스티렌투엑스 제네릭 제품들은 비교 용출과 비교 붕해 방식으로 허가받았다. 만약 애엽추출물의 급여 탈락이 결정되면 제약사들이 추진 중인 동등성 재평가 임상시험도 동력을 상실할 공산이 크다. GMP 적합판정 취소 행정소송 업계 파장 예의주시...보툴리눔 처분 소송도 종착지 임박 정부의 제조·품질관리기준(GMP) 적합판정서 취소 처분에 대한 행정소송도 올해 제약업계의 큰 관심사로 지목된다. 제약사들이 주장하는 GMP 적합판정 취소 처분의 부당성에 대해 법원이 결론을 내릴 전망이다. 한국휴텍스제약과 동구바이오제약은 피해금액이 크고 다른 기업들과 활발한 위수탁 관계를 맺고 있어 처분 패소시 제약업계 전반에 영향을 미칠 수 있다. 2022년 12월부터 GMP 적합판정을 거짓·부정하게 받거나 반복적으로 의약품 제조·품질관리에 관한 기록을 거짓으로 작성해 판매한 사실이 적발된 경우 GMP 적합판정을 취소하는 일명 'GMP 원스트라이크 아웃'이 도입됐다. 식품의약품안전처는 2023년 7월 휴텍스제약이 6개 제품을 제조하는 과정에서 첨가제를 임의로 증량하거나 감량해 허가 사항과 다르게 제조하고, 제조기록서를 거짓 작성하는 등의 위반 사실을 확인하고 GMP 적합판정 취소 처분을 결정했다. 휴텍스제약은 GMP 적합판정 취소 처분 취소소송을 제기했지만 지난해 1월 패소 판결을 받았고 현재 항소심이 진행 중이다. 휴텍스제약은 일시적으로 GMP 적합판정 취소 처분의 효력이 발생하면서 막대한 손실이 현실화한 상태다. 당초 휴텍스제약이 제기한 처분 집행정지 결정의 지연과 기각으로 2024년 2월 1일부터 지난 3월 4일까지 33일 동안 처분 효력이 발생했다. 휴텍스제약은 작년 상반기 외래 처방금액은 624억원으로 2023년 상반기 1581억원과 비교하면 2년새 60.5% 줄었다. 동구바이오제약의 GMP 적합판정 취소 처분은 위탁사들의 영업 활동에도 영향을 미칠 전망이다. 식약처는 2024년 8월 동구바이오제약의 내용고형제 제조시설에 대해 GMP 적합 판정 취소 처분을 통보했다. 식약처는 동구바이오제약이 해열진통제 록소리스정과 당뇨치료제 글리파엠정을 생산하는 과정에서 첨가제 등을 임의로 변경해 허가사항과 다르게 제조하고 제조기록서에는 허가사항과 동일하게 제조한 것처럼 거짓 작성했다고 판단했다. 동구바이오제약은 2024년 8월 처분 취소 소송을 제기했는데 1년 5개월 동안 2차례의 변론만 속행됐다. 동구바이오제약은 처분 집행정지 인용으로 처분에 따른 손실이 발생하지 않았다. 하지만 소송에서 패소하면 막대한 피해가 불가피하다. 동구바이오제약은 내용고형제 제조시설 행정처분에 따른 영업정지금액을 1430억원으로 추산했다. 2024년 전체 매출액 2149억원의 66.6%에 해당하는 규모다. 동구바이오제약의 수탁 사업을 활발히 한다는 점에서 처분이 효력을 발생하면 제약업계 전반에 걸쳐 파장이 커질 수 있다는 우려가 나온다. 예를 들어 동구바이오제약은 대화제약, 테라젠이텍스, JW신약, 에이프로젠바이오로직스, 한국피엠지제약, 에이치엘비제약, 제일약품, JW중외제약, 명문제약, 오스틴제약, 비보존제약, 진양제약, 인트로바이오파마, 서울제약, 넥스팜코리아, 케이엠에스제약, 한국유니온제약, 제뉴파마, 알리코제약, 성원애드콕제약, 동광제약 등 21곳에 콜린제제 연질캡슐을 생산·공급한다. 동구바이오제약의 공장 가동이 중단되면 위탁 업체들도 의약품을 공급받을 수 없어 동반 손실을 입게되는 구조다. 2000년부터 불거진 보툴리눔독소제제 허가 취소 행정소송은 종착지가 임박했다. 국내 제약바이오기업 7곳의 보툴리눔독소제제 16개 품목이 허가취소 처분이 예고됐다. 메디톡스, 휴젤, 파마리서치바이오, 제테마, 한국비엠아이, 한국비엔씨, 휴온스바이오파마 등 7개 업체가 보툴리눔독소제제의 허가취소 처분 등을 통보받았다. 메디톡스는 총 3건의 허가취소 처분에 대한 행정소송을 진행 중이다. 2020년 10월 식약처는 국가출하승인을 받지 않고 판매한 메디톡신주 메디톡신주 50・100・150・200단위, 코어톡스주에 대해 약사법 위반으로 품목 허가취소 행정처분 절차에 착수했다. 식약처는 2020년 12월 이노톡스에 대해 잠정 제조·판매·사용 중지와 허가 취소 등 처분 절차에 착수했다. 국민권익위원회에 공익신고로 제보된 허가제출서류 조작 의혹에 대해 검찰의 수사 결과에 따른 후속조치다. 검찰은 메디톡스가 이노톡스의 품목허가와 변경허가를 하는 과정에서 안정성 시험 자료를 위조했다는 이유로 공무집행방해로 기소했다. 식약처는 메디톡스가 ‘거짓이나 그 밖의 부정한 방법으로 품목허가와 변경허가를 받은 경우’에 해당한다고 판단해 품목 허가취소 절차에 착수했다. 메디톡신 메디톡신주 50・100・150・200단위, 코어톡스 등의 간접수출 위반 사건은 메디톡스가 1심과 2심에서 승소한 상태다. 메디톡스는 메디톡신의 성분 변경 처분에 대해 원액은 바뀌지 않았다는 이유로 처분이 부당하다는 행정소송을 제기했고 지난달 대법원 승소 판결을 받았다. 메디톡스가 청구한 이노톡스 행정처분 취소소송은 현재 1심 재판이 진행 중이다. 2021년 11월 식약처는 국가출하승인을 받지 않고 판매했다는 혐의로 휴젤의 보툴렉스, 보툴렉스50단위, 보툴렉스150단위, 보툴렉스200단위 등 4종과 파마리서치바이오의 리엔톡스100단위와 리엔톡스200단위 등에 대해 품목허가 취소 등 행정처분과 회수·폐기 절차에 착수했다. 2022년 12월 제테마의 제테마더톡신100단위, 한국비엠아이의 하이톡스100단위, 한국비엔씨의 비에녹스주 등 3개사의 3개 제품이 품목허가 취소가 통지됐다. 지난해 7월 휴온스바이오파마의 리즈톡스주100단위에 대해 허가 취소 처분이 예고됐다. 파마리서치바이오는 2023년 12월 식약처를 상대로 제기한 처분 취소소송에서 승소 판결을 받았다. 휴젤은 지난해 2월 서울행정법원으로부터 1심 승소 판결을 선고받았다. 한국비엔씨가 의약품 회수·폐기 및 잠정 제조중지 등 명령 취소 소송에서 지난해 9월 일부 승소했다. 재판부는 한국비엔씨의 보툴리눔독소제제 비에녹스에 대한 잠정 제조중지 명령의 효력을 이 사건 항소심 판결 선고시까지 정지한다고 판결했다. 한국비엔씨가 청구한 허가취소 처분에 대한 취소소송은 현재 1심 재판이 진행 중이다.2026-01-09 06:00:59천승현 기자
끝없는 재평가 수난과 소송전...제약사들의 복잡한 병오년[데일리팜=천승현 기자] 올해 제약사들은 정부 규제 후유증으로 혹독한 시험대에 오를 전망이다. 알포세레이트(콜린제제)의 임상재평가가 막바지로 향하면서 생존 여부와 막대한 환수에 대한 윤곽이 조금씩 드러날 것으로 예상된다. 제약사 수십곳이 연루된 애엽 추출물의 급여재평가도 초미의 관심사다. GMP 적합판정 취소와 보툴리눔독소제제 허가취소 처분에 대한 소송전 결과에 따라 제약업계 전반에 막대한 영향을 미칠 예정이다. 콜린제제 임상재평가 종료 임박...임상 실패시 대규모 환수·집단 소송 불가피 9일 업계에 따르면 올해부터 콜린제제의 임상재평가가 순차적으로 종료될 예정이다. 콜린제제의 임상재평가는 종근당과 대웅바이오의 주도로 진행 중이다. 종근당이 퇴행성 경도인지장애와 혈관성 경도인지장애 임상시험을 각각 수행하고, 대웅바이오가 치매 환자 대상 임상시험을 진행하는 방식이다. 종근당이 진행하는 경도인지장애 환자 대상 임상시험의 경우 종료시한이 3년 9개월로 설정됐다. 대웅바이오의 알츠하이머 환자 대상 임상시험의 경우 4년 6개월 이내에 마무리해야 한다. 당초 종근당의 혈관성 경도인지장애의 재평가 임상시험은 올해 3월 종료가 예정됐는데 내년 6월로 결과보고서 제출기한이 연장됐다. 퇴행성 경도인지장애 재평가 임상의 경우 2027년 3월로 종료 시기가 연장됐다. 대웅바이오의 알츠하이머 임상시험은 2027년 10월이 종료 기한으로 지정됐다. 콜린제제의 임상재평가 결과는 국내 제약업계 전반에 걸쳐 막대한 후폭풍을 가져올 수 있다. 만약 임상재평가가 실패로 결론나면 연간 6000억원 규모의 처방액 손실과 함께 초유의 수천억원 규모 환수 리스크가 현실화하기 때문이다. 지난 2020년 12월 보건복지부는 국민건강보험공단에 콜린제제를 보유한 업체들에 '임상시험에 실패할 경우 처방액을 반환하라‘는 내용의 요양급여계약을 명령했다. 협상 명령 8개월만에 제약사들은 콜린제제의 재평가 임상 실패로 최종적으로 적응증이 삭제될 경우 임상시험 계획서를 승인받은 날부터 삭제일까지 처방액의 20%를 건보공단에 돌려주겠다고 합의했다. 의약품 조사기관 유비스트에 따르면 지난 2024년 콜린제제의 외래 처방시장 규모는 6123억원이다. 만약 콜린제제 임상시험 계획 승인 이후 5년간 진행한 임상시험이 실패할 경우 제약사들의 환수 금액은 5000억원 이상으로 추산된다. 제약사들은 콜린제제의 임상재평가가 끝나지 않았는데도 이미 임상 실패를 가정한 부채를 인식한 상황이다. 종근당, 대웅바이오, 한미약품, 알리코제약, 동구바이오제약, 국제약품, 동광약품, 경동제약, 제뉴파마, 동국제약, 환인제약 등이 콜린제제를 판매 중인 주요 업체들이 많게는 수백억원 규모의 환수 금액 추정치를 미리 부채 항목 등에 반영했다. 제약사들은 환수를 저지하기 위해 전방위 소송전을 전개하고 있지만 좀처럼 승기를 잡지 못하는 상황이다. 복지부의 환수협상 명령 이후 제약사들은 협상 명령이 무효라는 행정소송을 일제히 제기했다. 제약사들은 1차 협상 명령과 2차 협상 명령에 대해 각각 2개 그룹으로 나눠 총 4건의 소송을 청구했는데 지난해 대법원까지 모두 패소했다. 제약사들은 지난 2024년 콜린제제 환수협상 계약은 무효라는 내용의 행정소송을 추가로 제기했다. 법무법인 세종이 종근당 등 24곳의 사건을 맡았고 법무법인 광장이 대웅바이오 등 13곳의 소송을 대리했다. 종근당 등은 지난해 9월 패소했고 대웅바이오 등은 작년 12월 기각 판결을 받았다. 콜린제제의 임상재평가는 임상시험이 종료되는 적응증별로 퇴출 여부가 결정될 가능성이 크다. 뇌질환 치료제 아세틸엘카르니틴은 적응증별로 임상재평가 결론이 도출됐다. 지난 2013년 식약처는 아세틸엘카르니틴제제에 대한 임상재평가를 지시했다. 재평가 임상은 적응증에 따라 ’일차적 퇴행성 질환‘과 ’뇌혈관 질환에 의한 이차적 퇴행성 질환‘ 2개 그룹으로 나눠 진행됐다. 임상시험 결과 지난 2019년 7월 일차적 퇴행성 질환을 입증하지 못해 해당 적응증이 삭제됐다. 2021년 8월에는 ‘뇌혈관 질환에 의한 이차적 퇴행성 질환’도 유효성을 입증하지 못한 것으로 결론났다. 아세틸엘카르니틴은 임상재평가 실패로 인한 처방액 환수 조항이 없어 시장 퇴출에서 마무리됐다. 제약사들은 콜린제제의 임상실패시 보건당국이 환수금액을 청구하더라도 또 다시 소송전이 펼쳐질 수 밖에 없다. 제약사들은 콜린제제의 허가가 유효한 상황에서 재평가 임상시험 실패로 막대한 금액을 부담하는 것은 납득하기 어렵다는 인식이 팽배하다. 제약사들은 올해 콜린제제의 급여축소에 따른 손실도 대비해야 하는 처지다. 복지부는 2020년 8월 콜린제제의 새로운 급여 기준 내용을 담은 ‘요양급여의 적용기준 및 방법에 관한 세부사항’ 일부 개정고시를 발령했다. 치매 진단을 받지 않은 환자가 콜린제제를 사용할 경우 약값 부담률을 30%에서 80%로 올리는 내용이다. 제약사들은 콜린제제 급여 축소의 부당함을 따지는 취소 소송을 제기했지만 지난해 최종 패소했다. 업계에서는 처방 현장에서 환자들의 콜린제제 약값 부담 2.7배 상승하면 처방 기피 현상이 발생할 수 있다는 우려가 커지는 실정이다. 실제로 콜린제제의 급여 축소는 지난해 9월 21일부터 적용됐는데 작년 10월 처방시장 규모는 333억원으로 전년동기보다 37.3% 감소했고 전월 대비 33.9% 축소됐다. 제약사들은 콜린제제의 약값이 저렴한 수준이어서 급여 축소 이후에도 기존에 만족도가 높은 의료진과 환자들을 중심으로 급격한 처방 중단으로 이어지지 않을 것으로 기대하는 모습이다. 애엽 추출물 첫 1천억대 급여재평가 탈락 가능성...제네릭 동등성 재평가도 영향 촉각 제약사들은 올해 애엽 추출물 위염치료제의 생존에 큰 관심을 기울인다. 40여개 업체가 애엽 추출물을 파는데다 제네릭의 동등성 재평가 성패에도 영향을 미친다. 애엽 성분 의약품은 쑥을 기반으로 만드는 천연물의약품이다. 동아에스티의 ‘스티렌’이 오리지널 제품으로 급성위염과 만성위염의 위점막 병변, 출혈, 발적, 부종 등의 개선에 사용된다. 건강보험심사평가원은 지난해 8월 약제급여평가위원회에서 심의한 결과 애엽 추출물에 대해 임상적 유용성 근거가 없다는 이유로 급여 적정성이 없다는 결론을 내렸다. 제약사들은 급여 재평가 결과를 수용할 수 없다며 이의신청을 제기했고 심평원은 ‘비용효과성 충족시 급여적정성 있음’이라는 결론을 내렸다. 애엽 추출물의 약가 인하에 합의한 제품에 대해 비용 효과성이 인정된다는 판단으로 급여 잔류를 결정했다. 하지만 지난해 12월 건강보험정책심의위원회는 애엽 추출물의 급여재평가 결론을 보류했다. 추가 검토 필요성이 제기됐다는 이유에서다. 당초 이달부터 애엽 추출물 성분 의약품 74종의 보험상한가가 평균 14.3% 인하되는 절충안이 예고됐지만 건정심에서는 이 안건을 다루지 않았다. 애엽 추출물은 지난 2024년 1298억원의 외래 처방시장을 형성했다. 급여 삭제시 연간 1000억원 이상의 수익이 증발하는 셈이다. 지난 2021년부터 급여재평가 결과 빌베리건조엑스, 스트렙토키나제·스트렙토도르나제, 옥시라세탐, 아세틸엘카르니틴, 이토프리드 등이 전 제품 급여 삭제가 결정됐는데 모두 연간 처방액이 1000억원 미만이었다. 애엽추출물은 용량과 제조법에 따라 총 4종류가 있는데 평균 약가는 107원, 124원, 186원, 205원이다. 4종류의 애엽추출물이 비슷하게 처방됐다고 가정하면 지난해에만 총 8억개 이상이 처방됐다는 계산이 나온다. 국민 1인당 15개 이상 처방받는 '국민 위염약'이 퇴출 기로에 놓인 셈이다. 만약 애엽추출물이 약가인하를 조건으로 급여목록에 잔류하더라도 제약사들은 대규모 손실이 예고됐다. 당초 약가 인하 대상 애엽 추출물 74개 품목은 지난해 4분기부터 올해 3분기까지 최근 1년 간 총 1066억원의 처방금액을 합작했다. 약가인하 제품들의 인하율을 적용하면 연간 152억원의 손실이 발생하는 것으로 추산됐다. 애엽에탄올연조엑스 성분 제네릭 제품들은 급여재평가를 통과하더라도 시장 잔류를 위한 또 다른 시험대에 오른다. 제약사 50여곳은 지난 6월 말 식품의약품안전처에 애엽 성분 위염치료제의 임상시험 계획서를 제출했다. 오리지널 의약품 스티렌과 스티렌투엑스를 각각 대조약으로 위염치료제 효능을 비교하는 내용의 임상시험이다. 식약처의 동등성 재평가 지시에 따른 임상시험 수행 계획이다. 제약사들은 동등성 재평가 대상 애엽 추출물 의약품을 스티렌과 스티렌투엑스와 각각 비교 임상시험하는 방식으로 동등성을 입증할 계획이다. 생약제제 특성상 유효 성분의 혈중농도를 비교하는 생물학적동등성시험으로 동등성을 입증하기 어렵다는 이유에서다. 스티렌과 스티렌투엑스 제네릭 제품들은 비교 용출과 비교 붕해 방식으로 허가받았다. 만약 애엽추출물의 급여 탈락이 결정되면 제약사들이 추진 중인 동등성 재평가 임상시험도 동력을 상실할 공산이 크다. GMP 적합판정 취소 행정소송 업계 파장 예의주시...보툴리눔 처분 소송도 종착지 임박 정부의 제조·품질관리기준(GMP) 적합판정서 취소 처분에 대한 행정소송도 올해 제약업계의 큰 관심사로 지목된다. 제약사들이 주장하는 GMP 적합판정 취소 처분의 부당성에 대해 법원이 결론을 내릴 전망이다. 한국휴텍스제약과 동구바이오제약은 피해금액이 크고 다른 기업들과 활발한 위수탁 관계를 맺고 있어 처분 패소시 제약업계 전반에 영향을 미칠 수 있다. 2022년 12월부터 GMP 적합판정을 거짓·부정하게 받거나 반복적으로 의약품 제조·품질관리에 관한 기록을 거짓으로 작성해 판매한 사실이 적발된 경우 GMP 적합판정을 취소하는 일명 'GMP 원스트라이크 아웃'이 도입됐다. 식품의약품안전처는 2023년 7월 휴텍스제약이 6개 제품을 제조하는 과정에서 첨가제를 임의로 증량하거나 감량해 허가 사항과 다르게 제조하고, 제조기록서를 거짓 작성하는 등의 위반 사실을 확인하고 GMP 적합판정 취소 처분을 결정했다. 휴텍스제약은 GMP 적합판정 취소 처분 취소소송을 제기했지만 지난해 1월 패소 판결을 받았고 현재 항소심이 진행 중이다. 휴텍스제약은 일시적으로 GMP 적합판정 취소 처분의 효력이 발생하면서 막대한 손실이 현실화한 상태다. 당초 휴텍스제약이 제기한 처분 집행정지 결정의 지연과 기각으로 2024년 2월 1일부터 지난 3월 4일까지 33일 동안 처분 효력이 발생했다. 휴텍스제약은 작년 상반기 외래 처방금액은 624억원으로 2023년 상반기 1581억원과 비교하면 2년새 60.5% 줄었다. 동구바이오제약의 GMP 적합판정 취소 처분은 위탁사들의 영업 활동에도 영향을 미칠 전망이다. 식약처는 2024년 8월 동구바이오제약의 내용고형제 제조시설에 대해 GMP 적합 판정 취소 처분을 통보했다. 식약처는 동구바이오제약이 해열진통제 록소리스정과 당뇨치료제 글리파엠정을 생산하는 과정에서 첨가제 등을 임의로 변경해 허가사항과 다르게 제조하고 제조기록서에는 허가사항과 동일하게 제조한 것처럼 거짓 작성했다고 판단했다. 동구바이오제약은 2024년 8월 처분 취소 소송을 제기했는데 1년 5개월 동안 2차례의 변론만 속행됐다. 동구바이오제약은 처분 집행정지 인용으로 처분에 따른 손실이 발생하지 않았다. 하지만 소송에서 패소하면 막대한 피해가 불가피하다. 동구바이오제약은 내용고형제 제조시설 행정처분에 따른 영업정지금액을 1430억원으로 추산했다. 2024년 전체 매출액 2149억원의 66.6%에 해당하는 규모다. 동구바이오제약의 수탁 사업을 활발히 한다는 점에서 처분이 효력을 발생하면 제약업계 전반에 걸쳐 파장이 커질 수 있다는 우려가 나온다. 예를 들어 동구바이오제약은 대화제약, 테라젠이텍스, JW신약, 에이프로젠바이오로직스, 한국피엠지제약, 에이치엘비제약, 제일약품, JW중외제약, 명문제약, 오스틴제약, 비보존제약, 진양제약, 인트로바이오파마, 서울제약, 넥스팜코리아, 케이엠에스제약, 한국유니온제약, 제뉴파마, 알리코제약, 성원애드콕제약, 동광제약 등 21곳에 콜린제제 연질캡슐을 생산·공급한다. 동구바이오제약의 공장 가동이 중단되면 위탁 업체들도 의약품을 공급받을 수 없어 동반 손실을 입게되는 구조다. 2000년부터 불거진 보툴리눔독소제제 허가 취소 행정소송은 종착지가 임박했다. 국내 제약바이오기업 7곳의 보툴리눔독소제제 16개 품목이 허가취소 처분이 예고됐다. 메디톡스, 휴젤, 파마리서치바이오, 제테마, 한국비엠아이, 한국비엔씨, 휴온스바이오파마 등 7개 업체가 보툴리눔독소제제의 허가취소 처분 등을 통보받았다. 메디톡스는 총 3건의 허가취소 처분에 대한 행정소송을 진행 중이다. 2020년 10월 식약처는 국가출하승인을 받지 않고 판매한 메디톡신주 메디톡신주 50・100・150・200단위, 코어톡스주에 대해 약사법 위반으로 품목 허가취소 행정처분 절차에 착수했다. 식약처는 2020년 12월 이노톡스에 대해 잠정 제조·판매·사용 중지와 허가 취소 등 처분 절차에 착수했다. 국민권익위원회에 공익신고로 제보된 허가제출서류 조작 의혹에 대해 검찰의 수사 결과에 따른 후속조치다. 검찰은 메디톡스가 이노톡스의 품목허가와 변경허가를 하는 과정에서 안정성 시험 자료를 위조했다는 이유로 공무집행방해로 기소했다. 식약처는 메디톡스가 ‘거짓이나 그 밖의 부정한 방법으로 품목허가와 변경허가를 받은 경우’에 해당한다고 판단해 품목 허가취소 절차에 착수했다. 메디톡신 메디톡신주 50・100・150・200단위, 코어톡스 등의 간접수출 위반 사건은 메디톡스가 1심과 2심에서 승소한 상태다. 메디톡스는 메디톡신의 성분 변경 처분에 대해 원액은 바뀌지 않았다는 이유로 처분이 부당하다는 행정소송을 제기했고 지난달 대법원 승소 판결을 받았다. 메디톡스가 청구한 이노톡스 행정처분 취소소송은 현재 1심 재판이 진행 중이다. 2021년 11월 식약처는 국가출하승인을 받지 않고 판매했다는 혐의로 휴젤의 보툴렉스, 보툴렉스50단위, 보툴렉스150단위, 보툴렉스200단위 등 4종과 파마리서치바이오의 리엔톡스100단위와 리엔톡스200단위 등에 대해 품목허가 취소 등 행정처분과 회수·폐기 절차에 착수했다. 2022년 12월 제테마의 제테마더톡신100단위, 한국비엠아이의 하이톡스100단위, 한국비엔씨의 비에녹스주 등 3개사의 3개 제품이 품목허가 취소가 통지됐다. 지난해 7월 휴온스바이오파마의 리즈톡스주100단위에 대해 허가 취소 처분이 예고됐다. 파마리서치바이오는 2023년 12월 식약처를 상대로 제기한 처분 취소소송에서 승소 판결을 받았다. 휴젤은 지난해 2월 서울행정법원으로부터 1심 승소 판결을 선고받았다. 한국비엔씨가 의약품 회수·폐기 및 잠정 제조중지 등 명령 취소 소송에서 지난해 9월 일부 승소했다. 재판부는 한국비엔씨의 보툴리눔독소제제 비에녹스에 대한 잠정 제조중지 명령의 효력을 이 사건 항소심 판결 선고시까지 정지한다고 판결했다. 한국비엔씨가 청구한 허가취소 처분에 대한 취소소송은 현재 1심 재판이 진행 중이다.2026-01-09 06:00:59천승현 기자 -
 일차의료 방문진료 청구 13배 증가...약국 단절은 한계[데일리팜=정흥준 기자]일차의료 방문진료 수가 시범사업 청구건수가 지난 5년간 13배 증가했지만, 해외와 달리 약 수령 연계가 되지 않아 한계가 있다는 지적이다. 실제 시범사업에 참여하는 의사도 “(대상 환자가)약 처방전은 받되 한 번도 약 탄적은 없다고 한다”며 약 수령 체계 개선 필요성을 제기했다. 8일 건강보험심사평가원의 ‘일차의료 방문진료 수가 시범사업 2차 효과평가 연구’ 결과에 따르면 2020년 1월부터 2024년 12월까지 방문진료료 청구 건수는 12만374건이다. 170억원 규모의 진료비가 지출됐다. 참여기관과 환자, 청구 건수는 지속적으로 증가하고 있다. 2020년 4936건이었던 청구건수는 작년 6만4193건으로 약 13배 상승했다. 등록 의료기관은 348개에서 993개로 증가했다. 다만, 등록 기관 중 참여율은 약 26%에 그쳤다. 실질적으로 참여한 의료기관은 2024년 기준 256곳이었다. 방문진료를 받은 환자 숫자는 2020년 1500명에서, 2024년 1만9227명으로 늘어났다. 진료비 총액은 5억6887만원에서 97억1701만원으로 증가했다. 2024년 기준 방문진료 의사 수는 기관당 1.7명이었다. 표시과목은 256곳 중 일반의가 150개소, 내과 48개소, 가정의학과 29개소 순으로 많았다. 환자는 70세 이상 환자가 88.9%를 차지했다. 2020년 83.7%에서 점차 증가하는 추세다. 의료보장 유형에서는 건강보험 환자 비율이 69.6%, 의료급여 환자가 26.6%로 집계됐다. "약 처방전만 받고 수령은 NO...약 재택 수령도 고려사항" 일차의료 방문진료 시범사업은 약국, 약사가 참여하지 않다보니 약 수령에서 한계가 드러났다. 연구에서는 참여 의사 심층인터뷰로 문제점을 짚었는데, 그 중 한 의사는 “처방전은 받되 한번도 약 탄적은 없다고 한다. 요양보호사가 와서 능력 있다면 구해주긴 하겠지만 그게 안 된다”고 했다. 반면, 해외에서 진행되는 방문진료 유사 사업에서는 약사 역할이 연계돼 있다. 일본은 통원 치료가 곤란한 환자에게 약국 약사가 방문해 약학적 관리·지도를 한 경우 월 4회 한도로 290~650점의 수가 가산을 산정한다. 마약 관리 지도와 유아 가산이 따로 있다. 대만은 건강보험과 계약한 의료기관 종사자로 구성된 팀이 재택의료 등을 제공하는데 의사는 월 180회, 약사는 월 45회 제한 안에서 서비스를 제공하고 있다. 2024년 7월부터 시행하는 ‘재택응급진료 시범사업’에서는 의사의 외래진료 서비스, 간호사의 가정간호 및 간병 지도, 호흡치료사의 호흡돌봄지도, 약사의 약사 돌봄 등이 함께 제공되고 있다. 연구진은 비대면진료 시범사업의 의약품 수령방식을 도입하는 방안을 제시했다. 연구진은 “환자가 거동불편자이고 보호자도 고령으로 노쇠한 경우 처방전을 받아 약국을 방문하기 어려울 수 있다. 환자 상황에 맞춰 비대면진료 시범사업과 같은 형태의 의약품 수령 방식을 고려할 수 있다”고 했다. 비대면진료 시범사업에서는 의사가 환자가 지정하는 약국으로 처방전을 직접 전송하고, 약사는 환자와 협의해 조제 가능 여부를 확인하고 수령 방식을 결정한다. 특히 취약계층 등은 재택 수령이 가능하다.2026-01-09 06:00:49정흥준 기자
일차의료 방문진료 청구 13배 증가...약국 단절은 한계[데일리팜=정흥준 기자]일차의료 방문진료 수가 시범사업 청구건수가 지난 5년간 13배 증가했지만, 해외와 달리 약 수령 연계가 되지 않아 한계가 있다는 지적이다. 실제 시범사업에 참여하는 의사도 “(대상 환자가)약 처방전은 받되 한 번도 약 탄적은 없다고 한다”며 약 수령 체계 개선 필요성을 제기했다. 8일 건강보험심사평가원의 ‘일차의료 방문진료 수가 시범사업 2차 효과평가 연구’ 결과에 따르면 2020년 1월부터 2024년 12월까지 방문진료료 청구 건수는 12만374건이다. 170억원 규모의 진료비가 지출됐다. 참여기관과 환자, 청구 건수는 지속적으로 증가하고 있다. 2020년 4936건이었던 청구건수는 작년 6만4193건으로 약 13배 상승했다. 등록 의료기관은 348개에서 993개로 증가했다. 다만, 등록 기관 중 참여율은 약 26%에 그쳤다. 실질적으로 참여한 의료기관은 2024년 기준 256곳이었다. 방문진료를 받은 환자 숫자는 2020년 1500명에서, 2024년 1만9227명으로 늘어났다. 진료비 총액은 5억6887만원에서 97억1701만원으로 증가했다. 2024년 기준 방문진료 의사 수는 기관당 1.7명이었다. 표시과목은 256곳 중 일반의가 150개소, 내과 48개소, 가정의학과 29개소 순으로 많았다. 환자는 70세 이상 환자가 88.9%를 차지했다. 2020년 83.7%에서 점차 증가하는 추세다. 의료보장 유형에서는 건강보험 환자 비율이 69.6%, 의료급여 환자가 26.6%로 집계됐다. "약 처방전만 받고 수령은 NO...약 재택 수령도 고려사항" 일차의료 방문진료 시범사업은 약국, 약사가 참여하지 않다보니 약 수령에서 한계가 드러났다. 연구에서는 참여 의사 심층인터뷰로 문제점을 짚었는데, 그 중 한 의사는 “처방전은 받되 한번도 약 탄적은 없다고 한다. 요양보호사가 와서 능력 있다면 구해주긴 하겠지만 그게 안 된다”고 했다. 반면, 해외에서 진행되는 방문진료 유사 사업에서는 약사 역할이 연계돼 있다. 일본은 통원 치료가 곤란한 환자에게 약국 약사가 방문해 약학적 관리·지도를 한 경우 월 4회 한도로 290~650점의 수가 가산을 산정한다. 마약 관리 지도와 유아 가산이 따로 있다. 대만은 건강보험과 계약한 의료기관 종사자로 구성된 팀이 재택의료 등을 제공하는데 의사는 월 180회, 약사는 월 45회 제한 안에서 서비스를 제공하고 있다. 2024년 7월부터 시행하는 ‘재택응급진료 시범사업’에서는 의사의 외래진료 서비스, 간호사의 가정간호 및 간병 지도, 호흡치료사의 호흡돌봄지도, 약사의 약사 돌봄 등이 함께 제공되고 있다. 연구진은 비대면진료 시범사업의 의약품 수령방식을 도입하는 방안을 제시했다. 연구진은 “환자가 거동불편자이고 보호자도 고령으로 노쇠한 경우 처방전을 받아 약국을 방문하기 어려울 수 있다. 환자 상황에 맞춰 비대면진료 시범사업과 같은 형태의 의약품 수령 방식을 고려할 수 있다”고 했다. 비대면진료 시범사업에서는 의사가 환자가 지정하는 약국으로 처방전을 직접 전송하고, 약사는 환자와 협의해 조제 가능 여부를 확인하고 수령 방식을 결정한다. 특히 취약계층 등은 재택 수령이 가능하다.2026-01-09 06:00:49정흥준 기자 -
 발매 1년됐는데...부광 CNS 신약 '라투다' 특허 도전장[데일리팜=김진구 기자] 부광약품의 양극성장애 신약 ‘라투다(루라시돈)’가 제네릭사들의 특허 공략 타깃이 됐다. 8일 제약업계에 따르면 영진약품·종근당·유니메드제약은 지난 7일 라투다 조성물특허 2건에 소극적 권리범위확인 심판을 청구했다. 이로써 라투다 특허에 도전하는 제네릭사는 총 5곳으로 늘었다. 작년 말 환인제약이 라투다 특허 2건에 회피 심판을 청구한 데 이어, 이달 6일엔 명인제약이 도전 대열에 합류한 바 있다. 식품의약품안전처 특허목록집에 등재된 라투다 특허는 2건이으로, 모두 2031년 5월 만료된다. 제네릭사들은 두 특허 각각에 심판을 청구했으며, 심판에서 승리할 경우 제네릭 품목허가와 조기 발매에 한 발 가까워진다. 라투다는 일본 스미토모 파마가 개발한 양극성장애 치료제다. 국내에선 만 13세 이상 청소년·성인의 조현병 치료, 만 10세 이상 소아·성인의 양극성 장애 치료제로 허가받았다. 기존 비정형 CNS 약물과 비교해 고지혈증·당뇨병과 체중 증가 등 이상반응이 낮다는 점이 특징으로 꼽힌다. 부광약품은 지난 2017년 스미토모와 국내 독점 라이선스 계약을 체결했다. 2023년 11월 국내 허가를 획득한 뒤, 2024년 8월 급여 적용과 함께 제품을 발매했다. 라투다의 빠른 시장 안착이 제네릭사 특허 공략의 배경으로 작용했다는 분석이다. 라투다는 2024년 3분기부터 작년 3분기까지 출시 1년 만에 누적 매출 100억원을 돌파했다. 실적이 빠르게 증가하며 작년 4분기엔 사용량-약가 연동제 모니터링 대상에 포함됐다. 동시에 부광약품의 핵심 제품으로 자리잡았다. 라투다를 중심으로 지난해 3분기 부광약품의 CNS 사업부 매출은 전년동기 대비 54% 증가했다. 회사는 출시 3년차인 올해 라투다 매출 300억원 달성과 조현병·양극성장애 치료제 시장에서 점유율 1위 달성을 목표로 하고 있다.2026-01-08 12:09:16김진구 기자
발매 1년됐는데...부광 CNS 신약 '라투다' 특허 도전장[데일리팜=김진구 기자] 부광약품의 양극성장애 신약 ‘라투다(루라시돈)’가 제네릭사들의 특허 공략 타깃이 됐다. 8일 제약업계에 따르면 영진약품·종근당·유니메드제약은 지난 7일 라투다 조성물특허 2건에 소극적 권리범위확인 심판을 청구했다. 이로써 라투다 특허에 도전하는 제네릭사는 총 5곳으로 늘었다. 작년 말 환인제약이 라투다 특허 2건에 회피 심판을 청구한 데 이어, 이달 6일엔 명인제약이 도전 대열에 합류한 바 있다. 식품의약품안전처 특허목록집에 등재된 라투다 특허는 2건이으로, 모두 2031년 5월 만료된다. 제네릭사들은 두 특허 각각에 심판을 청구했으며, 심판에서 승리할 경우 제네릭 품목허가와 조기 발매에 한 발 가까워진다. 라투다는 일본 스미토모 파마가 개발한 양극성장애 치료제다. 국내에선 만 13세 이상 청소년·성인의 조현병 치료, 만 10세 이상 소아·성인의 양극성 장애 치료제로 허가받았다. 기존 비정형 CNS 약물과 비교해 고지혈증·당뇨병과 체중 증가 등 이상반응이 낮다는 점이 특징으로 꼽힌다. 부광약품은 지난 2017년 스미토모와 국내 독점 라이선스 계약을 체결했다. 2023년 11월 국내 허가를 획득한 뒤, 2024년 8월 급여 적용과 함께 제품을 발매했다. 라투다의 빠른 시장 안착이 제네릭사 특허 공략의 배경으로 작용했다는 분석이다. 라투다는 2024년 3분기부터 작년 3분기까지 출시 1년 만에 누적 매출 100억원을 돌파했다. 실적이 빠르게 증가하며 작년 4분기엔 사용량-약가 연동제 모니터링 대상에 포함됐다. 동시에 부광약품의 핵심 제품으로 자리잡았다. 라투다를 중심으로 지난해 3분기 부광약품의 CNS 사업부 매출은 전년동기 대비 54% 증가했다. 회사는 출시 3년차인 올해 라투다 매출 300억원 달성과 조현병·양극성장애 치료제 시장에서 점유율 1위 달성을 목표로 하고 있다.2026-01-08 12:09:16김진구 기자 -
 "비급여 국소마취제 이중 부당청구 추정액 5년간 540억원"[데일리팜=강신국 기자] 5년간 비급여 국소마취제 비용 544억원이 부당청구 됐다며 대책 마련을 촉구하는 목소리가 나왔다. 경실련은 7일 부당한 비급여 사용과 비용 이중 청구가 의심되는 의료기관 및 부당 청구액 규모를 발표하고 건강보험공단에 조사와 대책 마련을 요구했다. 경실련에 따르면 국소마취제는 의료행위 수가에 재료비로 이미 포함돼 의료기관이 공단에서 직접 받아 환자에게 별도로 비용을 받을 수 없는 산정불가 급여다. 즉 환자에게 비급여 비용을 청구할 수 없으나 의약품 제조사(유통사)는 급여와 동일한 성분·효능의 의약품을 등재하지 않고 의료기관은 수십배 비싼 비급여 제품을 사용하고 그 비용을 환자에게 이중으로 청구한다는 게 경실련의 주장이다. 경실련은 "행위별 수가제는 진료 행위에 드는 비용을 정할 때 서비스 비용, 재료비용, 위험비용을 함께 책정해 환자에게 별도 부담하지 않도록 하고 있다"며 "산정불가의 취지는 환자의 추가 의료비 부담을 막아 치료에 대한 접근성을 보장하기 위한 건강보험 수가제도의 원칙인데 국소마취제의 비급여 청구는 이와 위배된다"고 밝혔다. 경실련 조사 결과, 국소마취제를 사용하는 3개 주요 의료행위(도뇨, 방광경, 유치카테타)는 연간 300만건 내외로 시행되고 있으며, 사용량 비중은 종합병원이 40% 내외로 가장 크고, 상급종합병원은 30% 내외, 병원급은 20% 초반으로 대부분 병원급 이상에서 실시되고 있다. 의료기관의 비급여 국소마취제 사용실태를 파악하기 위해 행위 빈도가 높은 상급종합병원의 비급여 가격 고지 실태를 조사한 결과 45개 병원 중 화순전남대병원만 유일하게 가격을 고지하지 않아 비급여를 사용하지 않는 것으로 판단된다. 나머지 44개 병원은 1~3개의 비급여 국소마취제 가격을 고지했는데 가장 많이 사용되는 제품은 인스틸라젤겔(11ml)로 34개 기관에서 사용됐고 가격은 급여 대비 최소 9.9배 ~ 최대 19배 비쌌다. 상급종합병원의 비급여 국소마취제 고지 가격과 의약품유통정보센터에 신고된 출고량을 종합해 신고된 비급여 제품의 환자 청구 총액을 산출했더니 출고된 비급여 제품이 모두 사용됐다고 가정하면 5년간 약 544억원 가량이 환자에게 부당하게 이중 청구됐을 것으로 추정했다. 경실련은 "의료기관이 건강보험 급여 대신 비급여 제품을 사용하는 것은 건강보험의 보장성과 안정성을 훼손할 뿐만 아니라 국민 의료비 부담을 가중시키는 행위로 보험자의 적극적 관리 필요하다"며 "비급여 의약품의 목록을 관리해 동일 성분의 비급여 제품 사용을 방지해야 한다"고 지적했다. 또한 "건강보험제도의 안정적 운영을 위해서는 건강보험 진료 뿐만 아니라 함께 이뤄지는 비급여 진료의 적정성 판단이 필요하므로 의료기관이 급여청구 시 비급여도 모두 함께 보고하도록 할 필요가 있다"고 덧붙였다. 경실련은 "건보공단은 비급여 국소마취제 이중 청구 현장 조사하고, 부당 청구액 환수해야 한다"며 "정부는 유사 사례 조사 및 등재 미신청 비급여 의약품 관리방안 마련해야 한다"고 촉구했다.2026-01-07 21:43:24강신국 기자
"비급여 국소마취제 이중 부당청구 추정액 5년간 540억원"[데일리팜=강신국 기자] 5년간 비급여 국소마취제 비용 544억원이 부당청구 됐다며 대책 마련을 촉구하는 목소리가 나왔다. 경실련은 7일 부당한 비급여 사용과 비용 이중 청구가 의심되는 의료기관 및 부당 청구액 규모를 발표하고 건강보험공단에 조사와 대책 마련을 요구했다. 경실련에 따르면 국소마취제는 의료행위 수가에 재료비로 이미 포함돼 의료기관이 공단에서 직접 받아 환자에게 별도로 비용을 받을 수 없는 산정불가 급여다. 즉 환자에게 비급여 비용을 청구할 수 없으나 의약품 제조사(유통사)는 급여와 동일한 성분·효능의 의약품을 등재하지 않고 의료기관은 수십배 비싼 비급여 제품을 사용하고 그 비용을 환자에게 이중으로 청구한다는 게 경실련의 주장이다. 경실련은 "행위별 수가제는 진료 행위에 드는 비용을 정할 때 서비스 비용, 재료비용, 위험비용을 함께 책정해 환자에게 별도 부담하지 않도록 하고 있다"며 "산정불가의 취지는 환자의 추가 의료비 부담을 막아 치료에 대한 접근성을 보장하기 위한 건강보험 수가제도의 원칙인데 국소마취제의 비급여 청구는 이와 위배된다"고 밝혔다. 경실련 조사 결과, 국소마취제를 사용하는 3개 주요 의료행위(도뇨, 방광경, 유치카테타)는 연간 300만건 내외로 시행되고 있으며, 사용량 비중은 종합병원이 40% 내외로 가장 크고, 상급종합병원은 30% 내외, 병원급은 20% 초반으로 대부분 병원급 이상에서 실시되고 있다. 의료기관의 비급여 국소마취제 사용실태를 파악하기 위해 행위 빈도가 높은 상급종합병원의 비급여 가격 고지 실태를 조사한 결과 45개 병원 중 화순전남대병원만 유일하게 가격을 고지하지 않아 비급여를 사용하지 않는 것으로 판단된다. 나머지 44개 병원은 1~3개의 비급여 국소마취제 가격을 고지했는데 가장 많이 사용되는 제품은 인스틸라젤겔(11ml)로 34개 기관에서 사용됐고 가격은 급여 대비 최소 9.9배 ~ 최대 19배 비쌌다. 상급종합병원의 비급여 국소마취제 고지 가격과 의약품유통정보센터에 신고된 출고량을 종합해 신고된 비급여 제품의 환자 청구 총액을 산출했더니 출고된 비급여 제품이 모두 사용됐다고 가정하면 5년간 약 544억원 가량이 환자에게 부당하게 이중 청구됐을 것으로 추정했다. 경실련은 "의료기관이 건강보험 급여 대신 비급여 제품을 사용하는 것은 건강보험의 보장성과 안정성을 훼손할 뿐만 아니라 국민 의료비 부담을 가중시키는 행위로 보험자의 적극적 관리 필요하다"며 "비급여 의약품의 목록을 관리해 동일 성분의 비급여 제품 사용을 방지해야 한다"고 지적했다. 또한 "건강보험제도의 안정적 운영을 위해서는 건강보험 진료 뿐만 아니라 함께 이뤄지는 비급여 진료의 적정성 판단이 필요하므로 의료기관이 급여청구 시 비급여도 모두 함께 보고하도록 할 필요가 있다"고 덧붙였다. 경실련은 "건보공단은 비급여 국소마취제 이중 청구 현장 조사하고, 부당 청구액 환수해야 한다"며 "정부는 유사 사례 조사 및 등재 미신청 비급여 의약품 관리방안 마련해야 한다"고 촉구했다.2026-01-07 21:43:24강신국 기자 -
 신년회서 드러난 입장차…정부·업계 '약가 개편' 엇갈린 시선[데일리팜=김진구 기자] 2026년 약계 신년교례회가 정부·국회·약업계 주요 인사 200여명이 참석한 가운데 개최됐다. 새해 덕담과 산업 비전 제시가 이어진 가운데, 행사 전반에서는 정부가 추진 중인 약가제도 개편을 둘러싼 시각차가 다시 한 번 드러났다. 한국제약바이오협회와 대한약사회는 약가제도 개편에 따른 산업 영향과 현장 혼선을 우려한 반면, 정부·여당은 약가제도 개편의 기본 방향을 재확인하며 지속 추진 의지를 밝혔다. 노연홍 한국제약바이오협회장은 환영사에서 약가제도 개편을 산업 전반에 영향을 미치는 중대 현안으로 지목했다. 노연홍 회장은 “약가제도 개편은 국내 제약바이오산업의 존립을 뒤흔들 수 있는 사안”이라며 “정부가 정해놓은 일정에 맞춰 추진하기보다 산업 현장과의 협의를 거쳐 국민보건·산업 성장·약가 재정 간 균형을 도모할 수 있는 방향으로 재설계해야 한다”고 말했다. 약가제도 개편의 속도 조절과 함께 제도 보완·조정 필요성을 분명히 한 발언으로 풀이된다. 대한약사회 역시 약가 정책으로 인한 현장 혼선을 우려했다. 권영희 대한약사회장은 “올해 초 대규모 약가 인하로 인해 약국가와 유통업계, 제약업계 모두 현장에서 큰 혼란이 예상된다”며 “반복되는 혼선을 줄이고 정책의 실효성을 높이기 위해 정부가 분명한 제도적 대안을 마련해야 한다”고 말했다. 그는 “재고 청구와 정산 문제 등 실무적 보완이 필요하다”고도 지적했다. 보건복지부는 약가제도 개편의 방향을 ‘혁신 보상과 공급 안정’으로 설명하며 지속 추진 의지를 밝혔다. 이형훈 보건복지부 차관은 “혁신의 가치는 충분히 보상하고 필수의약품은 안정적으로 공급할 수 있도록 약가제도 개선을 추진하겠다”며 “제약바이오 산업이 보다 혁신 지향적인 생태계로 발전할 수 있도록 지원하겠다”고 말했다. 오유경 식품의약품안전처장은 규제 환경 변화에 초점을 맞추며 산업 지원을 약속했다. 오 처장은 “올해를 의약품 규제 서비스 대전환의 첫 해로 삼겠다”며 “심사 인력 확충과 AI 기반 심사 보조 시스템 도입을 통해 심사 속도와 효율성을 높이겠다”고 말했다. 여당 의원들은 대체로 약가제도 개편의 정책 방향을 옹호하는 발언을 이어갔다. 김윤 더불어민주당 의원은 “약가제도 개편을 단순히 건강보험 재정을 절감하기 위해 약값을 깎는 정책으로만 이해해서는 곤란하다”며 “제약바이오 산업을 글로벌 경쟁력을 갖춘 혁신 생태계로 전환하기 위한 정책의 일부”라고 강조했다. 김윤 의원은 “물론 현장에서 제기되는 우려가 적지 않다는 점은 충분히 알고 있다”며 “우리나라 제약산업을 글로벌 수준으로 끌어올린다는 공동의 목표가 있다면 속도 조절과 제도 디테일은 충분히 논의하며 조정할 수 있다”고 말했다. 이어 “국회 차원에서 현장의 목소리를 반영해 약가 조정 정책이 산업 혁신으로 이어질 수 있도록 역할을 하겠다”고 덧붙였다. 서영석 더불어민주당 의원은 “여러 제도적 과제들이 놓여 있지만 판단의 기준은 결국 국민의 건강권”이라며 “국민 보건이라는 큰 틀 안에서 해법을 찾아가야 한다”고 말했다. 야당 의원들은 대체로 현행 약가제도와 정부가 추진 중인 개편 방향에 비판적인 시각을 드러냈다. 최수진 국민의힘 의원은 사용량-약가 연동제를 언급하며 “국민에게 부담 없이 공급할 수 있는 약은 저렴한 제네릭”이라며 “제네릭 약가가 100원 이하로 떨어진다는 건 사실상 생산하지 말라는 것”이라고 지적했다. 최 의원은 이어 “국민에게 더 저렴하게 공급할 수 있는 약의 가격을 단지 사용량이 많다고 인하하는 것은 단순히 숫자와 건보재정 측면에서만 보는 접근”이라며 “재정 건전화만을 이유로 산업이 발전하지 못한다면 한국 제약산업은 결국 경쟁력을 잃게 된다. 약가 인하는 매우 조심스럽게, 총체적인 관점에서 접근해야 할 사안”이라고 강조했다. 한지아 국민의힘 의원은 “제도는 현장을 이길 수 없다”며 산업 현실을 반영한 제도 설계를 주문했고, 이주연 개혁신당 의원 역시 “규제 개선과 투자 환경 조성이 병행되지 않으면 글로벌 경쟁에서 뒤처질 수 있다”고 우려를 표했다. 성분명 처방과 대체조제와 관련한 언급도 있었다. 권영희 약사회장은 “대체조제 사후 통보 간소화를 담은 약사법 개정안이 국회를 통과해 오는 2월 시행을 앞두고 있다”며 “이는 의약분업 이후 오랜 숙원 과제였다”고 평가했다. 권영희 회장은 성분명 처방과 관련해서도 구체적인 수치를 들어 발언했다. 권 회장은 “의약품 정책연구소 연구 결과에 따르면 성분명 처방을 통해 약품비와 사회적 비용을 포함해 총 9조 원 절감이 가능하다”며 정책적 효과를 제시했다. 성분명 처방에 대한 국민적 공감과 언론의 관심이 커지고 있다는 점도 함께 언급했다. 서영석 의원은 대체조제와 관련한 입법 성과를 거론하며 “대체조제 간소화법을 포함해 공직 약사들의 숙원 과제였던 수당 인상 등 제도 개선을 일부 이뤄냈다”며 “만족스럽지는 않지만 의미 있는 진전이었다”고 말했다. 다만 제도 전반에 대해서는 “여전히 해결해야 할 과제가 많다”고 덧붙였다.2026-01-07 18:44:15김진구 기자
신년회서 드러난 입장차…정부·업계 '약가 개편' 엇갈린 시선[데일리팜=김진구 기자] 2026년 약계 신년교례회가 정부·국회·약업계 주요 인사 200여명이 참석한 가운데 개최됐다. 새해 덕담과 산업 비전 제시가 이어진 가운데, 행사 전반에서는 정부가 추진 중인 약가제도 개편을 둘러싼 시각차가 다시 한 번 드러났다. 한국제약바이오협회와 대한약사회는 약가제도 개편에 따른 산업 영향과 현장 혼선을 우려한 반면, 정부·여당은 약가제도 개편의 기본 방향을 재확인하며 지속 추진 의지를 밝혔다. 노연홍 한국제약바이오협회장은 환영사에서 약가제도 개편을 산업 전반에 영향을 미치는 중대 현안으로 지목했다. 노연홍 회장은 “약가제도 개편은 국내 제약바이오산업의 존립을 뒤흔들 수 있는 사안”이라며 “정부가 정해놓은 일정에 맞춰 추진하기보다 산업 현장과의 협의를 거쳐 국민보건·산업 성장·약가 재정 간 균형을 도모할 수 있는 방향으로 재설계해야 한다”고 말했다. 약가제도 개편의 속도 조절과 함께 제도 보완·조정 필요성을 분명히 한 발언으로 풀이된다. 대한약사회 역시 약가 정책으로 인한 현장 혼선을 우려했다. 권영희 대한약사회장은 “올해 초 대규모 약가 인하로 인해 약국가와 유통업계, 제약업계 모두 현장에서 큰 혼란이 예상된다”며 “반복되는 혼선을 줄이고 정책의 실효성을 높이기 위해 정부가 분명한 제도적 대안을 마련해야 한다”고 말했다. 그는 “재고 청구와 정산 문제 등 실무적 보완이 필요하다”고도 지적했다. 보건복지부는 약가제도 개편의 방향을 ‘혁신 보상과 공급 안정’으로 설명하며 지속 추진 의지를 밝혔다. 이형훈 보건복지부 차관은 “혁신의 가치는 충분히 보상하고 필수의약품은 안정적으로 공급할 수 있도록 약가제도 개선을 추진하겠다”며 “제약바이오 산업이 보다 혁신 지향적인 생태계로 발전할 수 있도록 지원하겠다”고 말했다. 오유경 식품의약품안전처장은 규제 환경 변화에 초점을 맞추며 산업 지원을 약속했다. 오 처장은 “올해를 의약품 규제 서비스 대전환의 첫 해로 삼겠다”며 “심사 인력 확충과 AI 기반 심사 보조 시스템 도입을 통해 심사 속도와 효율성을 높이겠다”고 말했다. 여당 의원들은 대체로 약가제도 개편의 정책 방향을 옹호하는 발언을 이어갔다. 김윤 더불어민주당 의원은 “약가제도 개편을 단순히 건강보험 재정을 절감하기 위해 약값을 깎는 정책으로만 이해해서는 곤란하다”며 “제약바이오 산업을 글로벌 경쟁력을 갖춘 혁신 생태계로 전환하기 위한 정책의 일부”라고 강조했다. 김윤 의원은 “물론 현장에서 제기되는 우려가 적지 않다는 점은 충분히 알고 있다”며 “우리나라 제약산업을 글로벌 수준으로 끌어올린다는 공동의 목표가 있다면 속도 조절과 제도 디테일은 충분히 논의하며 조정할 수 있다”고 말했다. 이어 “국회 차원에서 현장의 목소리를 반영해 약가 조정 정책이 산업 혁신으로 이어질 수 있도록 역할을 하겠다”고 덧붙였다. 서영석 더불어민주당 의원은 “여러 제도적 과제들이 놓여 있지만 판단의 기준은 결국 국민의 건강권”이라며 “국민 보건이라는 큰 틀 안에서 해법을 찾아가야 한다”고 말했다. 야당 의원들은 대체로 현행 약가제도와 정부가 추진 중인 개편 방향에 비판적인 시각을 드러냈다. 최수진 국민의힘 의원은 사용량-약가 연동제를 언급하며 “국민에게 부담 없이 공급할 수 있는 약은 저렴한 제네릭”이라며 “제네릭 약가가 100원 이하로 떨어진다는 건 사실상 생산하지 말라는 것”이라고 지적했다. 최 의원은 이어 “국민에게 더 저렴하게 공급할 수 있는 약의 가격을 단지 사용량이 많다고 인하하는 것은 단순히 숫자와 건보재정 측면에서만 보는 접근”이라며 “재정 건전화만을 이유로 산업이 발전하지 못한다면 한국 제약산업은 결국 경쟁력을 잃게 된다. 약가 인하는 매우 조심스럽게, 총체적인 관점에서 접근해야 할 사안”이라고 강조했다. 한지아 국민의힘 의원은 “제도는 현장을 이길 수 없다”며 산업 현실을 반영한 제도 설계를 주문했고, 이주연 개혁신당 의원 역시 “규제 개선과 투자 환경 조성이 병행되지 않으면 글로벌 경쟁에서 뒤처질 수 있다”고 우려를 표했다. 성분명 처방과 대체조제와 관련한 언급도 있었다. 권영희 약사회장은 “대체조제 사후 통보 간소화를 담은 약사법 개정안이 국회를 통과해 오는 2월 시행을 앞두고 있다”며 “이는 의약분업 이후 오랜 숙원 과제였다”고 평가했다. 권영희 회장은 성분명 처방과 관련해서도 구체적인 수치를 들어 발언했다. 권 회장은 “의약품 정책연구소 연구 결과에 따르면 성분명 처방을 통해 약품비와 사회적 비용을 포함해 총 9조 원 절감이 가능하다”며 정책적 효과를 제시했다. 성분명 처방에 대한 국민적 공감과 언론의 관심이 커지고 있다는 점도 함께 언급했다. 서영석 의원은 대체조제와 관련한 입법 성과를 거론하며 “대체조제 간소화법을 포함해 공직 약사들의 숙원 과제였던 수당 인상 등 제도 개선을 일부 이뤄냈다”며 “만족스럽지는 않지만 의미 있는 진전이었다”고 말했다. 다만 제도 전반에 대해서는 “여전히 해결해야 할 과제가 많다”고 덧붙였다.2026-01-07 18:44:15김진구 기자
오늘의 TOP 10
- 1"창고형 노하우 전수"...메가팩토리약국 체인 설립 이유는?
- 2로수젯·케이캡 2천억, 리바로젯 1천억...K-신약 전성기
- 3생필품 배달원된 MR...판결문에 드러난 리베이트 백태
- 415개 장기 품절의약품 공개...조제 차질 등 불편 가중
- 55년 기다리고도…갱신 안 하는 젤잔즈 후발약
- 6재평가 궁여지책...안플라그·고덱스 약가인하 사례 사라질 듯
- 7삼일제약, 베트남 공장 시계가 돈다…상반기 KGMP 목표
- 8수원시약 "일반약 공동구매로 기형적약국 가격파괴 대응"
- 9연 240억 생산...종근당, 시밀러 사업 재도약 속도전
- 10중기부-복지부, 플랫폼 도매 금지법 회동…수정안·원안 충돌
-
상품명최고최저평균
-
게보린(10정)4,0003,0003,782
-
노스카나겔(20g)22,00018,00021,195
-
베나치오에프액(75ml)1,000800996
-
비코그린에스(20정)5,0004,5004,625
-
머시론정(21정)10,0008,5009,873





























![[리쥬올]리쥬올 PDRN 약국 1위 PDRN](https://cdn.platpharm.co.kr/2025/09/2509260220180000170.webp)
![[신신] 아렉스 두번효과로 강력한](https://cdn.platpharm.co.kr/2025/10/2510230254510000664.webp)

![[셀로맥스] 베베락스 온가족 안심 관장약](https://cdn.platpharm.co.kr/2025/09/2509171131320018843.webp)
![[더본메디칼] ATC인쇄리본 특가](https://cdn.platpharm.co.kr/2025/04/2504100527360001454.jpg)
![[신신] 새사래 상처연고 습윤밴드](https://cdn.platpharm.co.kr/2025/10/2510210339570001784.webp)
![[SK케미칼] 속편한정 복합소화제](https://cdn.platpharm.co.kr/2025/12/2512040916400005920.webp)
![[리쥬올]레티노 멜라세럼 저자극 레티놀](https://cdn.platpharm.co.kr/2025/09/2509260219360000145.webp)
![[유한양행] 미녹펜겔 탈모스팟 집중케어](https://cdn.platpharm.co.kr/2025/09/2509220824180004563.webp)
![[유한양행] 콘택콜드 걸렸구나 생각되면](https://cdn.platpharm.co.kr/2025/10/2510282252420008436.webp)
![[SK케미칼] 트라스트패취 피록시캄 성분](https://cdn.platpharm.co.kr/2025/10/2510020656150002375.webp)
![[종근당] 벤포벨에스 어른들의 피로회복제](https://cdn.platpharm.co.kr/2025/07/2507290841210004645.webp)
![[한독] 붙이는 통증 전문가, 케토톱 액티브 플라스타(쿨) 40매](https://i.baropharm.com/products/202503/1741829602305.png)
![[오펠라] 부드럽고 편안한, 둘코락스에스장용정 20정](https://i.baropharm.com/products/202511/1762260404625.png)
![[켄뷰] 다양한 통증에, 타이레놀정 500mg 10정](https://i.baropharm.com/products/6c6ea4f4-7ab2-44f2-a165-f062d80f525b.png)
![[아워팜] 혈행건강 히어로, 혈행건강 초임계 rTG 오메가3 프리미엄](https://i.baropharm.com/products/f724f191-7052-4ad5-bc92-cda889cf13a6.png)
![[아워팜] 아이들이 먼저찾는, 바로타민 kids 미네랄](https://i.baropharm.com/products/202512/1766121243228.png)
![[아워팜] CJ웰케어, 바이오코어 1000억 유산균](https://i.baropharm.com/products/202512/1765955416559.png)
![[아워팜] 에너지 바로 충전, 바로콤](https://i.baropharm.com/products/202512/1764922282624.png)
![[아워팜] 우리아이 맞춤설계, 바로타민 kids 엘더베리맛](https://i.baropharm.com/products/8eae7689-61be-4b71-9608-05364b05ea12.png)
![[휴온스 ] 비듬을 한번에, 니조랄 2%액](https://i.baropharm.com/products/478a284d-4361-4b4a-8a00-8bab80f34319.png?label=PLAN_01)
![[아워팜] 건강한 힘, 바로바이오틱스 kids 비피더스 50억](https://i.baropharm.com/products/202511/1763106585375.png)
![[레킷코리아] 목 아플 때, 스트렙실 허니&레몬 트로키 12정](https://i.baropharm.com/products/202502/1739520767049.png?label=PLAN_01)
![[켄뷰] 오리지널 폼타입, 로게인5%폼에어로졸60g](https://i.baropharm.com/products/dc84d96e-d0b4-46bc-bcc8-d62016406fe4.png)
