총 41건
-
 불붙은 gMG 시장…한독, '비브가트' 급여도전 채비[데일리팜=황병우 기자] 한독의 전신중증근무력증(gMG) 치료제 '비브가트(에프가티지모드알파)'가 경쟁약의 급여 진입으로 전략적 갈림길에 섰다. 희귀질환 치료제 특성상 급여 확보가 필수인 가운데, 한독은 기전 차별성을 무기로 빠른 급여 도전에 나설 채비를 서두르고 있다.비브가트 제품사진한독은 지난 1월 항아세틸콜린(AChR) 수용체 항체 양성인 전신중증근무력증(Generalized Myasthenia Gravis) 성인 환자의 치료에 사용하는 수입 희귀의약품 비브가트를 식품의약품안전처로부터 허가를 받았다.전신중증근무력증은 신경근 전달 장애로 인해 발생하는 만성 희귀자가면역질환으로, 환자의 약 85%가 아세틸콜린 수용체의 자가항체를 가지고 있다.이 항체가 수용체에 결합하면 보체계가 활성화되어 시냅스 후막이 파괴되고, 이러한 구조적 손상이 신경에서 근육으로 전달되는 신호를 약화시켜 신경근 전달 장애를 초래한다.비브가트는 체내 항체 IgG 항상성에 특이적이며, IgG가 리소좀에 의해 분해되지 않도록 하는 신생아 Fc 수용체(FcRn)에 자가항체 IgG가 결합하는 것을 막아 자가항체의 분해를 촉진함으로써, 자가항체로 매개된 중증근무력증 환자에서 치료 효과를 나타낸다.특히 FcRn에 결합하는 새로운 기전의 치료제로서 국내 최초로 허가되면서 향후 성인 중증근무력증 환자의 치료제 선택 폭이 넓어질 것으로 기대를 모으고 있다.그러나 12월 1일부터 한국아스트라제네카의 울토미리스가 전신중증근무력증 적응증에 대해 급여를 확대하면서 시장 상황이 급변하는 중이다.울토미리스 제품사진아스트라제네카는 C5억제제 울토미리스(라불리주맙)가 12월부터 항아세틸콜린 수용체 항체 양성인 전신중증근무력증 성인 환자에서 건강보험 급여가 적용됐다고 밝혔다.울토미리스 치료에 앞서 2가지 이상의 비스테로이드성 면역억제제를 투여한 이후 등 후속 옵션으로 허가받아 급여기준이 제한적이라는 평가를 받고 있지만 빠르게 급여에 진입했다는 측면에서 임상현장의 관심도 큰 상태다.한독의 비브가트는 2023년 아르젠엑스(argenx)와 국내 독점공급 계약을 체결해 허가 등록 및 급여, 독점유통을 담당하는 제품이다.회사에 따르면 올해 1월 허가를 받은 만큼 다음 순서인 급여 논의를 준비 중이다. 다만, 아직 건강보험심사평가원에 본격적인 급여 절차를 밟기 위한 서류를 제출하지는 않은 상태다.경쟁약의 급여 진입으로 급여의 속도도 중요해졌지만 새로운 기전의 치료제인 만큼 신중한게 접근한다는 입장이다.한독 관계자는 "같은 적응증의 치료제가 있는 만큼 내부적으로도 울토미리스의 급여 과정을 예의주시하고 있었다"며 "같은 적응증에서 급여를 받은 만큼 비브가트의 급여 도전에도 긍정적인 면이 있다고 본다"고 밝혔다.그는 이어 "다만 울토미리스는 기존에 다른 적응증에 급여가 적용되고 있는 상태에서 적응 증이 확대된 만큼 급여 트랙이 다르다"며 "비브가트는 신약으로 처음 급여를 받는 만큼 시간이 필요한 상황이다"고 말했다.즉, 울토미리스의 전신중증근무력증 급여 적용이 시장 경쟁을 예고하면서도 급여허들을 낮추는 양면의 모습이 있다는 해석이다.하지만 한독 입장에서는 급여를 여유있게 준비할 수 있는 상황은 아니다.울토미리스외에도 한국유씨비의 질브리스큐(질루코플란)와 리스티고(로자놀릭시주맙)가 각각 지난 2024년 11월과 올해 4월 허가를 받은 상태다.질브리스큐는 울토미리스와 같은 기전을 가지고 있으며, 리스티고는 비브가트와 똑같이 FcRn에 결합하는 기전을 가지고 있다.UCB제약이 최근 한국에서 적극적으로 허가와 급여 진입을 노리고 있는 만큼 한독 역시 급여 진입에 보다 속도를 낼 필요성도 존재한다는 의미다.한독 관계자는 "비브가트가 최대한 성공적으로 급여를 적용받을 수 있도록 적극적으로 방법을 살펴보고 있는 중이다"며 "희귀질환 치료제는 어떤 조건으로 급여를 받는지가 중요한 만큼 환자들에게 최대한 도움이 될 수 있도록 시기와 트랙, 급여조건을 살펴보고 있는 중이다"고 덧붙였다.2025-12-08 12:05:56황병우 기자
불붙은 gMG 시장…한독, '비브가트' 급여도전 채비[데일리팜=황병우 기자] 한독의 전신중증근무력증(gMG) 치료제 '비브가트(에프가티지모드알파)'가 경쟁약의 급여 진입으로 전략적 갈림길에 섰다. 희귀질환 치료제 특성상 급여 확보가 필수인 가운데, 한독은 기전 차별성을 무기로 빠른 급여 도전에 나설 채비를 서두르고 있다.비브가트 제품사진한독은 지난 1월 항아세틸콜린(AChR) 수용체 항체 양성인 전신중증근무력증(Generalized Myasthenia Gravis) 성인 환자의 치료에 사용하는 수입 희귀의약품 비브가트를 식품의약품안전처로부터 허가를 받았다.전신중증근무력증은 신경근 전달 장애로 인해 발생하는 만성 희귀자가면역질환으로, 환자의 약 85%가 아세틸콜린 수용체의 자가항체를 가지고 있다.이 항체가 수용체에 결합하면 보체계가 활성화되어 시냅스 후막이 파괴되고, 이러한 구조적 손상이 신경에서 근육으로 전달되는 신호를 약화시켜 신경근 전달 장애를 초래한다.비브가트는 체내 항체 IgG 항상성에 특이적이며, IgG가 리소좀에 의해 분해되지 않도록 하는 신생아 Fc 수용체(FcRn)에 자가항체 IgG가 결합하는 것을 막아 자가항체의 분해를 촉진함으로써, 자가항체로 매개된 중증근무력증 환자에서 치료 효과를 나타낸다.특히 FcRn에 결합하는 새로운 기전의 치료제로서 국내 최초로 허가되면서 향후 성인 중증근무력증 환자의 치료제 선택 폭이 넓어질 것으로 기대를 모으고 있다.그러나 12월 1일부터 한국아스트라제네카의 울토미리스가 전신중증근무력증 적응증에 대해 급여를 확대하면서 시장 상황이 급변하는 중이다.울토미리스 제품사진아스트라제네카는 C5억제제 울토미리스(라불리주맙)가 12월부터 항아세틸콜린 수용체 항체 양성인 전신중증근무력증 성인 환자에서 건강보험 급여가 적용됐다고 밝혔다.울토미리스 치료에 앞서 2가지 이상의 비스테로이드성 면역억제제를 투여한 이후 등 후속 옵션으로 허가받아 급여기준이 제한적이라는 평가를 받고 있지만 빠르게 급여에 진입했다는 측면에서 임상현장의 관심도 큰 상태다.한독의 비브가트는 2023년 아르젠엑스(argenx)와 국내 독점공급 계약을 체결해 허가 등록 및 급여, 독점유통을 담당하는 제품이다.회사에 따르면 올해 1월 허가를 받은 만큼 다음 순서인 급여 논의를 준비 중이다. 다만, 아직 건강보험심사평가원에 본격적인 급여 절차를 밟기 위한 서류를 제출하지는 않은 상태다.경쟁약의 급여 진입으로 급여의 속도도 중요해졌지만 새로운 기전의 치료제인 만큼 신중한게 접근한다는 입장이다.한독 관계자는 "같은 적응증의 치료제가 있는 만큼 내부적으로도 울토미리스의 급여 과정을 예의주시하고 있었다"며 "같은 적응증에서 급여를 받은 만큼 비브가트의 급여 도전에도 긍정적인 면이 있다고 본다"고 밝혔다.그는 이어 "다만 울토미리스는 기존에 다른 적응증에 급여가 적용되고 있는 상태에서 적응 증이 확대된 만큼 급여 트랙이 다르다"며 "비브가트는 신약으로 처음 급여를 받는 만큼 시간이 필요한 상황이다"고 말했다.즉, 울토미리스의 전신중증근무력증 급여 적용이 시장 경쟁을 예고하면서도 급여허들을 낮추는 양면의 모습이 있다는 해석이다.하지만 한독 입장에서는 급여를 여유있게 준비할 수 있는 상황은 아니다.울토미리스외에도 한국유씨비의 질브리스큐(질루코플란)와 리스티고(로자놀릭시주맙)가 각각 지난 2024년 11월과 올해 4월 허가를 받은 상태다.질브리스큐는 울토미리스와 같은 기전을 가지고 있으며, 리스티고는 비브가트와 똑같이 FcRn에 결합하는 기전을 가지고 있다.UCB제약이 최근 한국에서 적극적으로 허가와 급여 진입을 노리고 있는 만큼 한독 역시 급여 진입에 보다 속도를 낼 필요성도 존재한다는 의미다.한독 관계자는 "비브가트가 최대한 성공적으로 급여를 적용받을 수 있도록 적극적으로 방법을 살펴보고 있는 중이다"며 "희귀질환 치료제는 어떤 조건으로 급여를 받는지가 중요한 만큼 환자들에게 최대한 도움이 될 수 있도록 시기와 트랙, 급여조건을 살펴보고 있는 중이다"고 덧붙였다.2025-12-08 12:05:56황병우 기자 -
 비타민D·칼슘 복합제, 골다공증에 급여...27품목 등재[데일리팜=정흥준 기자] 비타민D·칼슘 복합제가 골다공증에 급여 기준이 신설되면서, 내달 27개 품목이 급여 등재된다.광동칼디정, 칼앤디정, 칼엠디정 등 27개 품목이 상한액 88원으로 급여 목록에 이름을 올릴 예정이다.또 척수소뇌변성증 치료제 씨트렐린구강붕해정과 쿠싱병치료제 이스투리사필름코팅정이 12월 급여 등재된다. 시신경척수염 치료제 울토미리스는 전신중증근무력증으로 급여 확대된다.20일 복지부 요양급여 적용기준 개정고시에 따르면, 내달 급여기준이 3개 신설되고 8개 항목이 변경된다.먼저 칼슘 및 비타민D 복합경구제는 골다공증에 요양급여 기준이 신설됐다. 국내 허가사항과 교과서, 가이드라인과 학회 의견 등을 참조했다.한미약품 칼엠디정, 광동제약 광동칼디정, 엔비케이제약 칼앤디정, 옵투스제약 칼디본정 등 27개 품목이 급여 등재된다.또 씨트렐린구강붕해정은 ‘유전자 검사 또는 Brain MRI 검사, CT 검사 등으로 척수소뇌변성증에 의한 운동실조증으로 진단된 20세 이상의 환자’에게 급여가 적용된다. 단, K-SARA 20점 미만으로 보행이 가능한 경우다.이스투리사필름코팅정은 ‘뇌하수체 수술이 불가능하거나, 수술 후 충분한 효과를 얻지 못한 성인 쿠싱병 환자’를 대상으로 급여기준이 신설됐다. 최초 투여 전 4주 이내 실시한 평균 24시간 소변 유리코티졸이 정상 상한선의 1.3배를 초과하는 경우에 한해서다.급여가 확대 적용되는 품목들도 다수 있다. IL-17A 억제제인 코센틱스센소레디펜은 화농성 한선염에 급여 기준이 마련된다. 최초 진단 후 1년 이상 경과한 18세 이상 성인이며, ▲2개 이상의 각기 다른 부위에 병변이 있고, 농양과 염증성 결절 수의 합이 3개 이상 ▲항생제로 3개월 이상 치료했으나 치료효과가 미흡하거나 부작용 등으로 치료를 중단한 중증이어야 한다.보톡스주는 소아 신경인성 배뇨근 과활동성에 급여가 확대된다. 5세 이상-18세 미만 방광기능환자 중 적절한 보존요법(행동치료)과 항콜린제 투여에 실패한 신경인성 배뇨근 과활동성인 경우 적용된다.울토미리스는 전신 중증근무력증에 급여 기준이 신설됐다. 항아세틸콜린수용체(AChR) 항체 양성인 전신 중증근무력증 성인 환자이면서 조건에 해당되는 경우 급여 적용된다.또 레미케이드는 ‘불응성 가와사키병에 Infliximab 제제 투여용량이 5mg/kg에서 5~10mg/kg로 급여기준이 확대된다.이외에도 고혈압+고지혈증 복합경구제가 추가됨에 따라 기존 급여 기준에 대상 약제가 추가됐다.2025-11-20 11:13:14정흥준
비타민D·칼슘 복합제, 골다공증에 급여...27품목 등재[데일리팜=정흥준 기자] 비타민D·칼슘 복합제가 골다공증에 급여 기준이 신설되면서, 내달 27개 품목이 급여 등재된다.광동칼디정, 칼앤디정, 칼엠디정 등 27개 품목이 상한액 88원으로 급여 목록에 이름을 올릴 예정이다.또 척수소뇌변성증 치료제 씨트렐린구강붕해정과 쿠싱병치료제 이스투리사필름코팅정이 12월 급여 등재된다. 시신경척수염 치료제 울토미리스는 전신중증근무력증으로 급여 확대된다.20일 복지부 요양급여 적용기준 개정고시에 따르면, 내달 급여기준이 3개 신설되고 8개 항목이 변경된다.먼저 칼슘 및 비타민D 복합경구제는 골다공증에 요양급여 기준이 신설됐다. 국내 허가사항과 교과서, 가이드라인과 학회 의견 등을 참조했다.한미약품 칼엠디정, 광동제약 광동칼디정, 엔비케이제약 칼앤디정, 옵투스제약 칼디본정 등 27개 품목이 급여 등재된다.또 씨트렐린구강붕해정은 ‘유전자 검사 또는 Brain MRI 검사, CT 검사 등으로 척수소뇌변성증에 의한 운동실조증으로 진단된 20세 이상의 환자’에게 급여가 적용된다. 단, K-SARA 20점 미만으로 보행이 가능한 경우다.이스투리사필름코팅정은 ‘뇌하수체 수술이 불가능하거나, 수술 후 충분한 효과를 얻지 못한 성인 쿠싱병 환자’를 대상으로 급여기준이 신설됐다. 최초 투여 전 4주 이내 실시한 평균 24시간 소변 유리코티졸이 정상 상한선의 1.3배를 초과하는 경우에 한해서다.급여가 확대 적용되는 품목들도 다수 있다. IL-17A 억제제인 코센틱스센소레디펜은 화농성 한선염에 급여 기준이 마련된다. 최초 진단 후 1년 이상 경과한 18세 이상 성인이며, ▲2개 이상의 각기 다른 부위에 병변이 있고, 농양과 염증성 결절 수의 합이 3개 이상 ▲항생제로 3개월 이상 치료했으나 치료효과가 미흡하거나 부작용 등으로 치료를 중단한 중증이어야 한다.보톡스주는 소아 신경인성 배뇨근 과활동성에 급여가 확대된다. 5세 이상-18세 미만 방광기능환자 중 적절한 보존요법(행동치료)과 항콜린제 투여에 실패한 신경인성 배뇨근 과활동성인 경우 적용된다.울토미리스는 전신 중증근무력증에 급여 기준이 신설됐다. 항아세틸콜린수용체(AChR) 항체 양성인 전신 중증근무력증 성인 환자이면서 조건에 해당되는 경우 급여 적용된다.또 레미케이드는 ‘불응성 가와사키병에 Infliximab 제제 투여용량이 5mg/kg에서 5~10mg/kg로 급여기준이 확대된다.이외에도 고혈압+고지혈증 복합경구제가 추가됨에 따라 기존 급여 기준에 대상 약제가 추가됐다.2025-11-20 11:13:14정흥준 -
 울토미리스 '시신경척수염·중증근무력증' 잇단 급여 호재[데일리팜=정흥준 기자] 한국아스트라제네카의 울토미리스(라부리주맙)가 이달 시신경척수염 급여 적용에 이어, 내달 중증근무력증까지 급여 범위를 확대한다.특히 중증근무력증은 복지부의 급여 적용 요청이 있어 지난 6일 약제급여평가위원회에서 별도 안건으로 논의됐다.12일 업계 관계자에 따르면 울토미리스는 약평위 통과로 12월 1일부터 ‘항아세틸콜린 수용체(AChR) 항체 양성인 전신성 중증 근무력증’에 급여 적용을 받는다.약평위 공개된 회의 자료에는 제외됐지만, 별도 추가 안건으로 논의가 이뤄졌다. 복지부의 중증근무력증 치료제 급여 적용 요청이 배경이 된 것으로 알려졌다.올해 복지부 국정감사에서는 중증근무력증을 포함한 희귀중증질환의 치료 접근성에 대한 지적이 있었다.서영석 더불어민주당 의원이 복지부로부터 받은 자료에 따르면, 중증근무력증 치료제 중 급여 적용 약제가 없는 상황이다.이에 복지부는 “보험 적용이 시급한 희귀질환 치료제는 현장 의견을 통해 현황을 지속 파악하고 있다. 의견을 반영해 제도 개선하도록 노력하겠다”는 답변을 내놨었다.이번 약평위 안건 추가와 심의 통과에는 국정감사 지적과 정부의 접근성 강화 방침이 영향을 미친 것으로 보인다.울토미리스는 이달 1일부터 ‘항아쿠아포린-4(AQP-4) 항체 양성인 시신경척수염범주질환(NMOSD) 치료’ 적응증으로 급여가 적용되고 있다. 대상 환자는 항아쿠아포린-4(이하 항AQP-4) 항체 양성인 만 18세 이상 NMOSD 환자다.울토미리스는 그동안 환자단체와 국회청원 등을 통해 급여 적용 요구가 이어졌던 약제다. 11~12월에 거쳐 급여 범위 확대가 이뤄지면서 향후 처방 환자가 크게 늘어날 전망이다.2025-11-12 11:41:15정흥준
울토미리스 '시신경척수염·중증근무력증' 잇단 급여 호재[데일리팜=정흥준 기자] 한국아스트라제네카의 울토미리스(라부리주맙)가 이달 시신경척수염 급여 적용에 이어, 내달 중증근무력증까지 급여 범위를 확대한다.특히 중증근무력증은 복지부의 급여 적용 요청이 있어 지난 6일 약제급여평가위원회에서 별도 안건으로 논의됐다.12일 업계 관계자에 따르면 울토미리스는 약평위 통과로 12월 1일부터 ‘항아세틸콜린 수용체(AChR) 항체 양성인 전신성 중증 근무력증’에 급여 적용을 받는다.약평위 공개된 회의 자료에는 제외됐지만, 별도 추가 안건으로 논의가 이뤄졌다. 복지부의 중증근무력증 치료제 급여 적용 요청이 배경이 된 것으로 알려졌다.올해 복지부 국정감사에서는 중증근무력증을 포함한 희귀중증질환의 치료 접근성에 대한 지적이 있었다.서영석 더불어민주당 의원이 복지부로부터 받은 자료에 따르면, 중증근무력증 치료제 중 급여 적용 약제가 없는 상황이다.이에 복지부는 “보험 적용이 시급한 희귀질환 치료제는 현장 의견을 통해 현황을 지속 파악하고 있다. 의견을 반영해 제도 개선하도록 노력하겠다”는 답변을 내놨었다.이번 약평위 안건 추가와 심의 통과에는 국정감사 지적과 정부의 접근성 강화 방침이 영향을 미친 것으로 보인다.울토미리스는 이달 1일부터 ‘항아쿠아포린-4(AQP-4) 항체 양성인 시신경척수염범주질환(NMOSD) 치료’ 적응증으로 급여가 적용되고 있다. 대상 환자는 항아쿠아포린-4(이하 항AQP-4) 항체 양성인 만 18세 이상 NMOSD 환자다.울토미리스는 그동안 환자단체와 국회청원 등을 통해 급여 적용 요구가 이어졌던 약제다. 11~12월에 거쳐 급여 범위 확대가 이뤄지면서 향후 처방 환자가 크게 늘어날 전망이다.2025-11-12 11:41:15정흥준 -
 '울토미리스' 급여기준 완화…"aHUS 치료 접근성 개선"김명규 고대안암병원 신장내과 교수 [데일리팜=손형민 기자] 비정형 용혈성 요독증후군(aHUS)에서 C5 보체 억제제의 보험급여 기준이 이달부터 완화됐다. 그간 사전심의를 거쳐야하는 등 까다로운 급여조건이 개선된 만큼 환자 접근성이 향상될 것으로 기대하고 있다.24일 한국아스트라제네카는 웨스틴 서울 파르나스호텔에서 '울토미리스(라불리주맙)'의 aHUS에 대한 급여 기준 완화를 기념하는 간담회를 개최했다.울토미리스는 기존 '솔리리스(에쿨리주맙)' 대비 반감기를 약 4배 연장한 차세대 C5 보체 억제제다. 솔리리스는 2주 간격으로 투여가 필요한 반면, 울토미리스는 8주로 투여 간격을 늘려 치료 편의성이 개선됐다.aHUS는 면역 시스템의 보체가 유전적 결함으로 인해 과활성화되며 혈전성 미세혈관병증을 유발하는 급성 희귀질환이다. 이로 인해 여러 장기 특히 신장에 심각한 손상을 초래할 수 있다. aHUS는 용혈 요독증후군이 대장균과 관련 없이 발생하는 경우를 가리킨다.세균 표피에서 보체 5번이 활성화되면 세포막 공격 복합체가 생성돼 세포막에 구멍이 생기게 된다. 정상적인 면역쳬계인 보체 활성화 과정이 계속되게 되면 혈관내피세포에 문제가 생겨 관련 질환이 발생하게 된다. 울토미리스는 이를 억제하는 기전을 갖고 있다.진단, 투여 요건 확대로 적시 치료 가능해져울토미리스는 지난 1월 혈전성 미세혈관병증(TMA)과 신장 손상을 동반한 aHUS 환자에서 건강보험급여를 적용 받게됐다.다만 울토미리스는 모두 사전심의제도를 통해 승인된 환자들만 사용이 가능했다. 이에 적절한 투약시기를 놓쳐 환자의 상태가 악화될 수 있는 만큼, 의료진들은 사후심사로 전환하는 등 급여 조건 개선이 필요하다는 의견이 제기된 바 있다.실제로 aHUS 사전심의제 시행 이래로 평균 급여 승인율은 18%(2018년 7월~2025년 8월까지 심의 사례 기준)에 그치는 등 치료 적기를 놓치는 경우가 많았다.이달 1일부터 적용된 개정안은 aHUS 환자의 진단과 투여 요건을 확대해 치료 지연을 최소화했다. 급여 치료효과 평가를 명확하게 해 치료 지속성을 기대할 수 있다는 게 전문가의 평가다.aHUS 급여기준 개정안 급여 개정안을 세부적으로 살펴보면, TMA 활성 여부를 판단하는 혈액학적 기준이 5개 지표 중 혈소판 감소를 포함한 3개 이상 충족으로 명확히 정리됐다.또 ADAMTS-13 활성 10% 이상을 포함한 투여 대상 기준을 충족하는 경우 급여를 인정하며, 검사 결과 확인 전이라도 혈소판 수 150×10⁹/L 이상이면 사전신청서 제출 후 즉시 투여가 가능하고 심의 결과 통보 전까지 투여분을 급여로 인정한다.여기에 aHUS로 인한 말기 신부전으로 신장이식 진행 시, 이식 전후 치료가 필요할 경우 사례별로 인정하도록 명시돼 새로운 치료경로가 생겨났다. 기존 솔리리스에서 울토미리스의 교체 투여 급여 인정 기준도 명확히 규정됐다.김명규 고대안암병원 신장내과 교수는 "aHUS는 48시간 이내에 말기 신부전과 장기 손상으로 악화될 수 있어 치료 타이밍이 예후에 큰 영향을 미친다"라며 "이번 개정된 급여 기준은 해외 사례를 많이 참고해 고위험군의 지속투여 근거가 강화됐다. 신속하게 치료 전략을 설계할 수 있는 환경이 마련됐다"라고 평가했다.2025-10-24 12:08:51손형민
'울토미리스' 급여기준 완화…"aHUS 치료 접근성 개선"김명규 고대안암병원 신장내과 교수 [데일리팜=손형민 기자] 비정형 용혈성 요독증후군(aHUS)에서 C5 보체 억제제의 보험급여 기준이 이달부터 완화됐다. 그간 사전심의를 거쳐야하는 등 까다로운 급여조건이 개선된 만큼 환자 접근성이 향상될 것으로 기대하고 있다.24일 한국아스트라제네카는 웨스틴 서울 파르나스호텔에서 '울토미리스(라불리주맙)'의 aHUS에 대한 급여 기준 완화를 기념하는 간담회를 개최했다.울토미리스는 기존 '솔리리스(에쿨리주맙)' 대비 반감기를 약 4배 연장한 차세대 C5 보체 억제제다. 솔리리스는 2주 간격으로 투여가 필요한 반면, 울토미리스는 8주로 투여 간격을 늘려 치료 편의성이 개선됐다.aHUS는 면역 시스템의 보체가 유전적 결함으로 인해 과활성화되며 혈전성 미세혈관병증을 유발하는 급성 희귀질환이다. 이로 인해 여러 장기 특히 신장에 심각한 손상을 초래할 수 있다. aHUS는 용혈 요독증후군이 대장균과 관련 없이 발생하는 경우를 가리킨다.세균 표피에서 보체 5번이 활성화되면 세포막 공격 복합체가 생성돼 세포막에 구멍이 생기게 된다. 정상적인 면역쳬계인 보체 활성화 과정이 계속되게 되면 혈관내피세포에 문제가 생겨 관련 질환이 발생하게 된다. 울토미리스는 이를 억제하는 기전을 갖고 있다.진단, 투여 요건 확대로 적시 치료 가능해져울토미리스는 지난 1월 혈전성 미세혈관병증(TMA)과 신장 손상을 동반한 aHUS 환자에서 건강보험급여를 적용 받게됐다.다만 울토미리스는 모두 사전심의제도를 통해 승인된 환자들만 사용이 가능했다. 이에 적절한 투약시기를 놓쳐 환자의 상태가 악화될 수 있는 만큼, 의료진들은 사후심사로 전환하는 등 급여 조건 개선이 필요하다는 의견이 제기된 바 있다.실제로 aHUS 사전심의제 시행 이래로 평균 급여 승인율은 18%(2018년 7월~2025년 8월까지 심의 사례 기준)에 그치는 등 치료 적기를 놓치는 경우가 많았다.이달 1일부터 적용된 개정안은 aHUS 환자의 진단과 투여 요건을 확대해 치료 지연을 최소화했다. 급여 치료효과 평가를 명확하게 해 치료 지속성을 기대할 수 있다는 게 전문가의 평가다.aHUS 급여기준 개정안 급여 개정안을 세부적으로 살펴보면, TMA 활성 여부를 판단하는 혈액학적 기준이 5개 지표 중 혈소판 감소를 포함한 3개 이상 충족으로 명확히 정리됐다.또 ADAMTS-13 활성 10% 이상을 포함한 투여 대상 기준을 충족하는 경우 급여를 인정하며, 검사 결과 확인 전이라도 혈소판 수 150×10⁹/L 이상이면 사전신청서 제출 후 즉시 투여가 가능하고 심의 결과 통보 전까지 투여분을 급여로 인정한다.여기에 aHUS로 인한 말기 신부전으로 신장이식 진행 시, 이식 전후 치료가 필요할 경우 사례별로 인정하도록 명시돼 새로운 치료경로가 생겨났다. 기존 솔리리스에서 울토미리스의 교체 투여 급여 인정 기준도 명확히 규정됐다.김명규 고대안암병원 신장내과 교수는 "aHUS는 48시간 이내에 말기 신부전과 장기 손상으로 악화될 수 있어 치료 타이밍이 예후에 큰 영향을 미친다"라며 "이번 개정된 급여 기준은 해외 사례를 많이 참고해 고위험군의 지속투여 근거가 강화됐다. 신속하게 치료 전략을 설계할 수 있는 환경이 마련됐다"라고 평가했다.2025-10-24 12:08:51손형민 -
 NMOSD 급여확대 잇단 요구...국감서 기준 개선 재점화[데일리팜=정흥준 기자] 시신경척수염(NMOSD) 치료 접근성 강화를 위한 급여 개선 요구가 올해 국감장에서 재점화될 전망이다.17일 건강보험심사평가원 국정감사에서 NMOSD 환자가 참고인으로 출석해 신약 보험 급여 개선을 촉구할 예정이다.NMOSD는 신경 손상을 유발하는 중추신경계 자가면역질환으로, 한 번의 재발로 실명이나 마비 등의 장애로 이어질 수 있는 희귀질환이다.NMOSD 치료제는 급여와 기준 확대가 서서히 이뤄지고 있다. 지난 2023년 급여 등재된 한국로슈의 엔스프링(사트랄리주맙)은 올해 8월부터 증상 재발 기준이 완화되며 급여범위가 확대됐다.미쓰비시다나베파마코리아의 업리즈나주(이네빌리주맙)도 지난 2일 약평위에서 조건부 급여를 인정받아 약가협상을 앞두고 있다.한국아스트라제네카의 솔리리스(에쿨리주맙)는 작년 4월부터 급여적용이 이뤄졌고, 울토미리스(라불리주맙)는 작년 7월 적응증에 시신경척수염을 추가했지만 아직 급여화는 되지 않은 상황이다.보험 급여 확대로 치료 접근성이 조금씩 나아지고 있지만, 희귀질환 고가약 특성상 까다로운 급여 기준을 완화해달라는 요구는 끊이지 않고 있다. 지난 8월 NMOSD 환자 보호자는 국회청원을 통해 재발 기준 등 급여 허들을 낮추고, 재발률이 낮은 치료제를 급여화 해달라고 토로한 바 있다.서미화 더불어민주당 의원실이 지난 달 주최한 국회토론회에서도 재발을 조건으로 한 신약 급여 기준이 불합리하다는 지적이 나왔다. 또 재발을 예방할 수 있는 약제에는 접근성을 높여야 한다는 주장도 있었다.엔스프링, 솔리리스 모두 증상 재발이 급여 기준인데다가, 맙테라(리툭시맙)를 급여로 투여 받아야 한다는 전제 조건까지 달려있기 때문이다.이번 국정감사에서도 서미화 의원이 NMOSD 환자를 참고인으로 부른 만큼 급여 확대와 기준 개선 요구 목소리에 더욱 힘이 실릴 것으로 보인다.희귀질환 치료제에 대한 접근성 강화는 복지위 국정감사에 자주 올라오는 주요 쟁점 중 하나다. 작년 국정감사에서 저조한 급여 사전승인율을 지적 받았던 솔리리스는 이번 달부터 비정형 용혈성 요독 증후군(이하 AHUS) 사전심사 급여 적용 기준이 개선됐다.2025-10-12 15:40:17정흥준
NMOSD 급여확대 잇단 요구...국감서 기준 개선 재점화[데일리팜=정흥준 기자] 시신경척수염(NMOSD) 치료 접근성 강화를 위한 급여 개선 요구가 올해 국감장에서 재점화될 전망이다.17일 건강보험심사평가원 국정감사에서 NMOSD 환자가 참고인으로 출석해 신약 보험 급여 개선을 촉구할 예정이다.NMOSD는 신경 손상을 유발하는 중추신경계 자가면역질환으로, 한 번의 재발로 실명이나 마비 등의 장애로 이어질 수 있는 희귀질환이다.NMOSD 치료제는 급여와 기준 확대가 서서히 이뤄지고 있다. 지난 2023년 급여 등재된 한국로슈의 엔스프링(사트랄리주맙)은 올해 8월부터 증상 재발 기준이 완화되며 급여범위가 확대됐다.미쓰비시다나베파마코리아의 업리즈나주(이네빌리주맙)도 지난 2일 약평위에서 조건부 급여를 인정받아 약가협상을 앞두고 있다.한국아스트라제네카의 솔리리스(에쿨리주맙)는 작년 4월부터 급여적용이 이뤄졌고, 울토미리스(라불리주맙)는 작년 7월 적응증에 시신경척수염을 추가했지만 아직 급여화는 되지 않은 상황이다.보험 급여 확대로 치료 접근성이 조금씩 나아지고 있지만, 희귀질환 고가약 특성상 까다로운 급여 기준을 완화해달라는 요구는 끊이지 않고 있다. 지난 8월 NMOSD 환자 보호자는 국회청원을 통해 재발 기준 등 급여 허들을 낮추고, 재발률이 낮은 치료제를 급여화 해달라고 토로한 바 있다.서미화 더불어민주당 의원실이 지난 달 주최한 국회토론회에서도 재발을 조건으로 한 신약 급여 기준이 불합리하다는 지적이 나왔다. 또 재발을 예방할 수 있는 약제에는 접근성을 높여야 한다는 주장도 있었다.엔스프링, 솔리리스 모두 증상 재발이 급여 기준인데다가, 맙테라(리툭시맙)를 급여로 투여 받아야 한다는 전제 조건까지 달려있기 때문이다.이번 국정감사에서도 서미화 의원이 NMOSD 환자를 참고인으로 부른 만큼 급여 확대와 기준 개선 요구 목소리에 더욱 힘이 실릴 것으로 보인다.희귀질환 치료제에 대한 접근성 강화는 복지위 국정감사에 자주 올라오는 주요 쟁점 중 하나다. 작년 국정감사에서 저조한 급여 사전승인율을 지적 받았던 솔리리스는 이번 달부터 비정형 용혈성 요독 증후군(이하 AHUS) 사전심사 급여 적용 기준이 개선됐다.2025-10-12 15:40:17정흥준 -
 "NMOSD, 한 번 재발도 막아야" 울토미리스 급여 촉구[데일리팜=황병우 기자] 단 한 번의 재발로도 급격한 삶의 질 저하가 있는 시신경척수염 범주질환의 혁신 치료옵션이 등장하면서 접근성 개선에 대한 목소리가 커지고 있다.임상에서 73.5주간 재발 0건을 기록하는 등 기존 치료제의 한계를 보완한 울토미리스(라불리주맙)를 통한 패러다임 전환이 필요하다는 평가다.NMOS, '재발 억제' 중심의 치료 접근 필요성 대두 시신경척수염 범주질환(이하 NMOSD)은 신경 손상을 유발하는 중추신경계 자가면역질환이다. 시신경염과 척수염을 주요 특징으로 하는 이 질환은 환자의 90% 이상이 재발을 경험한다.시신경척수염 범주질환(NMOSD)은 재발이 반복될수록 신경 손상이 누적돼 하반신 마비, 실명 등을 겪을 수 있다.(자료사진)재발이 반복될수록 신경 손상이 누적되어 안구 통증, 시력 저하 등을 비롯해 척추 혹은 사지의 통증, 근력 약화, 보행 장애, 하반신 지각운동 장애 등의 증상이 나타날 수 있으며, 하반신 마비, 실명 등을 겪을 수 있다.NMOSD는 사회·경제 활동이 활발한 30~40대 여성에서 발생 빈도가 높다. 이로 인해 환자들은 직업 활동 중단, 대인 관계 축소, 활동 제약 등으로 사회적 단절을 겪게 되며, 이는 개인의 삶뿐 아니라 가정과 사회공동체 전반에도 부정적인 영향을 미칠 수 있다.실제 NMOSD 환자인 A씨의 경우 16세 무렵 처음 증상이 나타났지만, NMOSD라는 정확한 진단을 받기까지 5년이 걸렸다. 뒤늦게 NMOSD로 확진을 받은 이후 치료에 전념했지만, 잦은 재발의 후유증 탓에 지금도 일상생활에는 큰 제약이 따르고 있다는 설명이다.현재는 맙테라(리툭시맙) 기반 치료를 받고 있으나, 부작용 때문에 식사나 보행조차 가족의 도움 없이는 어렵다. 또한 장기간 면역억제 치료를 받으며 면역력이 크게 떨어져 감기, 폐렴, 장염에 자주 시달리고 있으며, 때때로 호흡곤란이나 쇼크로 응급 상황을 겪기도 한다.이처럼 NMOSD 치료에서는 재발을 조기에 차단하는 것이 핵심이다.국내외 전문가들 역시 "NMOSD는 한 번의 재발로도 심각한 손상을 남길 수 있는 만큼, 재발 자체를 예방하려는 치료 접근이 무엇보다 중요하다"고 강조하고 있다.울토미리스, NMOSD 치료에서 '무재발' 효과 확인이 가운데, 차세대 C5 보체 억제제 울토미리스가 NMOSD 환자를 대상으로 한 임상 3상 시험에서 무재발 효과를 확인하며 혁신적 치료 옵션으로 주목받고 있다.투약 반감기 개선으로 기존 치료제의 한계를 보완했을 뿐 아니라, 울토미리스 투여군(58명)에서 치료기간 동안 재발률 0%를 기록하며 NMOSD 치료 패러다임 전환 가능성을 제시했다.울토미리스 제품사진실제 울토미리스는 3상 임상인 CHAMPION-NMOSD 연구에서 울토미리스는 치료기간 동안(중앙값 기준 73.5주) 단 한 건의 재발도 발생하지 않았으며, 위약군 대비 재발 위험을 98.6% 감소시킨 것으로 나타났다.투약 간격 또한 주목받는 요소다. 울토미리스는 8주 간격 투여가 가능해, 2주 간격 치료가 필요했던 솔리리스 대비 투약 빈도 측면에서 환자의 치료 부담을 크게 줄일 수 있을 것으로 기대된다.김호진 국립암센터 신경과 교수는 "투약 간격은 단순히 병원 방문 횟수를 줄이는 것을 넘어 보행 및 시각 기능이 좋지 않은 환자들의 체력적인 소모와 병원 방문에 따른 추가 비용 절감을 기대할 수 있다"며 "이와 같은 치료 편의성 개선은 치료 부담을 줄여 환자의 삶의 질과 치료 순응도 향상에 도움을 줄 수 있을 것"이라고 설명했다.다만 울토미리스는 아직까지 건강보험 급여가 적용되지 않아 실제 치료 접근성에는 제한이 있는 상황이다.이에 의료 현장과 한국시신경척수염환우회를 중심으로 효과가 입증된 치료제에 대한 접근성이 보장되어야 한다는 요구가 점점 더 커지고 있다.환자 A 씨는 "매일매일 재발이 언제 올지 모른다는 불안감 속에 살아간다"며 "재발을 막아주는 치료제가 있다는 사실을 알지만, 보험이 적용되지 않는 현재로서는 치료를 시도하기조차 어려운 상황"이라고 말했다.한편, NMOSD에 대한 올바른 이해와 사회적 공감대 형성을 위해, 오는 9월 25일 국회의사당 의원회관 대회의실에서 Stay ZERO 콘서트가 개최될 예정이다.이번 콘서트는 ‘재발 없는 삶’을 염원하는 환자들의 목소리를 사회에 알리고, 재발 예방 치료의 중요성과 치료 접근성 개선 필요성에 대한 인식을 확산시키는 것을 목적으로 한다.2025-09-22 12:09:19황병우
"NMOSD, 한 번 재발도 막아야" 울토미리스 급여 촉구[데일리팜=황병우 기자] 단 한 번의 재발로도 급격한 삶의 질 저하가 있는 시신경척수염 범주질환의 혁신 치료옵션이 등장하면서 접근성 개선에 대한 목소리가 커지고 있다.임상에서 73.5주간 재발 0건을 기록하는 등 기존 치료제의 한계를 보완한 울토미리스(라불리주맙)를 통한 패러다임 전환이 필요하다는 평가다.NMOS, '재발 억제' 중심의 치료 접근 필요성 대두 시신경척수염 범주질환(이하 NMOSD)은 신경 손상을 유발하는 중추신경계 자가면역질환이다. 시신경염과 척수염을 주요 특징으로 하는 이 질환은 환자의 90% 이상이 재발을 경험한다.시신경척수염 범주질환(NMOSD)은 재발이 반복될수록 신경 손상이 누적돼 하반신 마비, 실명 등을 겪을 수 있다.(자료사진)재발이 반복될수록 신경 손상이 누적되어 안구 통증, 시력 저하 등을 비롯해 척추 혹은 사지의 통증, 근력 약화, 보행 장애, 하반신 지각운동 장애 등의 증상이 나타날 수 있으며, 하반신 마비, 실명 등을 겪을 수 있다.NMOSD는 사회·경제 활동이 활발한 30~40대 여성에서 발생 빈도가 높다. 이로 인해 환자들은 직업 활동 중단, 대인 관계 축소, 활동 제약 등으로 사회적 단절을 겪게 되며, 이는 개인의 삶뿐 아니라 가정과 사회공동체 전반에도 부정적인 영향을 미칠 수 있다.실제 NMOSD 환자인 A씨의 경우 16세 무렵 처음 증상이 나타났지만, NMOSD라는 정확한 진단을 받기까지 5년이 걸렸다. 뒤늦게 NMOSD로 확진을 받은 이후 치료에 전념했지만, 잦은 재발의 후유증 탓에 지금도 일상생활에는 큰 제약이 따르고 있다는 설명이다.현재는 맙테라(리툭시맙) 기반 치료를 받고 있으나, 부작용 때문에 식사나 보행조차 가족의 도움 없이는 어렵다. 또한 장기간 면역억제 치료를 받으며 면역력이 크게 떨어져 감기, 폐렴, 장염에 자주 시달리고 있으며, 때때로 호흡곤란이나 쇼크로 응급 상황을 겪기도 한다.이처럼 NMOSD 치료에서는 재발을 조기에 차단하는 것이 핵심이다.국내외 전문가들 역시 "NMOSD는 한 번의 재발로도 심각한 손상을 남길 수 있는 만큼, 재발 자체를 예방하려는 치료 접근이 무엇보다 중요하다"고 강조하고 있다.울토미리스, NMOSD 치료에서 '무재발' 효과 확인이 가운데, 차세대 C5 보체 억제제 울토미리스가 NMOSD 환자를 대상으로 한 임상 3상 시험에서 무재발 효과를 확인하며 혁신적 치료 옵션으로 주목받고 있다.투약 반감기 개선으로 기존 치료제의 한계를 보완했을 뿐 아니라, 울토미리스 투여군(58명)에서 치료기간 동안 재발률 0%를 기록하며 NMOSD 치료 패러다임 전환 가능성을 제시했다.울토미리스 제품사진실제 울토미리스는 3상 임상인 CHAMPION-NMOSD 연구에서 울토미리스는 치료기간 동안(중앙값 기준 73.5주) 단 한 건의 재발도 발생하지 않았으며, 위약군 대비 재발 위험을 98.6% 감소시킨 것으로 나타났다.투약 간격 또한 주목받는 요소다. 울토미리스는 8주 간격 투여가 가능해, 2주 간격 치료가 필요했던 솔리리스 대비 투약 빈도 측면에서 환자의 치료 부담을 크게 줄일 수 있을 것으로 기대된다.김호진 국립암센터 신경과 교수는 "투약 간격은 단순히 병원 방문 횟수를 줄이는 것을 넘어 보행 및 시각 기능이 좋지 않은 환자들의 체력적인 소모와 병원 방문에 따른 추가 비용 절감을 기대할 수 있다"며 "이와 같은 치료 편의성 개선은 치료 부담을 줄여 환자의 삶의 질과 치료 순응도 향상에 도움을 줄 수 있을 것"이라고 설명했다.다만 울토미리스는 아직까지 건강보험 급여가 적용되지 않아 실제 치료 접근성에는 제한이 있는 상황이다.이에 의료 현장과 한국시신경척수염환우회를 중심으로 효과가 입증된 치료제에 대한 접근성이 보장되어야 한다는 요구가 점점 더 커지고 있다.환자 A 씨는 "매일매일 재발이 언제 올지 모른다는 불안감 속에 살아간다"며 "재발을 막아주는 치료제가 있다는 사실을 알지만, 보험이 적용되지 않는 현재로서는 치료를 시도하기조차 어려운 상황"이라고 말했다.한편, NMOSD에 대한 올바른 이해와 사회적 공감대 형성을 위해, 오는 9월 25일 국회의사당 의원회관 대회의실에서 Stay ZERO 콘서트가 개최될 예정이다.이번 콘서트는 ‘재발 없는 삶’을 염원하는 환자들의 목소리를 사회에 알리고, 재발 예방 치료의 중요성과 치료 접근성 개선 필요성에 대한 인식을 확산시키는 것을 목적으로 한다.2025-09-22 12:09:19황병우 -
 경구용 PNH 신약 '파발타', 종합병원 처방권 진입[데일리팜=어윤호 기자] 먹는 PNH 신약 '파발타'가 종합병원 처방권에 진입하고 있다.관련 업계에 따르면 한국노바티스의 경구용 발작성혈색소뇨증(PNH, Paroxysmal Nocturnal Hemoglobinuria)치료제 파발타(입타코판)는 서울대병원을 비롯해 경북대병원, 원주세브란스병원, 충남대병원, 화순전남대병원 등 의료기관의 약사위원회(DC, Drug committee)를 통과했다.7월 보험급여 등재 전후로 조금씩 처방 영역을 넓혀가는 모습이다.PNH는 전 세계적으로 100만명 당 약 1.5명 정도가 발생하는 것으로 추정되는 희귀질환이다.이 질환의 치료는 그간 C5억제제에 의존했다. 2010년 '솔리리스(에쿨리주맙)'가 국내 처음 허가됐고, 2022년 '울토미리스(라불리주맙)'가 허가돼 PNH 치료에 사용돼 왔다. 두 치료옵션 모두 체내 면역에 관여하는 보체 시스템의 대체 경로 안에서 말단에 위치한 C5를 억제하는 기전인 C5 억제제이며 정맥주사제다.그러다 지난해 4월, C3 및 C3b에 결합해 보체연쇄반응을 억제하는 기전의 피하주사제 '엠파벨리(페그세타코플란)'가 허가됐고, 8월에는 B인자를 억제하는 기전의 경구제 파발타가 등장했다.C5 억제제의 기전적 한계로 남은 PNH 미충족 수요, 혈관 외 용혈(EVH)’ PNH는 적혈구에 유전적 결핍이 생기면서 시작되는데 이로 인해 혈관 내 용혈(IVH, Intravascular Hemolysis)과 혈관 외 용혈(EVH, Extravascular Hemolysis)이 발생한다.이런 용혈은 곧 혈전증, 골수부전을 야기해 생명을 위태롭게 만든다. 때문에 PNH 치료는 용혈을 조절하는 것이 중요한데 현재 PNH의 표준치료법인 C5 억제제는 IVH는 유의하게 조절하지만, 기전적으로 EVH는 조절하는데 한계가 있다.B인자억제제 파발타의 급여 등재에 관심이 모이는 이유다. B인자는 C5 뿐만 아니라 C3 및 C3b보다 대체 경로 내 상위에 존재하는 인자로 이를 억제할 경우 IVH 뿐만 아니라 EVH까지도 포괄적으로 조절할 수 있다.실제 파발타는 치료 경험이 없는 환자 대상에게 유효성을 보였다. 치료 경험이 없는 PNH 환자를 대상으로 한 APPOINT-PNH 연구에 따르면 환자 33명 중 19명은 적혈구 수혈 없이 헤모글로빈 수치가 12g/dL 이상에 도달했다.또한 92% 환자가 임상적으로 유의한 헤모글로빈 수 2g/dL 이상 증가를 보였으며, 수혈 없이 헤모글로빈 수치가 12g/dL 이상 지속된 환자는 63%였다. 연구 기간인 24주동안 헤모글로빈 수치가 지속적으로 증가하는 추세를 보였으며, 20주차부터는 헤모글로빈 정상화 수치에 도달해 24주 차까지 지속됐다. 또한 98%가 수혈 의존성을 극복했다.장준호 삼성서울병원 혈액내과 교수는 "C5 억제제가 처음 등장했을 당시, 전문가들은 PNH 치료의 패러다임이 전환됐다. 그러나 C5 억제제는 여전히 혈관 외 용혈(EVH)을 조절하는데 한계가 있다"고 말했다.아울러 "파발타는 PNH 치료의 또 한번의 패러다임 전환을 주도할 신약이다. B인자 억제라는 기전은 대체 경로의 상단에 위치한 B인자에 관여하기 때문에 혈관 내외 용혈을 모두 조절할 수 있으며 임상을 통해 고무적인 결과를 보였다"고 강조했다.2025-09-06 06:12:05어윤호
경구용 PNH 신약 '파발타', 종합병원 처방권 진입[데일리팜=어윤호 기자] 먹는 PNH 신약 '파발타'가 종합병원 처방권에 진입하고 있다.관련 업계에 따르면 한국노바티스의 경구용 발작성혈색소뇨증(PNH, Paroxysmal Nocturnal Hemoglobinuria)치료제 파발타(입타코판)는 서울대병원을 비롯해 경북대병원, 원주세브란스병원, 충남대병원, 화순전남대병원 등 의료기관의 약사위원회(DC, Drug committee)를 통과했다.7월 보험급여 등재 전후로 조금씩 처방 영역을 넓혀가는 모습이다.PNH는 전 세계적으로 100만명 당 약 1.5명 정도가 발생하는 것으로 추정되는 희귀질환이다.이 질환의 치료는 그간 C5억제제에 의존했다. 2010년 '솔리리스(에쿨리주맙)'가 국내 처음 허가됐고, 2022년 '울토미리스(라불리주맙)'가 허가돼 PNH 치료에 사용돼 왔다. 두 치료옵션 모두 체내 면역에 관여하는 보체 시스템의 대체 경로 안에서 말단에 위치한 C5를 억제하는 기전인 C5 억제제이며 정맥주사제다.그러다 지난해 4월, C3 및 C3b에 결합해 보체연쇄반응을 억제하는 기전의 피하주사제 '엠파벨리(페그세타코플란)'가 허가됐고, 8월에는 B인자를 억제하는 기전의 경구제 파발타가 등장했다.C5 억제제의 기전적 한계로 남은 PNH 미충족 수요, 혈관 외 용혈(EVH)’ PNH는 적혈구에 유전적 결핍이 생기면서 시작되는데 이로 인해 혈관 내 용혈(IVH, Intravascular Hemolysis)과 혈관 외 용혈(EVH, Extravascular Hemolysis)이 발생한다.이런 용혈은 곧 혈전증, 골수부전을 야기해 생명을 위태롭게 만든다. 때문에 PNH 치료는 용혈을 조절하는 것이 중요한데 현재 PNH의 표준치료법인 C5 억제제는 IVH는 유의하게 조절하지만, 기전적으로 EVH는 조절하는데 한계가 있다.B인자억제제 파발타의 급여 등재에 관심이 모이는 이유다. B인자는 C5 뿐만 아니라 C3 및 C3b보다 대체 경로 내 상위에 존재하는 인자로 이를 억제할 경우 IVH 뿐만 아니라 EVH까지도 포괄적으로 조절할 수 있다.실제 파발타는 치료 경험이 없는 환자 대상에게 유효성을 보였다. 치료 경험이 없는 PNH 환자를 대상으로 한 APPOINT-PNH 연구에 따르면 환자 33명 중 19명은 적혈구 수혈 없이 헤모글로빈 수치가 12g/dL 이상에 도달했다.또한 92% 환자가 임상적으로 유의한 헤모글로빈 수 2g/dL 이상 증가를 보였으며, 수혈 없이 헤모글로빈 수치가 12g/dL 이상 지속된 환자는 63%였다. 연구 기간인 24주동안 헤모글로빈 수치가 지속적으로 증가하는 추세를 보였으며, 20주차부터는 헤모글로빈 정상화 수치에 도달해 24주 차까지 지속됐다. 또한 98%가 수혈 의존성을 극복했다.장준호 삼성서울병원 혈액내과 교수는 "C5 억제제가 처음 등장했을 당시, 전문가들은 PNH 치료의 패러다임이 전환됐다. 그러나 C5 억제제는 여전히 혈관 외 용혈(EVH)을 조절하는데 한계가 있다"고 말했다.아울러 "파발타는 PNH 치료의 또 한번의 패러다임 전환을 주도할 신약이다. B인자 억제라는 기전은 대체 경로의 상단에 위치한 B인자에 관여하기 때문에 혈관 내외 용혈을 모두 조절할 수 있으며 임상을 통해 고무적인 결과를 보였다"고 강조했다.2025-09-06 06:12:05어윤호 -
 한독·JW중외 수입신약, 같은 질환 치료제로 내달 급여등재JW중외제약이 수입하는 타발리스와 한독이 수입하는 도프텔렛. 둘 다 ITP 치료제로 급여 적용된다. [데일리팜=이탁순 기자] 7월에 PNH(발작성 야간 혈색소뇨증) 경구 신약과 중증 아토피피부염 생물학적제제 신약, 면역 혈소판 감소증(ITP) 신약 등 4개 신약이 건강보험 급여가 적용돼 본격적으로 환자들에게 사용된다.복지부는 19일 PNH 치료 신약 파발타캡슐200mg(입타코판염산염수화물, 한국노바티스) 등 신약 4개 브랜드의 급여기준 신설을 예고했다. 급여 적용 시행일은 내달 1일이다.급여 등재되는 신약은 '파발타캡슐200mg'을 비롯해 중증아토피피부염 치료제 '엡글리스오토인젝터주250mg(레브리키주맙, 한국릴리)', 면역 혈소판 감소증(ITP) 치료제 '도프텔렛정20mg(아바트롬보팍말레산염, 한독)'과 '타발리스정100·150mg (포스타마티닙나트륨수화물, JW중외제약)'이다.파발타캡슐200mg은 발작성 야간 혈색소뇨증 경구 치료제로, 그간 사용된 주사제보다 편의성이 향상될 것으로 기대되고 있다. 더불어 용혈 조절 효과가 기존 C5 억제제(솔리리스, 울토미리스)보다 나아질 것으로 전망된다.PNH는 전 세계적으로 100만명 당 약 1.5명 정도가 발생하는 희귀질환이다. 그동안 치료제로는 C5억제제로 솔리리스(에쿨리주맙)와 울토미리스(라불리주맙)가 주로 사용돼 왔다. 작년 11월에는 C3 및 C3b에 결합해 보체연쇄반응을 억제하는 기전의 피하주사제 '엠파벨리(페그세타코플란, 한독)'도 급여 출시됐다.이번 경구신약 파발타의 급여 적용으로 환자들의 치료제 접근성 향상과 치료 효과 개선이 기대된다.엡글리스오토인젝터주250mg는 3년 이상 증상이 지속되는 성인(만 18세 이상) 및 청소년(만 12세-만 17세, 체중 40kg 이상) 만성 중증 아토피피부염 환자에 급여 적용된다.이 약은 '듀피젠트(두필루맙)', '아트랄자(트랄로키누맙)'에 이은 세번째 아토피피부염 치료 생물학적 제제이다.엡글리스는 3상 임상 연구를 통해 임상적 유효성 및 안전성 프로파일을 확인하며 국내 아토피피부염 환자들에게 1차 치료 옵션이 될 것으로 기대되고 있다.도프텔렛정과 타발리스정은 나란히 corticosteroid와 immunoglobulin에 불응인 성인 만성 면역 혈소판 감소증(ITP) 치료에 급여를 적용받게 된다.ITP는 면역체계가 혈소판을 바이러스로 오인해 공격하는 자가면역질환으로 혈소판 수치가 정상 범위 이하로 감소하면서 출혈 위험이 증가하는 질환이다. 이에 환자는 멍이 쉽게 들고 출혈이 잦으며 심한 경우 뇌출혈이나 위장 출혈로 이어질 수 있다.대한혈액학회 ITP 임상진료지침에 따르면 1차 치료제로 스테로이드와 면역글로불린이 권장, 만성 ITP 환자의 경우 2차 치료제로 비장절제술이나 혈소판 작용체 수용제(TPO-RA)가 사용되고 있다.한독과 JW중외제약 등 국내 제약사가 수입하는 희귀질환 신약이 나란히 급여 적용받으면서 시장에서 어떤 평가를 얻을지 업계 시선이 모아지고 있다.2025-06-19 23:05:02이탁순
한독·JW중외 수입신약, 같은 질환 치료제로 내달 급여등재JW중외제약이 수입하는 타발리스와 한독이 수입하는 도프텔렛. 둘 다 ITP 치료제로 급여 적용된다. [데일리팜=이탁순 기자] 7월에 PNH(발작성 야간 혈색소뇨증) 경구 신약과 중증 아토피피부염 생물학적제제 신약, 면역 혈소판 감소증(ITP) 신약 등 4개 신약이 건강보험 급여가 적용돼 본격적으로 환자들에게 사용된다.복지부는 19일 PNH 치료 신약 파발타캡슐200mg(입타코판염산염수화물, 한국노바티스) 등 신약 4개 브랜드의 급여기준 신설을 예고했다. 급여 적용 시행일은 내달 1일이다.급여 등재되는 신약은 '파발타캡슐200mg'을 비롯해 중증아토피피부염 치료제 '엡글리스오토인젝터주250mg(레브리키주맙, 한국릴리)', 면역 혈소판 감소증(ITP) 치료제 '도프텔렛정20mg(아바트롬보팍말레산염, 한독)'과 '타발리스정100·150mg (포스타마티닙나트륨수화물, JW중외제약)'이다.파발타캡슐200mg은 발작성 야간 혈색소뇨증 경구 치료제로, 그간 사용된 주사제보다 편의성이 향상될 것으로 기대되고 있다. 더불어 용혈 조절 효과가 기존 C5 억제제(솔리리스, 울토미리스)보다 나아질 것으로 전망된다.PNH는 전 세계적으로 100만명 당 약 1.5명 정도가 발생하는 희귀질환이다. 그동안 치료제로는 C5억제제로 솔리리스(에쿨리주맙)와 울토미리스(라불리주맙)가 주로 사용돼 왔다. 작년 11월에는 C3 및 C3b에 결합해 보체연쇄반응을 억제하는 기전의 피하주사제 '엠파벨리(페그세타코플란, 한독)'도 급여 출시됐다.이번 경구신약 파발타의 급여 적용으로 환자들의 치료제 접근성 향상과 치료 효과 개선이 기대된다.엡글리스오토인젝터주250mg는 3년 이상 증상이 지속되는 성인(만 18세 이상) 및 청소년(만 12세-만 17세, 체중 40kg 이상) 만성 중증 아토피피부염 환자에 급여 적용된다.이 약은 '듀피젠트(두필루맙)', '아트랄자(트랄로키누맙)'에 이은 세번째 아토피피부염 치료 생물학적 제제이다.엡글리스는 3상 임상 연구를 통해 임상적 유효성 및 안전성 프로파일을 확인하며 국내 아토피피부염 환자들에게 1차 치료 옵션이 될 것으로 기대되고 있다.도프텔렛정과 타발리스정은 나란히 corticosteroid와 immunoglobulin에 불응인 성인 만성 면역 혈소판 감소증(ITP) 치료에 급여를 적용받게 된다.ITP는 면역체계가 혈소판을 바이러스로 오인해 공격하는 자가면역질환으로 혈소판 수치가 정상 범위 이하로 감소하면서 출혈 위험이 증가하는 질환이다. 이에 환자는 멍이 쉽게 들고 출혈이 잦으며 심한 경우 뇌출혈이나 위장 출혈로 이어질 수 있다.대한혈액학회 ITP 임상진료지침에 따르면 1차 치료제로 스테로이드와 면역글로불린이 권장, 만성 ITP 환자의 경우 2차 치료제로 비장절제술이나 혈소판 작용체 수용제(TPO-RA)가 사용되고 있다.한독과 JW중외제약 등 국내 제약사가 수입하는 희귀질환 신약이 나란히 급여 적용받으면서 시장에서 어떤 평가를 얻을지 업계 시선이 모아지고 있다.2025-06-19 23:05:02이탁순 -
 PNH 새 치료옵션 풍년...'피아스카이' 국내 허가 임박[데일리팜=어윤호 기자] PNH 신약 '피아스카이'가 국내 시장 진입을 앞두고 있다.관련 업계에 따르면 한국로슈 발작성 야간혈색소뇨증(PNH, Paroxysmal Nocturnal Hemoglobinuria)치료제 피아스카이(크로발리맙)에 대한 식품의약품안전처의 막바지 허가 심사가 이뤄지고 있다. 하반기 내 정식 승인이 예상된다.이 약물은 2024녀 6월 미국 FDA 승인을 획득, 같은해 8월에는 유럽에서 상용화됐다. 또 국내에서는 지난해 2월 희귀의약품으로 지정되기도 했다.일본 쥬가이가 물질을 발굴해 로슈가 개발한 피아스카이는 새로운 C5 항체 저해제의 일종으로 소용량을 4주 간격으로 피하주사하면 혈액 속에서 재순환해 지속적으로 보체를 억제하는 기전을 갖고 있다.피아스카이는 PNH 환자를 대상으로 아스트라제네카의 '솔리리스(에쿨리주맙)'와 직접 비교한 중추적인 임상3상 COMMODORE2 연구를 통해 가능성을 확인했다.연구 결과, 4주마다 피하주사로 투여하는 크로발리맙이 질병을 조절한 것으로 나타났고, 현재 표준 치료제인 2주마다 정맥 투여하는 솔리리스와 비교했을 때 안전성이 비열등한 것으로 확인됐다.해당 임상에서 이상반응은 크로발리맙 투여군의 78%, 에쿨리주맙 투여군의 80%에서 발생했고 가장 흔한 이상반응은 주입 관련 반응이었다.또한 이와 별도로 이루어진 3상 COMMODORE1 연구에서 확보된 효능 및 안전성 데이터를 보면, 현재 허가를 취득해 사용 중인 C5저해제들에서 크로발리맙으로 전환한 PNH 환자들 역시 안정적인 유효성 프로파일을 보였다.한편 PNH 시장 경쟁은 앞으로 더욱 치열해질 전망이다. 아스트라제네카는 2023년 유럽, 2027년 미국 특허 만료를 앞둔 솔리리스의 후발 약물로 '울토미리스(라불리주맙)'를 시장에 내놓은 상황이다. 울토미리스는 2주마다 정맥주사하는 솔리리스 대비 투여 간격을 8주에 1회로 대폭 늘렸다.노바티스의 경우 경구용 PNH치료제 '파발타(입타코판)'의 미국에 이어 국내 허가를 획득했다. 파발타는 면역계 대체보체 경로에서 근위적으로 작용하는 B인자 억제제로 적혈구 파괴를 포괄적으로 제어한다. 이 약은 현재 국민건강보험공단과 약가협상을 진행중이며, 협상을 타결할 경우 보험급여 등재가 이뤄질 전망이다.여기에 삼성바이오에피스의 솔리리스 바이오시밀러 '에피스클리'가 국내 상용화가 이뤄져다. 이는 솔리리스 바이오시밀러 중 최초 국내 허가 사례로, 삼성바이오에피스는 지난해 유럽에서도 허가된 바 있다.장준호 삼성서울병원 혈액내과 교수는 "C5 억제제가 처음 등장했을 당시, 전문가들은 PNH 치료의 패러다임이 전환됐다고 평했다. 그러나 C5 억제제는 여전히 혈관 외 용혈(EVH)을 조절하는데 한계가 있다. 새로운 치료옵션에 대한 기대가 크다"고 말했다.2025-06-04 06:00:00어윤호
PNH 새 치료옵션 풍년...'피아스카이' 국내 허가 임박[데일리팜=어윤호 기자] PNH 신약 '피아스카이'가 국내 시장 진입을 앞두고 있다.관련 업계에 따르면 한국로슈 발작성 야간혈색소뇨증(PNH, Paroxysmal Nocturnal Hemoglobinuria)치료제 피아스카이(크로발리맙)에 대한 식품의약품안전처의 막바지 허가 심사가 이뤄지고 있다. 하반기 내 정식 승인이 예상된다.이 약물은 2024녀 6월 미국 FDA 승인을 획득, 같은해 8월에는 유럽에서 상용화됐다. 또 국내에서는 지난해 2월 희귀의약품으로 지정되기도 했다.일본 쥬가이가 물질을 발굴해 로슈가 개발한 피아스카이는 새로운 C5 항체 저해제의 일종으로 소용량을 4주 간격으로 피하주사하면 혈액 속에서 재순환해 지속적으로 보체를 억제하는 기전을 갖고 있다.피아스카이는 PNH 환자를 대상으로 아스트라제네카의 '솔리리스(에쿨리주맙)'와 직접 비교한 중추적인 임상3상 COMMODORE2 연구를 통해 가능성을 확인했다.연구 결과, 4주마다 피하주사로 투여하는 크로발리맙이 질병을 조절한 것으로 나타났고, 현재 표준 치료제인 2주마다 정맥 투여하는 솔리리스와 비교했을 때 안전성이 비열등한 것으로 확인됐다.해당 임상에서 이상반응은 크로발리맙 투여군의 78%, 에쿨리주맙 투여군의 80%에서 발생했고 가장 흔한 이상반응은 주입 관련 반응이었다.또한 이와 별도로 이루어진 3상 COMMODORE1 연구에서 확보된 효능 및 안전성 데이터를 보면, 현재 허가를 취득해 사용 중인 C5저해제들에서 크로발리맙으로 전환한 PNH 환자들 역시 안정적인 유효성 프로파일을 보였다.한편 PNH 시장 경쟁은 앞으로 더욱 치열해질 전망이다. 아스트라제네카는 2023년 유럽, 2027년 미국 특허 만료를 앞둔 솔리리스의 후발 약물로 '울토미리스(라불리주맙)'를 시장에 내놓은 상황이다. 울토미리스는 2주마다 정맥주사하는 솔리리스 대비 투여 간격을 8주에 1회로 대폭 늘렸다.노바티스의 경우 경구용 PNH치료제 '파발타(입타코판)'의 미국에 이어 국내 허가를 획득했다. 파발타는 면역계 대체보체 경로에서 근위적으로 작용하는 B인자 억제제로 적혈구 파괴를 포괄적으로 제어한다. 이 약은 현재 국민건강보험공단과 약가협상을 진행중이며, 협상을 타결할 경우 보험급여 등재가 이뤄질 전망이다.여기에 삼성바이오에피스의 솔리리스 바이오시밀러 '에피스클리'가 국내 상용화가 이뤄져다. 이는 솔리리스 바이오시밀러 중 최초 국내 허가 사례로, 삼성바이오에피스는 지난해 유럽에서도 허가된 바 있다.장준호 삼성서울병원 혈액내과 교수는 "C5 억제제가 처음 등장했을 당시, 전문가들은 PNH 치료의 패러다임이 전환됐다고 평했다. 그러나 C5 억제제는 여전히 혈관 외 용혈(EVH)을 조절하는데 한계가 있다. 새로운 치료옵션에 대한 기대가 크다"고 말했다.2025-06-04 06:00:00어윤호 -
 PNH 치료제 '피아스키', 최초의 월 1회 피하주사제3편: 피하주사 발작성 야간혈색소증 치료제, 피아스키(Crovalimab)'피아스키(PiaSky, pea-UH-sky, 성분명: 크로발리맙, Crovalimab-akkz, 로슈)'는 보체 단백질 C5를 표적으로 하는 재활용형 단클론항체(recycling monoclonal antibody) 기반 치료제로, 발작성 야간혈색소뇨증(paroxysmal nocturnal hemoglobinuria, PNH) 환자의 치료를 위해 개발되었다. 이 약제는 2024년 2월 중국에서 세계 최초로 승인된 이후, 3월 일본, 6월 미국 FDA, 8월 유럽 EMA에서 '13세 이상(체중 40kg 이상)의 소아 및 성인 PNH 환자'에 승인되었다.발작성 야간혈색소뇨증(PNH)은 후천적 조혈모세포 클론 이상에 의해 발생하는 드문 혈액 질환으로, GPI anchor(앵커) 단백질 결손에 따라 보체조절인자가 부족해지면서 만성 혈관 내 용혈(IVH), 조혈 기능 저하, 혈전증 등이 주요 임상 양상으로 나타난다. 이는 보체계 과활성화에 의해 매개되는 보체-매개 질환(complement-mediated diseases)이다.이에 피아스키는 PNH 치료를 위해 개발되었으며, 선천면역계의 중요한 요소이자 감염에 대한 신체의 1차 방어선인 보체계(complement system)를 차단하도록 설계되었다.국내에서 승인된 C5 억제제로는 '솔리리스(Eculizumab)' 및 '울토미리스(Ravulizumab)'가 있으며, 모두 보체의 말단(C5)을 억제하여 막공격복합체(membrane attack complex, MAC) 형성을 차단함으로써 혈관 내 용혈을 억제한다. 또한 모두 정맥주사(IV infusion)로 투여되며, 각각 2주 간격, 8주 간격으로 유지된다.그리고 '엠파벨리(Pegcetacoplan)'는 C3 억제제로서 C3/C3b를 직접 억제하여 보체 활성의 중심 단계부터 차단함으로써, 혈관 내 및 혈관 외 용혈을 동시에 조절할 수 있다. '파발타(Iptacopan, Factor B 억제제)'와 '보이데야(Danicopan, Factor D 억제제)'는 보체 대체 경로(alternative pathway)의 초기 단계를 선택적으로 억제하는 약제이다.피아시키의 글로벌 승인은 C5 억제제 치료 경험이 없는 PNH 환자를 대상으로 한 COMMODORE 2 3상 임상시험 결과를 근거로 이루어졌다. 이 연구에서 피아스키는 4주 간격의 피하주사로 투여되었으며, 주요 평가 지표인 용혈 조절률(LDH ≤ 1.5×ULN 유지) 및 수혈 회피율에 있어 대조군인 기존 치료제 솔리리스와 비열등성(non-inferiority)을 입증하였다. 더불어 안전성 프로파일 또한 양호하여, 자가 투여를 포함한 장기적 치료 전략에서의 유용성을 뒷받침하였다.발작성 야간혈색소뇨증(PNH) 적혈구란 무엇인가?발작성 야간혈색소뇨증(PNH)은 골수부전증후군(bone marrow failure syndromes)의 한 아형으로 분류되는 후천성 클론성 조혈모세포질환(acquired clonal hematopoietic stem cell disorder)이며, 이는 phosphatidylinositol glycan anchor biosynthesis class A(PIGA) 유전자에 발생한 기능 상실성 체세포 돌연변이(loss-of-function somatic mutation)에 의해 분자유전학적으로 정의되는 질환이다.이러한 유전적 변이는 glycosylphosphatidylinositol-anchor(GPI-앵커)의 생합성 경로에 결함을 유발하며, 이로 인해 GPI-앵커 단백질이 결핍된 적혈구가 형성된다.건강한 적혈구는 PIGA 유전자 변이를 가진 PNH 적혈구와 분자적 및 세포생물학적 수준에서 근본적인 차이를 나타낸다.정상 적혈구에서는 GPI-앵커가 소포체(endoplasmic reticulum, ER) 내막에서 여러 단계의 효소 반응을 통해 생합성된다. CD55와 CD57과 같은 GPI-앵커 단백질은 세포질 리보솜에서 번역되며, N-말단에 위치한 신호 서열(signal sequence)의 유도에 따라 소포체 내강으로 이동한다. 이후, 소포체 내강에서는 GPI 트랜스아미다제(transamidase) 복합체에 의해 단백질의 C-말단이 절단되고, 완성된 GPI 앵커가 공유 결합 형태로 단백질에 부착된다. 형성된 GPI-앵커 단백질은 소포체에서 골지체(Golgi apparatus)를 경유하여 세포막으로 수송되며, 최종적으로 세포막의 지질 뗏목(membrane raft) 영역에 선호적으로 삽입되어 생리적 기능을 수행한다. 대표적인 GPI-앵커 단백질로는 CD55(decay-accelerating factor)와 CD59(membrane inhibitor of reactive lysis)가 있으며, 이들 단백질은 보체계 활성 조절에 핵심적인 역할을 한다. CD55는 C3 전환효소의 형성을 저해하고, CD59는 막공격복합체(MAC)의 세포막 삽입을 차단함으로써 보체-매개 용혈(complement-mediated hemolysis)로부터 적혈구를 방어하는 중요한 보호 인자로 작용한다.PIGA-PNH 적혈구는 GPI-앵커 합성 경로의 초기 단계를 담당하는 PIGA 유전자에 발생하는 단일 체세포 돌연변이에 의해 발생하며, 이는 PNH의 가장 전형적이고 흔한 형태이다. 이러한 경우, CD55와 CD59를 포함한 모든 GPI-앵커 단백질이 적혈구 표면에서 결손되며, 특히 보체 대체 경로(alternative pathway)의 비가역적이고 자발적인 활성에 대한 방어가 결여됨으로써, 혈관 내 용혈(intravascular hemolysis, IVH)이 발생하게 된다.또한, 일부 GPI-앵커 단백질은 세포 간 접착, 신호 전달, 면역 조절 등 다양한 생리적 기능에 관여하기 때문에, 이들의 결손은 세포 간 상호작용의 장애, 클론성 면역 회피(clonal immune escape), 혈관 기능 이상 및 혈전 성향 증가(thrombotic diathesis) 등을 일으킨다.PIGT(Phosphatidylinositol Glycan Anchor biosynthesis, class T)-PNH 적혈구는 드물게 발생하는 자가 염증성 표현형(autoinflammatory phenotype)의 PNH로, PIGT 유전자에 발생한 생식세포 돌연변이와 체세포 결실(two-hit)에 의해 발생한다.PIGT 유전자의 기능이 결손된 경우, GPI 앵커 자체는 정상적으로 합성되지만, CD55 및 CD59와 같은 GPI-앵커 단백질이 적혈구 세포막에 부착되지 못하게 되어, 보체 조절 능력을 상실한 적혈구가 생성된다. 이러한 적혈구는 혈관 내 용혈(IVH)을 유발할 수 있으며, 동시에 혈장 내 유리 GPI(free GPI)의 존재로 인해 발열, 발진, 관절통 등의 자가 염증성 자가면역 증상이 동반될 수 있다. 이러한 점에서 PIGT 결손에 의한 PNH는 PIGA 결손에 의한 PNH와 임상적으로 구별된다.PNH에서 보체계 활성화가 어떻게 일어나는가?보체계(Complement system)는 선천면역(intrinsic immunity)의 핵심 구성 요소로서, 병원체에 대한 신속하고 강력한 방어 반응을 유도하는 고도로 통합된 생물학적 방어 체계이다. 그러나 이러한 강력한 면역 반응은 보체계를 활성화시켜 자가세포에 대한 비특이적 손상을 초래하기도 한다. 보체계의 활성화는 세 가지 주요 활성화 경로-고전 경로(classical pathway, CP), 렉틴 경로(lectin pathway, LP), 대체 경로(alternative pathway, AP)-를 통해 유도된다.고전 경로(CP)는 병원체 표면에 결합한 항원-항체 면역복합체(antigen-antibody complex)에 의해 유도된다. 렉틴 경로(LP)는 병원체 표면의 만노오스 잔기(mannose residues) 또는 특이 다당류(polysaccharides)에 결합한 MBL(mannose-binding lectin) 및 MASP(mannan-binding lectin-associated serine protease) 복합체에 의해 활성화된다. 한편, 대체 경로(AP)는 항원 비특이적으로 항상 낮은 수준에서 C3의 자발적 가수분해(spontaneous hydrolysis)가 지속적으로 일어나는 tick-over 기전(기본 활성 유지 기전)에 의해 유도되며, 이는 손상된 세포막 표면에서 선택적으로 보체 반응을 개시한다.일단, 보체계 활성화가 시작되면, 중심 단백질인 C3가 C3 전환효소(C3 convertase)에 의해 C3a와 C3b로 절단되며, 이 과정은 세 가지 경로 모두에서 공통적으로 일어난다.고전 경로(CP) 및 렉틴 경로(LP)에서는 보체 단백질 C4와 C2가 활성화되어 각각 C4b와 C2a로 절단된 후, 이들이 결합하여 C3 전환효소인 C4bC2a 복합체를 형성한다. 이 효소 복합체는 C3를 C3a와 C3b로 분해하여 보체 연쇄 반응(complement cascade)의 중심 단계인 C3 활성화를 유도한다.반면, 대체 경로(AP)에서는 자발적으로 형성된 C3b가 인자 B(Factor B)와 결합하며, 이 복합체는 인자 D(Factor D)에 의해 Bb와 Ba로 절단된다. 그 결과 생성된 C3bBb 복합체는 추가적인 C3 분자의 절단을 통해 새로운 C3b를 지속적으로 생성함으로써, 보체 활성화를 가속화하고 확대하는 증폭 고리(amplification loop)를 형성한다. 이 양성 되먹이 기전(positive feedback mechanism)은 병원체 표면에 대한 보체 침착을 증가시키며, 선천면역 반응의 신속하고 강력한 활성화를 가능하게 한다.따라서, C3a와 C3b는 보체계의 중심 단백질인 C3가 C3 전환효소에 의해 절단되면서 생성되는 두 가지 주요 활성 산물이다. 각각의 역할은 면역 반응에서 매우 다르며 상호 보완적이다.이 중 C3a는 C3 전환효소에 의해 절단된 소단편으로, 대표적인 염증 유발 인자(anaphylatoxin)이다. C3a는 호산구, 호중구, 대식세포 등의 면역 세포에 작용하는 화학주성인자(chemotactic factor)로, 히스타민 분비를 유도하고 혈관 확장 및 혈관 투과성을 증가시킴으로써 염증 반응을 증폭시킨다. 또한, 백혈구의 병변 부위로의 이동을를 촉진하여 선천면역 반응을 활성화한다. 그러나 C3a가 과도하게 생성되거나 조절이 실패할 경우, 알레르기 반응 또는 조직 손상 등의 병리적 염증 상태에 관여한다.다음, C3b는 C3 C3 전환효소에 의해 절단된 대단편으로, 병원체 표면에 결합하여 식작용(phagocytosis)을 유도하는 주요 옵소닌(opsonin)으로 작용한다. 이는 식세포가 병원체를 인식하고 제거하는 데 필수적인 신호를 제공하며, 선천면역 반응에서 중요한 역할을 한다. 이 외에도 C3b는 보체 연쇄 반응의 말단 효과기 기전인 막공격복합체(MAC) 형성의 초기 단계를 유도한다. 이를 위해 C3b는 C5 전환효소(C4b2aC3b 또는 C3bBbC3b)의 형성에 관여하며, 이후 C5가 분해되어 생성된 C5b는 C6, C7, C8 및 다수의 C9와 순차적으로 결합하여 보체 종말 복합체(terminal complement complex, TCC)를 형성한 후, 막공격복합체(membrane attack complex, MAC)로 완성된다. MAC은 적혈구 세포막에 삽입되어 삼투성 불균형을 유도하고, 세포막에 구멍(pore)을 형성함으로써 세포 용해(lysis)를 초래한다.이러한 보체계의 체계적인 활성화는 PNH 환자에서 병리학적 기전으로 작용한다. 즉, 후천적인 PIGA 유전자 돌연변이는 GPI-앵커의 생합성 결함을 초래하며, 이로 인해 CD55 및 CD59와 같은 GPI-앵커화된 보체 조절 단백질이 적혈구 세포막에서 결손된다.결과적으로, 이들 조절 단백질이 결손된 PNH 적혈구는 조절되지 않은 보체 활성화에 지속적으로 노출되며, 그 결과 보체-매개 혈관 내 용혈(complement-mediated intravascular hemolysis)에 극도로 취약한 상태가 된다.보체-매개 용혈(Complement-mediated hemolysis)이란 무엇인가? 보체-매개 질환(complement-mediated diseases)은 선천면역 체계의 핵심 구성 요소인 보체 시스템의 비정상적인 활성화 또는 조절 장애로 인해 발생하는 질환이다. 이들은 크게 자가면역, 감염, 혈액학적, 신장, 안과 및 희귀질환 영역에 걸쳐 있으며, 치료 표적으로서 점차 중요성이 부각되고 있다. 이 중 보체-매개 용혈complement-mediated hemolysis)은 적혈구 세포막의 구조적 파괴로 인해 세포 내 함유물, 특히 헤모글로빈이 혈장 내로 유리되는 병리적 현상을 의미하며, 발생 위치에 따라 혈관 내 용혈(IVH)과 혈관 외 용혈(EVH)로 분류된다. IVH는 적혈구가 혈관 내에서 직접 파괴되고 EVH는 적혈구가 비장이나 간의 대식세포에 의해 제거된다.혈관 내 용혈(IVH)은 일반적으로 보체 종말 경로(terminal complement pathway)의 활성화에 의해 유도되며, 이는 C5의 절단을 기점으로 C5b–C9로 구성된 막공격복합체(MAC)가 형성되어 적혈구 세포막에 삽입됨으로써 삼투압 불균형 및 세포 용해를 초래한다. PNH 환자에서는 CD55 및 CD59와 같은 GPI-앵커화된 보체 조절 단백질의 결손으로 인해 보체-매개 용혈에 대한 방어 기전이 상실되며, 그 결과 MAC의 삽입에 의한 적혈구의 직접적인 파괴가 진행된다.이러한 IVH가 발생하면, 적혈구 내 헤모글로빈이 혈장으로 방출되며, 방출된 유리 헤모글로빈(free hemoglobin)은 혈류 내 일산화질소(nitric oxide, NO)와 결합하여 NO의 생리적 기능을 저해함으로써 혈관 확장 및 혈소판 활성이 억제된다. 이에 따라, 혈관 수축, 혈소판 활성화, 혈전 생성 등과 같은 병태생리적 변화가 유도된다. 또한, 혈중 자유 헤모글로빈은 신장을 통해 여과되어 소변으로 배출되며, 이 과정에서 신세뇨관 독성을 일으켜 만성 신기능 저하를 초래할 수 있다.혈관 외 용혈(EVH)은 보체계가 불완전하게 억제되거나, 보체 활성화가 상위 단계(C3 수준)에서 지속될 때 발생한다. 보체가 활성화되면 생성된 C3b 및 그 분해 산물이 적혈구 표면에 침착되어 옵소닌으로 작용하며, 이는 비장, 간, 골수의 대식세포에 의해 적혈구가 인식되고 식작용을 유도하는 신호가 된다.EVH는 세포막의 직접적 파괴 없이 식세포에 의한 적혈구 제거로 발생하기 때문에, 혈관 내 유리 헤모글로빈의 유리는 거의 관찰되지 않는다. 대신, 간접 빌리루빈 상승, 망상적혈구 증가, 비장 비대와 같은 간접적인 용혈 지표가 임상적으로 관찰된다. 이는 혈관 손상이나 출혈을 직접 유발하지 않는다는 점에서 IVH와 병태생리적으로 구별된다.보체 억제제에는 어떤 약제들이 있는가?현재 PNH 치료는 보체 활성 경로 내 표적 분자의 선택에 따라 C5 억제제, C3 억제제, 또는 대체 경로(AP) 억제제(예: Factor B 및 Factor D 억제제)로 치료제가 다양화되고 있다. 이러한 치료제의 선택은 환자의 임상 양상, 유전적 배경, 치료 반응성 및 약물 순응도를 종합적으로 고려해야 한다. PNH의 치료는 보체계의 비정상적 활성화를 억제하여 혈관 내 용혈(IVH) 및 혈관 외 용혈(EVH)을 조절하는 데 중점을 둔다. 이에 따라 최근 다양한 표적 보체 억제제들이 개발되었으며, 이들은 작용 기전과 표적 단계에 따라 분류된다.먼저, C5 억제제는 보체 종말경로(terminal pathway) 억제제로 국내에는 에쿨리주맙(Eculizumab, 제품명: 솔리리스 주, SolirisⓇ, 아스트라제네카)과 라불리주맙(Ravulizumab, 제픔명: 울토미리스 주, UltomirisⓇ, 아스트라제네카)이 승인되어 있다.에쿨리주맙은 최초의 C5 억제제로 2007년에 미국 FDA에서 ‘발작성 야간 혈색소뇨증(PNH)’에 승인되었고, 현재 국내에서는 발작성 야간 혈색소뇨증(PNH)를 비롯하여 ‘비정형 용혈성 요독 증후군(atypical Hemolytic Uremic Syndrome, aHUS)’, ‘중증 근무력증(generalized Myasthenia Gravis, gMG)’, ‘시신경 척수염 범주 질환(neuromyelitis optica spectrum disorder, NMOSD)’ 치료에 승인되어 있다. 또한 바이오시밀러로 에피스클리 주(EpysqliⓇ, 삼성바이오에피스)가 식약처로부터 2024년 1월 솔리리스와 동일한 적응증으로 승인되었다.라불리주맙은 두 번째 C5 억제제로 2018년 미국 FDA에서 ‘발작성 야간 혈색소뇨증(PNH)’에 승인되었고, 현재 국내에서는 에쿨리주맙과 동일한 적응증으로 승인되어 있다. 라불리주맙의 가장 큰 특징은 기존 에쿨리주맙에 비해 투여 간격이 길다는 점이다. 즉, 약 4배 긴 반감기로 인해 에쿨리주맙은 2주마다 투여해야 하지만, 라불리주맙은 8주마다 투여하면 된다.이들 약제는 모두 보체 C5 단백질의 절단을 차단함으로써 막공격복합체(MAC)의 형성을 억제하고, IVH를 효과적으로 차단할 수 있다. 그러나, 상위 보체 경로, 특히 C3b 침착을 차단하지는 못하므로, 일부 환자에서는 지속적인 C3b 매개 EVH가 남아있을 수 있으며, 이로 인해 빈혈 지속, Coombs 양성 반응, 수혈 필요성 등의 임상 문제가 나타날 수 있다.두 번째, C3 억제제로 페그세타코플란(Pegcetacoplan, 제품명: 엠파벨리 주 EmpaveliⓇ, 한독)이 2021년 미국 FDA와 유럽 EMA 및 2024년 5월 국내에서 ‘성인의 발작성 야간혈색소뇨증(PNH)의 치료’에 승인되었다. 동일 성분의 페그세타코플란(Pegcetacoplan, 제품명: 사이포브레 주 SyfovreⓇ, Apelis)는 2023년 미국 FDA로부터 유리체강 내 주사(intravitreal injection)로 ‘나이 관련 황반변성(age-related macular degeneration, AMD)으로 인한 지도모양위축(Geographic Atrophy, GA) 치료제’에 승인된 바 있다.이 약제는 C3 및 C3b를 직접 억제하는 근위 보체(proximal complement) 억제제로, CP, LP, AP 등 모든 보체 활성화 경로에서 C3 전환 이후의 반응을 포괄적으로 차단한다. 이로 인해 IVH와 EVH를 동시에 억제할 수 있다.특히, 기존 C5 억제제 치료에도 빈혈이 지속되는 환자에게 임상적 유용성을 입증하였다. 다만, 보체 전체의 광범위한 억제에 따른 감염 위험성 증가와 투여 주기(주 2회 피하 주사)에 대한 고려가 필요하다.세 번째, 보체 대체 경로(AP)를 선택적으로 차단하는 경구용 억제제로 이프타코판(Iptacopan, 제품명: 파발타 캡슐, FabhaltaⓇ, 노바티스)과 다니코판(Danicopan, 제품명: 보이데야 정, VoydeyaⓇ, 아스트라제네카)이 있다.이들 약제는 AP 중심의 병태생리를 가진 PNH 환자 또는 C5 억제제에 불충분한 반응을 보이는 환자에서 선택적이고 효과적인 보체 조절을 가능하게 하며, 경구 투약 경로와 병용 치료를 통해 치료 접근성 및 환자 편의성을 향상시킬 수 있다.이프타코판은 2023년 미국 FDA, 2024년 5월 유럽 EMA 및 2024년 8월 국내에서 ‘성인의 발작성 야간혈색소뇨증(PNH의 치료’에 승인되었다. 이 약제는 최초의 경구용 PNH 치료제이며, 인자 B(Factor B)를 표적으로 하는 선택적 대체 경로(AP) 억제제이다.이 약제는 적혈구막에 존재하는 Factor B 및 AP 경로의 C3 전환효소(C3bBb)에 결합하여 그 활성을 저해하고, 더 나아가 AP 경로의 C5 전환효소(C3bC3bBb) 형성까지 차단한다. 결과적으로, 보체 활성화의 증폭 루프를 차단하여 C3b 의존적 EVH와 C5 매개 IVH를 모두 억제하는 기전을 가진다. 이러한 작용 특성으로 인해 기존의 C5 억제제를 대체할 수 있는 차세대 보체 억제제라고 할 수 있다.다니코판은 2024년 미국 FDA, 유럽 EMA 및 국내에서 “성인의 발작성야간 혈색소뇨증(PNH)의 기존에 C5 억제제(라불리주맙 또는 에쿨리주맙)를 투여 중인 PNH 환자에서 혈관 외 용혈(EVH) 증상이나 징후가 있는 경우 라불리주맙 혹은 에쿨리주맙에 부가요법”으로 승인받았다.이 약제는 인자 D(Factor D)에 가역적으로 결합하는 선택적 대체 경로(AP) 억제제로, C3 전환효소 형성의 초기 단계를 저해하는 기전을 갖는다. Factor D는 Factor B가 C3b와 결합한 복합체(C3bB)를 활성화하여 Bb와 Ba로 절단하는 세린계 단백질분해효소로, 이는 AP의 C3 전환효소(C3bBb) 형성의 핵심 단계이다. 이 약제는 이 과정에서 Factor D의 활성을 억제함으로써 Bb 형성을 차단하고, 최종적으로 C3bBb 복합체의 생성을 저해한다. 그러나 이프타코판과는 달리, 이 약제는 이미 형성된 C3 전환효소(C3bBb) 및 C5 전환효소(C3bBbC3b)에 직접 작용하지 않으므로 이들 복합체의 활성을 직접 억제하지는 않는다.C5 억제제는 어떤 약제인가?C5 억제제는 보체 연쇄 반응의 말단 용혈 경로를 차단하기 위해 C5에 결합하여 이를 억제하는 보체 기반 치료제이다. 이들 약제는 C5b 생성을 억제하고, 막공격복합체(MAC)의 형성을 차단함으로써, 보체-매개 혈관 내 용혈(IVH)로부터 PNH 적혈구를 보호하는 기전을 갖는다.C5 억제제 치료를 받은 PNH 환자는 임상적 개선이 뚜렷하게 나타난다. 치료 후 IVH의 생화학적 지표인 젖산탈수소효소(lactate dehydrogenase, LDH) 수치가 유의하게 감소하며, 이는 IVH이 효과적으로 억제되었음을 의미한다.PNH 적혈구의 클론 크기는 대체로 증가하는 경향을 보이나, 백혈구 계열의 클론 크기에는 뚜렷한 변화가 관찰되지 않는다. 헤모글로빈 수치는 대부분 정상 하한 이하에서 유지되며, 절대 망상적혈구 수(absolute reticulocyte count, ARC)는 지속적으로 정상 상한치를 초과하는 양상을 보인다. 이는 지속적인 용혈에도 불구하고 골수의 보상 반응이 활발하게 유지되고 있음을 시사한다.이러한 유의한 임상적 이점에도 불구하고, C5 억제제는 본질적인 한계를 지닌다. C5의 억제를 통해 보체 연쇄 반응의 말단 효과기 기전은 차단되지만, 상위 단계인 C3의 활성화는 여전히 조절되지 않은 채 지속된다.PNH 적혈구는 보체 조절 단백질인 CD55 및 CD59의 발현 또한 결핍되어 있어, 세포 표면에 과도한 C3b가 침착된다. 침착된 C3b는 다시 분해되어 C3dg(degradation fragment g) 등의 분절 단백질을 형성하며, 이들 단백질은 CR2(complement receptor 3, 보체 수용체 2) 등과 결합한다. 이로 인해 적혈구는 간과 비장에 분포한 모세망내계(RES)의 식세포에 의해 인식되고 제거된다. 이러한 식세포- 매개 적혈구 제거가 EVH의 원인 된다.지속적인 EVH는 경미한 LDH 상승, 혈중 하플로글로빈의 소실, 총 빌리루빈 상승, ARC 증가, 그리고 정상 이하의 헤모글로빈 농도를 동반한 안정화된 만성 빈혈 등의 생화학적 지표로 나타난다.따라서, C5 억제제는 보체 말단 경로를 효과적으로 차단하여 IVH는 억제하지만, 보체 활성의 상위 경로에서 생성되는 C3b의 침착을 충분히 제어하지 못해 EVH가 발생할 수 있다.크로발리주맙은 에쿨리주맙과 약리학적으로 어떤 차이가 있는가?에쿨리주맙과 크로발리주맙은 보체 단백질 C5를 표적으로 하는 단클론항체로, 막공격복합체(MAC)의 형성을 억제함으로써 PNH 등 보체 매개 질환의 치료에 사용된다. 두 약제는 동일한 표적을 공유하지만, 결합 부위, 작용 기전, 항체 구조, 체내 약동학적 특성 등에서 중요한 약리학적 차이를 보인다.1. C5 결합 부위 및 유전자 변이에 대한 반응성에쿨리주맙은 C5의 α-사슬에 결합하여 C5 전환효소에 의한 절단(C5a 및 C5b 생성)을 차단함으로써 MAC 형성을 억제한다. 그러나 이 약제는 C5의 특정 유전자 변이(R885H 등)에 대해 결합력이 감소하므로, 일부 환자에서는 충분한 치료 효과를 기대하기 어렵다. 반면, 크로발리주맙은 C5의 β-사슬에 결합함으로써, 야생형뿐만 아니라 C5 변이형에 대해서도 안정적이고 지속적인 억제 효과를 나타낸다.2. 작용 기전의 차이두 약제 모두 C5 절단을 차단하여 MAC 형성을 억제하지만, 크로발리주맙은 형성된 C5b6 복합체의 세포막 침착까지 억제하는 이중 기전을 가진다. 이로 인해 C5 절단 억제뿐만 아니라 잔여 보체 활성으로 인한 조직 손상 가능성까지 추가적으로 제한할 수 있다. 반면, 에쿨리주맙은 이러한 C5b6 억제 기전을 갖고 있지 않다.3. 항체 구조 및 재활용 기술에쿨리주맙은 기존의 인간화 IgG2/4 단클론항체로, 세포 내로 흡수된 이후 리소좀 내에서 분해된다. 그 결과 체내 반감기는 약 11일로 짧으며, 2주 간격의 정맥 주사 투여가 필요하다. 반면, 크로발리주맙은 SMART 기술이 적용된 항체로, pH 의존적 항원 결합 및 FcRn(Fc receptor neonatal) 매개 재활용 메커니즘을 통해 체내에서 효율적으로 재순환된다. 이로 인해 반감기가 연장되며, 동일한 용량으로도 더 오랜 기간 동안 효과를 유지할 수 있다.4. 투여 방식 및 환자 편의성에쿨리주맙은 정맥 주사만 가능하며, 자가 투여가 불가능하여 치료 순응도와 환자 편의성이 낮은 편이다. 반면, 크로발리주맙은 피하 주사로도 투여가 가능하며, 자가 투여 역시 가능하다. 또한, 투여 간격이 4~8주까지 연장 가능하여 장기 치료에서의 환자 부담을 줄일 수 있다.크로발리주맙은 어떤 약제인가?크로발리맙(Crovalimab, 제품명 PiaSky®)은 보체 단백질 C5를 표적으로 하는 인간화 단클론항체로, 약물 설계 단계에서부터 SMART(Sequential Monoclonal Antibody Recycling Technology) 플랫폼이 적용된 차세대 보체 억제제이다. 이 약제는 pH-의존적 항원 결합 특성과 FcRn(neonatal Fc receptor, 신생아 Fc 수용체) 매개 재활용 기전을 활용함으로써, 항체의 반감기를 연장하고 투약 용량 및 빈도를 감소시키는 데 기여한다. 또한, C5 유전자의 특정 변이(R885H 등)로 인해 기존 C5 억제제(예: 에쿨리주맙, 라불리주맙)에 저항성을 보이는 환자군에서도 안정적인 약물 반응성을 유지하는 이점이 보고되었다.크로발리맙의 SMART 기술은 항체가 표적에 결합한 후에도 세포 내 분해되지 않고 재활용될 수 있도록 설계된 항체 공학 기술이다. 이 기술의 핵심 기전은 다음 세 가지로 요약된다.첫째, FcRn는 항체의 Fc 영역에 결합하여, 세포 내 리소좀 분해를 회피하고 항체가 혈류로 다시 방출(recycling)될 수 있도록 한다. 이를 통해 항체의 체내 반감기가 연장되며, 장시간 약리 효과가 유지된다.둘째, pH-의존적 친화력 조절 기능(pH-dependent affinity tuning)은 항체가 엔도솜 내 산성 환경(pH 5.5 이하)에서는 항원(C5)으로부터 이탈하고 FcRn에 결합하며, 혈중 중성 pH에서는 다시 표적에 결합하도록 설계되었다. 이러한 pH 의존적 해리 및 재결합 특성은 반복적인 항원 차단을 가능하게 한다.셋째, 등전점 조절(isoelectric point tuning)을 통해 항체의 산성 환경에서의 용해도 및 표적 결합 특성이 조절되어, 세포 내 효율적인 수송과 재방출이 가능해진다. 이를 통해 항체는 기존 항체 대비 적은 용량으로도 지속적인 약리 효과를 발휘하며, 투여 빈도를 줄일 수 있어 치료 편의성 및 비용 효율성 측면에서 이점을 제공한다.이와 같은 재활용 기반 항체 특성은 C5와의 효율적인 결합 및 세포 내 표적 단백질 제거, FcRn 매개 항체의 재활용, 향상된 약물 지속 시간으로 이어진다. 또한, 크로발리맙은 높은 용해성을 가지고 있으므로 소량으로도 피하 주사가 가능하다.이러한 크로발리맙의 임상 개발은 COMPOSER(1/2상), COMMODORE 1 및 2(3상), COMMODORE 3(중국 내 3상) 임상시험을 통해 진행되었다. 이 중 3상 무작위 배정 비교 임상인 COMMODORE 2 연구는 C5 억제제 치료 경험이 없는 PNH 환자를 대상으로 수행되었으며, 이 결과를 바탕으로 미국 FDA 승인을 획득하였다.이 연구에서 크로발리맙은 4주 간격의 피하 주사로 투여되었으며, 질병 조절 효능과 안전성이 기존 치료제인 에쿨리주맙 대비 비열등(non-inferior)한 것으로 입증되었다. 치료 관련 이상반응 발생률 역시 두 치료제 간에 유의한 차이를 보이지 않았다.크로발리맙은 초기 정맥 투여 부하 용량으로 치료를 시작하며, 이후 4주간 주 1회 피하 투여를 통해 부하 용량을 유지한다. 이후에는 환자 교육을 통해 자가 투여가 가능하도록 설계되어 있으며, 4주 간격의 유지 요법은 기존 2주 간격의 정맥 투여 기반 치료에 비해 투약 빈도를 감소시키는 이점을 갖는다.미국 FDA의 허가에 따르면, 크로발리맙은 ‘체중 40kg 이상의 13세 이상 소아 및 성인 PNH 환자’를 적응증으로 승인되었으며, 심각한 수막구균 감염 위험을 줄이기 위한 REMS(Risk Evaluation and Mitigation Strategy) 프로그램 하에 처방 및 조제가 이루어지도록 규정되었다.크로발리주맙의 허가임상은COMMODORE 2 연구는 보체 억제제 치료 경험이 없는 PNH 환자를 대상으로 크로발리맙의 유효성과 안전성을 평가하기 위해 수행된 활성 대조, 공개 라벨, 비열등성 3상 무작위 배정 임상 시험이다.총 204명의 환자가 등록되었으며, 이들은 2:1 비율로 무작위 배정되어 크로발리맙(n=135) 또는 에쿨리주맙(n=69)을 투여받았다. 크로발리맙은 1일차에 정맥 주사로 단회 초기 용량을 투여한 뒤, 2일차부터 22일차까지 총 4회, 주 1회 피하 주사로 투여되었고, 이후 29일차부터는 4주 간격의 피하 주사를 통해 유지요법을 진행하였다.이 연구는 총 24주간의 주요 치료 기간(primary treatment period)으로 구성되었으며, 이후에는 환자에게 크로발리맙 치료를 지속하거나 전환할 수 있는 연장 투여 기간(extension period)이 제공되었다. 대상 환자는 혈중 LDH 수치가 정상 상한값(ULN)의 2배 이상이며, 최근 3개월 이내에 하나 이상의 PNH 관련 증상 또는 징후가 있었던 경우에 한해 포함되었다.무작위 배정은 최근 LDH 수치(≥2×ULN∼≤4× ULN 또는 ≽4×ULN)와 수혈 이력(0회, 1∼6회, 또는 6회 이상)에 따라 층화(stratification)하여 수행되었다.주요 유효성 평가지표는 다음과 같다:수혈 회피(Transfusion avoidance) 환자의 비율: 베이스라인부터 25주차까지 농축 적혈구(pRBC) 수혈 없이 유지된 환자의 비율로 평가되었다. 용혈 조절(Hemolysis control) 도달 환자의 비율: 5주차부터 25주차까지의 기간 동안 평균적으로 LDH 수치가 ULN의 1.5배 이하로 유지된 환자의 비율을 측정하였다. 돌파성 용혈(Breakthrough hemolysis, BTH) 발생 환자의 비율: LDH가 일시적으로 1.5×ULN 이하로 조절되었다가 이후 2×ULN 이상으로 상승하고, 새로운 혹은 악화된 혈관 내 용혈의 증상 또는 징후가 함께 동반된 경우를 BTH로 정의하여 평가하였다. 혈색소 안정화(Stabilized hemoglobin) 환자의 비율: 수혈 없이 베이스라인 대비 혈색소 수치가 ≥2 g/dL 이상 감소하지 않은 환자의 비율로 평가되었다.주요 결과는 다음과 같다:수혈 회피 비율: 크로발리맙 군에서 65.7%, 에쿨리주맙 군에서 68.1%로 나타나 두 군 간 유사한 수준의 수혈 회피율이 관찰되었다. LDH ≤1.5×ULN에 도달한 환자의 비율: 크로발리맙 군에서 79.3%, 에쿨리주맙 군에서 79.0%로 양 군 간 차이가 없었으며, 이는 용혈 조절 측면에서 비열등성을 충족함을 시사한다. 돌파성 용혈 발생률: 크로발리맙 군에서 10.4%, 에쿨리주맙 군에서 14.5%로, 오히려 크로발리맙에서 더 낮은 경향을 보였다. 혈색소 안정화율: 크로발리맙 군에서 63.4%, 에쿨리주맙 군에서 60.9%로 나타나, 혈색소 유지 효과 역시 비슷한 수준으로 평가되었다.크로발리주맙은 어떤 쟁점이 있는가?크로발리맙은 기존의 C5 억제 치료에서 동반되던 여러 제한점을 극복하고자 개발된 차세대 보체 억제제로, SMART 기반 항체 엔지니어링 기술을 적용한 최초의 월 1회 피하 주사 형태의 치료제이다. 이 약제는 C5에 반복적으로 결합 및 억제할 수 있도록 설계되어, 체내에서 장기간 작용하며, 상대적으로 적은 용량으로도 치료 효과를 유지할 수 있는 것이 특징이다.크로발리맙은 보체 연쇄 반응의 말단인 C5를 표적으로 결합하여 C5a 및 C5b의 생성을 차단함으로써 MAC 형성을 억제하고, 빠르고 지속적인 보체 억제를 유도한다. 특히 혈중에서 FcRn 매개 항체 재활용 기전을 통해 반복적으로 작용할 수 있어, 4주 간격 투여가 가능하다.기존 치료제는 모두 C5의 α-사슬을 표적으로 하는 반면, 크로발리맙은 C5의 β-사슬에 결합하여 작용한다. 이로 인해 R885H와 같은 특정 C5 유전자 변이 보유 환자에서 기존 치료제에 비해 더 높은 결합력과 억제 효과를 나타낼 수 있어, 기존 치료제에 반응하지 않는 환자군에 대한 새로운 치료 옵션으로 제시된다.한편, 크로발리맙과 기존 치료제를 병용하거나, 교체 투여 중 두 약제가 동시에 투여되는 경우, 각기 다른 C5 에피토프에 결합하는 항체들 사이에서 약물–표적–약물 복합체(drug–target–drug complex, DTDC)가 형성될 수 있다. 이 복합체는 면역복합체의 일종으로 간주될 수 있으며, 교체 기간 중 약물의 안전성 및 유효성에 영향을 줄 가능성이 제기된다. 이에 따라, C5 억제제 간 전환 시에는 신중한 임상적 고려와 면밀한 환자 모니터링이 필요하다.크로발리맙은 자가 투여 가능한 피하주사 기반 PNH 치료제로, 정맥 주사 기반의 기존 치료제와 비교해 환자와 보호자의 치료 부담을 경감시킬 수 있다. 특히, 의료기관 방문의 빈도 감소와 자가 관리 가능성은 장기 치료가 필요한 PNH 환자에게 실질적인 삶의 질 향상을 제공할 수 있다.결론적으로, 크로발리맙(PiaSkyⓇ)은 C5 억제를 통한 기존 치료제의 보체 억제 전략의 유효성을 유지하면서도, 투여 경로의 간편화, 투여 간격의 연장, 특정 유전자 변이에 대한 대응력 등의 특성을 갖춘 차세대 보체 억제제로 평가된다. 이는 PNH 치료의 편의성과 맞춤화를 동시에 실현하는 전환점을 마련한 약제라 할 수 있다.참고문헌 1. Robert A. Brodsky “Paroxysmal nocturnal hemoglobinuria withoutGPI-anchor deficiency” J Clin Invest. 2019;129(12):5074-5076. 2. Peter Hillmen, Regina Horneff, Michael Yeh, Martin Kolev  and Pascal Deschatelets “Navigating the Complement Pathway to Optimize PNH Treatment with Pegcetacoplan and Other Currently Approved Complement Inhibitors“ Int. J. Mol. Sci. 2024, 25, 9477. 3. Carmelo Gurnari, Ishani Nautiyal, Simona Pagliuca. “Current Opinions on the Clinical Utility of Ravulizumab for the Treatment of ParoxysmalNocturnal Hemoglobinuria” Therapeutics and Clinical Risk Management 2021:17 1343–1351. 4. Regina Horneff, Barbara Czech, Michael Yeh andElena Surova. “Three Years On: The Role of Pegcetacoplan in Paroxysmal Nocturnal Hemoglobinuria (PNH) since Its Initial Approval” Int. J. Mol. Sci. 2024, 25(16), 8698. 5. Alexander Röth 1, Jun-ichi Nishimura 2, Zsolt Nagy 3, et al, “The complement C5 inhibitor crovalimab in paroxysmal nocturnal hemoglobinuria” Blood. 2020 Jan 24;135(12):912–920. 6. Melissa A. Colden, Melissa A. Colden, Sushant Kumar, et al “Insights Into the Emergence of Paroxysmal Nocturnal Hemoglobinuria” Front. Immunol., 2022 Volume 12 – 2021. 7. 기타 인터넷 자료(보도 자료, 제품 설명서 등)2025-05-13 18:10:35최병철 박사
PNH 치료제 '피아스키', 최초의 월 1회 피하주사제3편: 피하주사 발작성 야간혈색소증 치료제, 피아스키(Crovalimab)'피아스키(PiaSky, pea-UH-sky, 성분명: 크로발리맙, Crovalimab-akkz, 로슈)'는 보체 단백질 C5를 표적으로 하는 재활용형 단클론항체(recycling monoclonal antibody) 기반 치료제로, 발작성 야간혈색소뇨증(paroxysmal nocturnal hemoglobinuria, PNH) 환자의 치료를 위해 개발되었다. 이 약제는 2024년 2월 중국에서 세계 최초로 승인된 이후, 3월 일본, 6월 미국 FDA, 8월 유럽 EMA에서 '13세 이상(체중 40kg 이상)의 소아 및 성인 PNH 환자'에 승인되었다.발작성 야간혈색소뇨증(PNH)은 후천적 조혈모세포 클론 이상에 의해 발생하는 드문 혈액 질환으로, GPI anchor(앵커) 단백질 결손에 따라 보체조절인자가 부족해지면서 만성 혈관 내 용혈(IVH), 조혈 기능 저하, 혈전증 등이 주요 임상 양상으로 나타난다. 이는 보체계 과활성화에 의해 매개되는 보체-매개 질환(complement-mediated diseases)이다.이에 피아스키는 PNH 치료를 위해 개발되었으며, 선천면역계의 중요한 요소이자 감염에 대한 신체의 1차 방어선인 보체계(complement system)를 차단하도록 설계되었다.국내에서 승인된 C5 억제제로는 '솔리리스(Eculizumab)' 및 '울토미리스(Ravulizumab)'가 있으며, 모두 보체의 말단(C5)을 억제하여 막공격복합체(membrane attack complex, MAC) 형성을 차단함으로써 혈관 내 용혈을 억제한다. 또한 모두 정맥주사(IV infusion)로 투여되며, 각각 2주 간격, 8주 간격으로 유지된다.그리고 '엠파벨리(Pegcetacoplan)'는 C3 억제제로서 C3/C3b를 직접 억제하여 보체 활성의 중심 단계부터 차단함으로써, 혈관 내 및 혈관 외 용혈을 동시에 조절할 수 있다. '파발타(Iptacopan, Factor B 억제제)'와 '보이데야(Danicopan, Factor D 억제제)'는 보체 대체 경로(alternative pathway)의 초기 단계를 선택적으로 억제하는 약제이다.피아시키의 글로벌 승인은 C5 억제제 치료 경험이 없는 PNH 환자를 대상으로 한 COMMODORE 2 3상 임상시험 결과를 근거로 이루어졌다. 이 연구에서 피아스키는 4주 간격의 피하주사로 투여되었으며, 주요 평가 지표인 용혈 조절률(LDH ≤ 1.5×ULN 유지) 및 수혈 회피율에 있어 대조군인 기존 치료제 솔리리스와 비열등성(non-inferiority)을 입증하였다. 더불어 안전성 프로파일 또한 양호하여, 자가 투여를 포함한 장기적 치료 전략에서의 유용성을 뒷받침하였다.발작성 야간혈색소뇨증(PNH) 적혈구란 무엇인가?발작성 야간혈색소뇨증(PNH)은 골수부전증후군(bone marrow failure syndromes)의 한 아형으로 분류되는 후천성 클론성 조혈모세포질환(acquired clonal hematopoietic stem cell disorder)이며, 이는 phosphatidylinositol glycan anchor biosynthesis class A(PIGA) 유전자에 발생한 기능 상실성 체세포 돌연변이(loss-of-function somatic mutation)에 의해 분자유전학적으로 정의되는 질환이다.이러한 유전적 변이는 glycosylphosphatidylinositol-anchor(GPI-앵커)의 생합성 경로에 결함을 유발하며, 이로 인해 GPI-앵커 단백질이 결핍된 적혈구가 형성된다.건강한 적혈구는 PIGA 유전자 변이를 가진 PNH 적혈구와 분자적 및 세포생물학적 수준에서 근본적인 차이를 나타낸다.정상 적혈구에서는 GPI-앵커가 소포체(endoplasmic reticulum, ER) 내막에서 여러 단계의 효소 반응을 통해 생합성된다. CD55와 CD57과 같은 GPI-앵커 단백질은 세포질 리보솜에서 번역되며, N-말단에 위치한 신호 서열(signal sequence)의 유도에 따라 소포체 내강으로 이동한다. 이후, 소포체 내강에서는 GPI 트랜스아미다제(transamidase) 복합체에 의해 단백질의 C-말단이 절단되고, 완성된 GPI 앵커가 공유 결합 형태로 단백질에 부착된다. 형성된 GPI-앵커 단백질은 소포체에서 골지체(Golgi apparatus)를 경유하여 세포막으로 수송되며, 최종적으로 세포막의 지질 뗏목(membrane raft) 영역에 선호적으로 삽입되어 생리적 기능을 수행한다. 대표적인 GPI-앵커 단백질로는 CD55(decay-accelerating factor)와 CD59(membrane inhibitor of reactive lysis)가 있으며, 이들 단백질은 보체계 활성 조절에 핵심적인 역할을 한다. CD55는 C3 전환효소의 형성을 저해하고, CD59는 막공격복합체(MAC)의 세포막 삽입을 차단함으로써 보체-매개 용혈(complement-mediated hemolysis)로부터 적혈구를 방어하는 중요한 보호 인자로 작용한다.PIGA-PNH 적혈구는 GPI-앵커 합성 경로의 초기 단계를 담당하는 PIGA 유전자에 발생하는 단일 체세포 돌연변이에 의해 발생하며, 이는 PNH의 가장 전형적이고 흔한 형태이다. 이러한 경우, CD55와 CD59를 포함한 모든 GPI-앵커 단백질이 적혈구 표면에서 결손되며, 특히 보체 대체 경로(alternative pathway)의 비가역적이고 자발적인 활성에 대한 방어가 결여됨으로써, 혈관 내 용혈(intravascular hemolysis, IVH)이 발생하게 된다.또한, 일부 GPI-앵커 단백질은 세포 간 접착, 신호 전달, 면역 조절 등 다양한 생리적 기능에 관여하기 때문에, 이들의 결손은 세포 간 상호작용의 장애, 클론성 면역 회피(clonal immune escape), 혈관 기능 이상 및 혈전 성향 증가(thrombotic diathesis) 등을 일으킨다.PIGT(Phosphatidylinositol Glycan Anchor biosynthesis, class T)-PNH 적혈구는 드물게 발생하는 자가 염증성 표현형(autoinflammatory phenotype)의 PNH로, PIGT 유전자에 발생한 생식세포 돌연변이와 체세포 결실(two-hit)에 의해 발생한다.PIGT 유전자의 기능이 결손된 경우, GPI 앵커 자체는 정상적으로 합성되지만, CD55 및 CD59와 같은 GPI-앵커 단백질이 적혈구 세포막에 부착되지 못하게 되어, 보체 조절 능력을 상실한 적혈구가 생성된다. 이러한 적혈구는 혈관 내 용혈(IVH)을 유발할 수 있으며, 동시에 혈장 내 유리 GPI(free GPI)의 존재로 인해 발열, 발진, 관절통 등의 자가 염증성 자가면역 증상이 동반될 수 있다. 이러한 점에서 PIGT 결손에 의한 PNH는 PIGA 결손에 의한 PNH와 임상적으로 구별된다.PNH에서 보체계 활성화가 어떻게 일어나는가?보체계(Complement system)는 선천면역(intrinsic immunity)의 핵심 구성 요소로서, 병원체에 대한 신속하고 강력한 방어 반응을 유도하는 고도로 통합된 생물학적 방어 체계이다. 그러나 이러한 강력한 면역 반응은 보체계를 활성화시켜 자가세포에 대한 비특이적 손상을 초래하기도 한다. 보체계의 활성화는 세 가지 주요 활성화 경로-고전 경로(classical pathway, CP), 렉틴 경로(lectin pathway, LP), 대체 경로(alternative pathway, AP)-를 통해 유도된다.고전 경로(CP)는 병원체 표면에 결합한 항원-항체 면역복합체(antigen-antibody complex)에 의해 유도된다. 렉틴 경로(LP)는 병원체 표면의 만노오스 잔기(mannose residues) 또는 특이 다당류(polysaccharides)에 결합한 MBL(mannose-binding lectin) 및 MASP(mannan-binding lectin-associated serine protease) 복합체에 의해 활성화된다. 한편, 대체 경로(AP)는 항원 비특이적으로 항상 낮은 수준에서 C3의 자발적 가수분해(spontaneous hydrolysis)가 지속적으로 일어나는 tick-over 기전(기본 활성 유지 기전)에 의해 유도되며, 이는 손상된 세포막 표면에서 선택적으로 보체 반응을 개시한다.일단, 보체계 활성화가 시작되면, 중심 단백질인 C3가 C3 전환효소(C3 convertase)에 의해 C3a와 C3b로 절단되며, 이 과정은 세 가지 경로 모두에서 공통적으로 일어난다.고전 경로(CP) 및 렉틴 경로(LP)에서는 보체 단백질 C4와 C2가 활성화되어 각각 C4b와 C2a로 절단된 후, 이들이 결합하여 C3 전환효소인 C4bC2a 복합체를 형성한다. 이 효소 복합체는 C3를 C3a와 C3b로 분해하여 보체 연쇄 반응(complement cascade)의 중심 단계인 C3 활성화를 유도한다.반면, 대체 경로(AP)에서는 자발적으로 형성된 C3b가 인자 B(Factor B)와 결합하며, 이 복합체는 인자 D(Factor D)에 의해 Bb와 Ba로 절단된다. 그 결과 생성된 C3bBb 복합체는 추가적인 C3 분자의 절단을 통해 새로운 C3b를 지속적으로 생성함으로써, 보체 활성화를 가속화하고 확대하는 증폭 고리(amplification loop)를 형성한다. 이 양성 되먹이 기전(positive feedback mechanism)은 병원체 표면에 대한 보체 침착을 증가시키며, 선천면역 반응의 신속하고 강력한 활성화를 가능하게 한다.따라서, C3a와 C3b는 보체계의 중심 단백질인 C3가 C3 전환효소에 의해 절단되면서 생성되는 두 가지 주요 활성 산물이다. 각각의 역할은 면역 반응에서 매우 다르며 상호 보완적이다.이 중 C3a는 C3 전환효소에 의해 절단된 소단편으로, 대표적인 염증 유발 인자(anaphylatoxin)이다. C3a는 호산구, 호중구, 대식세포 등의 면역 세포에 작용하는 화학주성인자(chemotactic factor)로, 히스타민 분비를 유도하고 혈관 확장 및 혈관 투과성을 증가시킴으로써 염증 반응을 증폭시킨다. 또한, 백혈구의 병변 부위로의 이동을를 촉진하여 선천면역 반응을 활성화한다. 그러나 C3a가 과도하게 생성되거나 조절이 실패할 경우, 알레르기 반응 또는 조직 손상 등의 병리적 염증 상태에 관여한다.다음, C3b는 C3 C3 전환효소에 의해 절단된 대단편으로, 병원체 표면에 결합하여 식작용(phagocytosis)을 유도하는 주요 옵소닌(opsonin)으로 작용한다. 이는 식세포가 병원체를 인식하고 제거하는 데 필수적인 신호를 제공하며, 선천면역 반응에서 중요한 역할을 한다. 이 외에도 C3b는 보체 연쇄 반응의 말단 효과기 기전인 막공격복합체(MAC) 형성의 초기 단계를 유도한다. 이를 위해 C3b는 C5 전환효소(C4b2aC3b 또는 C3bBbC3b)의 형성에 관여하며, 이후 C5가 분해되어 생성된 C5b는 C6, C7, C8 및 다수의 C9와 순차적으로 결합하여 보체 종말 복합체(terminal complement complex, TCC)를 형성한 후, 막공격복합체(membrane attack complex, MAC)로 완성된다. MAC은 적혈구 세포막에 삽입되어 삼투성 불균형을 유도하고, 세포막에 구멍(pore)을 형성함으로써 세포 용해(lysis)를 초래한다.이러한 보체계의 체계적인 활성화는 PNH 환자에서 병리학적 기전으로 작용한다. 즉, 후천적인 PIGA 유전자 돌연변이는 GPI-앵커의 생합성 결함을 초래하며, 이로 인해 CD55 및 CD59와 같은 GPI-앵커화된 보체 조절 단백질이 적혈구 세포막에서 결손된다.결과적으로, 이들 조절 단백질이 결손된 PNH 적혈구는 조절되지 않은 보체 활성화에 지속적으로 노출되며, 그 결과 보체-매개 혈관 내 용혈(complement-mediated intravascular hemolysis)에 극도로 취약한 상태가 된다.보체-매개 용혈(Complement-mediated hemolysis)이란 무엇인가? 보체-매개 질환(complement-mediated diseases)은 선천면역 체계의 핵심 구성 요소인 보체 시스템의 비정상적인 활성화 또는 조절 장애로 인해 발생하는 질환이다. 이들은 크게 자가면역, 감염, 혈액학적, 신장, 안과 및 희귀질환 영역에 걸쳐 있으며, 치료 표적으로서 점차 중요성이 부각되고 있다. 이 중 보체-매개 용혈complement-mediated hemolysis)은 적혈구 세포막의 구조적 파괴로 인해 세포 내 함유물, 특히 헤모글로빈이 혈장 내로 유리되는 병리적 현상을 의미하며, 발생 위치에 따라 혈관 내 용혈(IVH)과 혈관 외 용혈(EVH)로 분류된다. IVH는 적혈구가 혈관 내에서 직접 파괴되고 EVH는 적혈구가 비장이나 간의 대식세포에 의해 제거된다.혈관 내 용혈(IVH)은 일반적으로 보체 종말 경로(terminal complement pathway)의 활성화에 의해 유도되며, 이는 C5의 절단을 기점으로 C5b–C9로 구성된 막공격복합체(MAC)가 형성되어 적혈구 세포막에 삽입됨으로써 삼투압 불균형 및 세포 용해를 초래한다. PNH 환자에서는 CD55 및 CD59와 같은 GPI-앵커화된 보체 조절 단백질의 결손으로 인해 보체-매개 용혈에 대한 방어 기전이 상실되며, 그 결과 MAC의 삽입에 의한 적혈구의 직접적인 파괴가 진행된다.이러한 IVH가 발생하면, 적혈구 내 헤모글로빈이 혈장으로 방출되며, 방출된 유리 헤모글로빈(free hemoglobin)은 혈류 내 일산화질소(nitric oxide, NO)와 결합하여 NO의 생리적 기능을 저해함으로써 혈관 확장 및 혈소판 활성이 억제된다. 이에 따라, 혈관 수축, 혈소판 활성화, 혈전 생성 등과 같은 병태생리적 변화가 유도된다. 또한, 혈중 자유 헤모글로빈은 신장을 통해 여과되어 소변으로 배출되며, 이 과정에서 신세뇨관 독성을 일으켜 만성 신기능 저하를 초래할 수 있다.혈관 외 용혈(EVH)은 보체계가 불완전하게 억제되거나, 보체 활성화가 상위 단계(C3 수준)에서 지속될 때 발생한다. 보체가 활성화되면 생성된 C3b 및 그 분해 산물이 적혈구 표면에 침착되어 옵소닌으로 작용하며, 이는 비장, 간, 골수의 대식세포에 의해 적혈구가 인식되고 식작용을 유도하는 신호가 된다.EVH는 세포막의 직접적 파괴 없이 식세포에 의한 적혈구 제거로 발생하기 때문에, 혈관 내 유리 헤모글로빈의 유리는 거의 관찰되지 않는다. 대신, 간접 빌리루빈 상승, 망상적혈구 증가, 비장 비대와 같은 간접적인 용혈 지표가 임상적으로 관찰된다. 이는 혈관 손상이나 출혈을 직접 유발하지 않는다는 점에서 IVH와 병태생리적으로 구별된다.보체 억제제에는 어떤 약제들이 있는가?현재 PNH 치료는 보체 활성 경로 내 표적 분자의 선택에 따라 C5 억제제, C3 억제제, 또는 대체 경로(AP) 억제제(예: Factor B 및 Factor D 억제제)로 치료제가 다양화되고 있다. 이러한 치료제의 선택은 환자의 임상 양상, 유전적 배경, 치료 반응성 및 약물 순응도를 종합적으로 고려해야 한다. PNH의 치료는 보체계의 비정상적 활성화를 억제하여 혈관 내 용혈(IVH) 및 혈관 외 용혈(EVH)을 조절하는 데 중점을 둔다. 이에 따라 최근 다양한 표적 보체 억제제들이 개발되었으며, 이들은 작용 기전과 표적 단계에 따라 분류된다.먼저, C5 억제제는 보체 종말경로(terminal pathway) 억제제로 국내에는 에쿨리주맙(Eculizumab, 제품명: 솔리리스 주, SolirisⓇ, 아스트라제네카)과 라불리주맙(Ravulizumab, 제픔명: 울토미리스 주, UltomirisⓇ, 아스트라제네카)이 승인되어 있다.에쿨리주맙은 최초의 C5 억제제로 2007년에 미국 FDA에서 ‘발작성 야간 혈색소뇨증(PNH)’에 승인되었고, 현재 국내에서는 발작성 야간 혈색소뇨증(PNH)를 비롯하여 ‘비정형 용혈성 요독 증후군(atypical Hemolytic Uremic Syndrome, aHUS)’, ‘중증 근무력증(generalized Myasthenia Gravis, gMG)’, ‘시신경 척수염 범주 질환(neuromyelitis optica spectrum disorder, NMOSD)’ 치료에 승인되어 있다. 또한 바이오시밀러로 에피스클리 주(EpysqliⓇ, 삼성바이오에피스)가 식약처로부터 2024년 1월 솔리리스와 동일한 적응증으로 승인되었다.라불리주맙은 두 번째 C5 억제제로 2018년 미국 FDA에서 ‘발작성 야간 혈색소뇨증(PNH)’에 승인되었고, 현재 국내에서는 에쿨리주맙과 동일한 적응증으로 승인되어 있다. 라불리주맙의 가장 큰 특징은 기존 에쿨리주맙에 비해 투여 간격이 길다는 점이다. 즉, 약 4배 긴 반감기로 인해 에쿨리주맙은 2주마다 투여해야 하지만, 라불리주맙은 8주마다 투여하면 된다.이들 약제는 모두 보체 C5 단백질의 절단을 차단함으로써 막공격복합체(MAC)의 형성을 억제하고, IVH를 효과적으로 차단할 수 있다. 그러나, 상위 보체 경로, 특히 C3b 침착을 차단하지는 못하므로, 일부 환자에서는 지속적인 C3b 매개 EVH가 남아있을 수 있으며, 이로 인해 빈혈 지속, Coombs 양성 반응, 수혈 필요성 등의 임상 문제가 나타날 수 있다.두 번째, C3 억제제로 페그세타코플란(Pegcetacoplan, 제품명: 엠파벨리 주 EmpaveliⓇ, 한독)이 2021년 미국 FDA와 유럽 EMA 및 2024년 5월 국내에서 ‘성인의 발작성 야간혈색소뇨증(PNH)의 치료’에 승인되었다. 동일 성분의 페그세타코플란(Pegcetacoplan, 제품명: 사이포브레 주 SyfovreⓇ, Apelis)는 2023년 미국 FDA로부터 유리체강 내 주사(intravitreal injection)로 ‘나이 관련 황반변성(age-related macular degeneration, AMD)으로 인한 지도모양위축(Geographic Atrophy, GA) 치료제’에 승인된 바 있다.이 약제는 C3 및 C3b를 직접 억제하는 근위 보체(proximal complement) 억제제로, CP, LP, AP 등 모든 보체 활성화 경로에서 C3 전환 이후의 반응을 포괄적으로 차단한다. 이로 인해 IVH와 EVH를 동시에 억제할 수 있다.특히, 기존 C5 억제제 치료에도 빈혈이 지속되는 환자에게 임상적 유용성을 입증하였다. 다만, 보체 전체의 광범위한 억제에 따른 감염 위험성 증가와 투여 주기(주 2회 피하 주사)에 대한 고려가 필요하다.세 번째, 보체 대체 경로(AP)를 선택적으로 차단하는 경구용 억제제로 이프타코판(Iptacopan, 제품명: 파발타 캡슐, FabhaltaⓇ, 노바티스)과 다니코판(Danicopan, 제품명: 보이데야 정, VoydeyaⓇ, 아스트라제네카)이 있다.이들 약제는 AP 중심의 병태생리를 가진 PNH 환자 또는 C5 억제제에 불충분한 반응을 보이는 환자에서 선택적이고 효과적인 보체 조절을 가능하게 하며, 경구 투약 경로와 병용 치료를 통해 치료 접근성 및 환자 편의성을 향상시킬 수 있다.이프타코판은 2023년 미국 FDA, 2024년 5월 유럽 EMA 및 2024년 8월 국내에서 ‘성인의 발작성 야간혈색소뇨증(PNH의 치료’에 승인되었다. 이 약제는 최초의 경구용 PNH 치료제이며, 인자 B(Factor B)를 표적으로 하는 선택적 대체 경로(AP) 억제제이다.이 약제는 적혈구막에 존재하는 Factor B 및 AP 경로의 C3 전환효소(C3bBb)에 결합하여 그 활성을 저해하고, 더 나아가 AP 경로의 C5 전환효소(C3bC3bBb) 형성까지 차단한다. 결과적으로, 보체 활성화의 증폭 루프를 차단하여 C3b 의존적 EVH와 C5 매개 IVH를 모두 억제하는 기전을 가진다. 이러한 작용 특성으로 인해 기존의 C5 억제제를 대체할 수 있는 차세대 보체 억제제라고 할 수 있다.다니코판은 2024년 미국 FDA, 유럽 EMA 및 국내에서 “성인의 발작성야간 혈색소뇨증(PNH)의 기존에 C5 억제제(라불리주맙 또는 에쿨리주맙)를 투여 중인 PNH 환자에서 혈관 외 용혈(EVH) 증상이나 징후가 있는 경우 라불리주맙 혹은 에쿨리주맙에 부가요법”으로 승인받았다.이 약제는 인자 D(Factor D)에 가역적으로 결합하는 선택적 대체 경로(AP) 억제제로, C3 전환효소 형성의 초기 단계를 저해하는 기전을 갖는다. Factor D는 Factor B가 C3b와 결합한 복합체(C3bB)를 활성화하여 Bb와 Ba로 절단하는 세린계 단백질분해효소로, 이는 AP의 C3 전환효소(C3bBb) 형성의 핵심 단계이다. 이 약제는 이 과정에서 Factor D의 활성을 억제함으로써 Bb 형성을 차단하고, 최종적으로 C3bBb 복합체의 생성을 저해한다. 그러나 이프타코판과는 달리, 이 약제는 이미 형성된 C3 전환효소(C3bBb) 및 C5 전환효소(C3bBbC3b)에 직접 작용하지 않으므로 이들 복합체의 활성을 직접 억제하지는 않는다.C5 억제제는 어떤 약제인가?C5 억제제는 보체 연쇄 반응의 말단 용혈 경로를 차단하기 위해 C5에 결합하여 이를 억제하는 보체 기반 치료제이다. 이들 약제는 C5b 생성을 억제하고, 막공격복합체(MAC)의 형성을 차단함으로써, 보체-매개 혈관 내 용혈(IVH)로부터 PNH 적혈구를 보호하는 기전을 갖는다.C5 억제제 치료를 받은 PNH 환자는 임상적 개선이 뚜렷하게 나타난다. 치료 후 IVH의 생화학적 지표인 젖산탈수소효소(lactate dehydrogenase, LDH) 수치가 유의하게 감소하며, 이는 IVH이 효과적으로 억제되었음을 의미한다.PNH 적혈구의 클론 크기는 대체로 증가하는 경향을 보이나, 백혈구 계열의 클론 크기에는 뚜렷한 변화가 관찰되지 않는다. 헤모글로빈 수치는 대부분 정상 하한 이하에서 유지되며, 절대 망상적혈구 수(absolute reticulocyte count, ARC)는 지속적으로 정상 상한치를 초과하는 양상을 보인다. 이는 지속적인 용혈에도 불구하고 골수의 보상 반응이 활발하게 유지되고 있음을 시사한다.이러한 유의한 임상적 이점에도 불구하고, C5 억제제는 본질적인 한계를 지닌다. C5의 억제를 통해 보체 연쇄 반응의 말단 효과기 기전은 차단되지만, 상위 단계인 C3의 활성화는 여전히 조절되지 않은 채 지속된다.PNH 적혈구는 보체 조절 단백질인 CD55 및 CD59의 발현 또한 결핍되어 있어, 세포 표면에 과도한 C3b가 침착된다. 침착된 C3b는 다시 분해되어 C3dg(degradation fragment g) 등의 분절 단백질을 형성하며, 이들 단백질은 CR2(complement receptor 3, 보체 수용체 2) 등과 결합한다. 이로 인해 적혈구는 간과 비장에 분포한 모세망내계(RES)의 식세포에 의해 인식되고 제거된다. 이러한 식세포- 매개 적혈구 제거가 EVH의 원인 된다.지속적인 EVH는 경미한 LDH 상승, 혈중 하플로글로빈의 소실, 총 빌리루빈 상승, ARC 증가, 그리고 정상 이하의 헤모글로빈 농도를 동반한 안정화된 만성 빈혈 등의 생화학적 지표로 나타난다.따라서, C5 억제제는 보체 말단 경로를 효과적으로 차단하여 IVH는 억제하지만, 보체 활성의 상위 경로에서 생성되는 C3b의 침착을 충분히 제어하지 못해 EVH가 발생할 수 있다.크로발리주맙은 에쿨리주맙과 약리학적으로 어떤 차이가 있는가?에쿨리주맙과 크로발리주맙은 보체 단백질 C5를 표적으로 하는 단클론항체로, 막공격복합체(MAC)의 형성을 억제함으로써 PNH 등 보체 매개 질환의 치료에 사용된다. 두 약제는 동일한 표적을 공유하지만, 결합 부위, 작용 기전, 항체 구조, 체내 약동학적 특성 등에서 중요한 약리학적 차이를 보인다.1. C5 결합 부위 및 유전자 변이에 대한 반응성에쿨리주맙은 C5의 α-사슬에 결합하여 C5 전환효소에 의한 절단(C5a 및 C5b 생성)을 차단함으로써 MAC 형성을 억제한다. 그러나 이 약제는 C5의 특정 유전자 변이(R885H 등)에 대해 결합력이 감소하므로, 일부 환자에서는 충분한 치료 효과를 기대하기 어렵다. 반면, 크로발리주맙은 C5의 β-사슬에 결합함으로써, 야생형뿐만 아니라 C5 변이형에 대해서도 안정적이고 지속적인 억제 효과를 나타낸다.2. 작용 기전의 차이두 약제 모두 C5 절단을 차단하여 MAC 형성을 억제하지만, 크로발리주맙은 형성된 C5b6 복합체의 세포막 침착까지 억제하는 이중 기전을 가진다. 이로 인해 C5 절단 억제뿐만 아니라 잔여 보체 활성으로 인한 조직 손상 가능성까지 추가적으로 제한할 수 있다. 반면, 에쿨리주맙은 이러한 C5b6 억제 기전을 갖고 있지 않다.3. 항체 구조 및 재활용 기술에쿨리주맙은 기존의 인간화 IgG2/4 단클론항체로, 세포 내로 흡수된 이후 리소좀 내에서 분해된다. 그 결과 체내 반감기는 약 11일로 짧으며, 2주 간격의 정맥 주사 투여가 필요하다. 반면, 크로발리주맙은 SMART 기술이 적용된 항체로, pH 의존적 항원 결합 및 FcRn(Fc receptor neonatal) 매개 재활용 메커니즘을 통해 체내에서 효율적으로 재순환된다. 이로 인해 반감기가 연장되며, 동일한 용량으로도 더 오랜 기간 동안 효과를 유지할 수 있다.4. 투여 방식 및 환자 편의성에쿨리주맙은 정맥 주사만 가능하며, 자가 투여가 불가능하여 치료 순응도와 환자 편의성이 낮은 편이다. 반면, 크로발리주맙은 피하 주사로도 투여가 가능하며, 자가 투여 역시 가능하다. 또한, 투여 간격이 4~8주까지 연장 가능하여 장기 치료에서의 환자 부담을 줄일 수 있다.크로발리주맙은 어떤 약제인가?크로발리맙(Crovalimab, 제품명 PiaSky®)은 보체 단백질 C5를 표적으로 하는 인간화 단클론항체로, 약물 설계 단계에서부터 SMART(Sequential Monoclonal Antibody Recycling Technology) 플랫폼이 적용된 차세대 보체 억제제이다. 이 약제는 pH-의존적 항원 결합 특성과 FcRn(neonatal Fc receptor, 신생아 Fc 수용체) 매개 재활용 기전을 활용함으로써, 항체의 반감기를 연장하고 투약 용량 및 빈도를 감소시키는 데 기여한다. 또한, C5 유전자의 특정 변이(R885H 등)로 인해 기존 C5 억제제(예: 에쿨리주맙, 라불리주맙)에 저항성을 보이는 환자군에서도 안정적인 약물 반응성을 유지하는 이점이 보고되었다.크로발리맙의 SMART 기술은 항체가 표적에 결합한 후에도 세포 내 분해되지 않고 재활용될 수 있도록 설계된 항체 공학 기술이다. 이 기술의 핵심 기전은 다음 세 가지로 요약된다.첫째, FcRn는 항체의 Fc 영역에 결합하여, 세포 내 리소좀 분해를 회피하고 항체가 혈류로 다시 방출(recycling)될 수 있도록 한다. 이를 통해 항체의 체내 반감기가 연장되며, 장시간 약리 효과가 유지된다.둘째, pH-의존적 친화력 조절 기능(pH-dependent affinity tuning)은 항체가 엔도솜 내 산성 환경(pH 5.5 이하)에서는 항원(C5)으로부터 이탈하고 FcRn에 결합하며, 혈중 중성 pH에서는 다시 표적에 결합하도록 설계되었다. 이러한 pH 의존적 해리 및 재결합 특성은 반복적인 항원 차단을 가능하게 한다.셋째, 등전점 조절(isoelectric point tuning)을 통해 항체의 산성 환경에서의 용해도 및 표적 결합 특성이 조절되어, 세포 내 효율적인 수송과 재방출이 가능해진다. 이를 통해 항체는 기존 항체 대비 적은 용량으로도 지속적인 약리 효과를 발휘하며, 투여 빈도를 줄일 수 있어 치료 편의성 및 비용 효율성 측면에서 이점을 제공한다.이와 같은 재활용 기반 항체 특성은 C5와의 효율적인 결합 및 세포 내 표적 단백질 제거, FcRn 매개 항체의 재활용, 향상된 약물 지속 시간으로 이어진다. 또한, 크로발리맙은 높은 용해성을 가지고 있으므로 소량으로도 피하 주사가 가능하다.이러한 크로발리맙의 임상 개발은 COMPOSER(1/2상), COMMODORE 1 및 2(3상), COMMODORE 3(중국 내 3상) 임상시험을 통해 진행되었다. 이 중 3상 무작위 배정 비교 임상인 COMMODORE 2 연구는 C5 억제제 치료 경험이 없는 PNH 환자를 대상으로 수행되었으며, 이 결과를 바탕으로 미국 FDA 승인을 획득하였다.이 연구에서 크로발리맙은 4주 간격의 피하 주사로 투여되었으며, 질병 조절 효능과 안전성이 기존 치료제인 에쿨리주맙 대비 비열등(non-inferior)한 것으로 입증되었다. 치료 관련 이상반응 발생률 역시 두 치료제 간에 유의한 차이를 보이지 않았다.크로발리맙은 초기 정맥 투여 부하 용량으로 치료를 시작하며, 이후 4주간 주 1회 피하 투여를 통해 부하 용량을 유지한다. 이후에는 환자 교육을 통해 자가 투여가 가능하도록 설계되어 있으며, 4주 간격의 유지 요법은 기존 2주 간격의 정맥 투여 기반 치료에 비해 투약 빈도를 감소시키는 이점을 갖는다.미국 FDA의 허가에 따르면, 크로발리맙은 ‘체중 40kg 이상의 13세 이상 소아 및 성인 PNH 환자’를 적응증으로 승인되었으며, 심각한 수막구균 감염 위험을 줄이기 위한 REMS(Risk Evaluation and Mitigation Strategy) 프로그램 하에 처방 및 조제가 이루어지도록 규정되었다.크로발리주맙의 허가임상은COMMODORE 2 연구는 보체 억제제 치료 경험이 없는 PNH 환자를 대상으로 크로발리맙의 유효성과 안전성을 평가하기 위해 수행된 활성 대조, 공개 라벨, 비열등성 3상 무작위 배정 임상 시험이다.총 204명의 환자가 등록되었으며, 이들은 2:1 비율로 무작위 배정되어 크로발리맙(n=135) 또는 에쿨리주맙(n=69)을 투여받았다. 크로발리맙은 1일차에 정맥 주사로 단회 초기 용량을 투여한 뒤, 2일차부터 22일차까지 총 4회, 주 1회 피하 주사로 투여되었고, 이후 29일차부터는 4주 간격의 피하 주사를 통해 유지요법을 진행하였다.이 연구는 총 24주간의 주요 치료 기간(primary treatment period)으로 구성되었으며, 이후에는 환자에게 크로발리맙 치료를 지속하거나 전환할 수 있는 연장 투여 기간(extension period)이 제공되었다. 대상 환자는 혈중 LDH 수치가 정상 상한값(ULN)의 2배 이상이며, 최근 3개월 이내에 하나 이상의 PNH 관련 증상 또는 징후가 있었던 경우에 한해 포함되었다.무작위 배정은 최근 LDH 수치(≥2×ULN∼≤4× ULN 또는 ≽4×ULN)와 수혈 이력(0회, 1∼6회, 또는 6회 이상)에 따라 층화(stratification)하여 수행되었다.주요 유효성 평가지표는 다음과 같다:수혈 회피(Transfusion avoidance) 환자의 비율: 베이스라인부터 25주차까지 농축 적혈구(pRBC) 수혈 없이 유지된 환자의 비율로 평가되었다. 용혈 조절(Hemolysis control) 도달 환자의 비율: 5주차부터 25주차까지의 기간 동안 평균적으로 LDH 수치가 ULN의 1.5배 이하로 유지된 환자의 비율을 측정하였다. 돌파성 용혈(Breakthrough hemolysis, BTH) 발생 환자의 비율: LDH가 일시적으로 1.5×ULN 이하로 조절되었다가 이후 2×ULN 이상으로 상승하고, 새로운 혹은 악화된 혈관 내 용혈의 증상 또는 징후가 함께 동반된 경우를 BTH로 정의하여 평가하였다. 혈색소 안정화(Stabilized hemoglobin) 환자의 비율: 수혈 없이 베이스라인 대비 혈색소 수치가 ≥2 g/dL 이상 감소하지 않은 환자의 비율로 평가되었다.주요 결과는 다음과 같다:수혈 회피 비율: 크로발리맙 군에서 65.7%, 에쿨리주맙 군에서 68.1%로 나타나 두 군 간 유사한 수준의 수혈 회피율이 관찰되었다. LDH ≤1.5×ULN에 도달한 환자의 비율: 크로발리맙 군에서 79.3%, 에쿨리주맙 군에서 79.0%로 양 군 간 차이가 없었으며, 이는 용혈 조절 측면에서 비열등성을 충족함을 시사한다. 돌파성 용혈 발생률: 크로발리맙 군에서 10.4%, 에쿨리주맙 군에서 14.5%로, 오히려 크로발리맙에서 더 낮은 경향을 보였다. 혈색소 안정화율: 크로발리맙 군에서 63.4%, 에쿨리주맙 군에서 60.9%로 나타나, 혈색소 유지 효과 역시 비슷한 수준으로 평가되었다.크로발리주맙은 어떤 쟁점이 있는가?크로발리맙은 기존의 C5 억제 치료에서 동반되던 여러 제한점을 극복하고자 개발된 차세대 보체 억제제로, SMART 기반 항체 엔지니어링 기술을 적용한 최초의 월 1회 피하 주사 형태의 치료제이다. 이 약제는 C5에 반복적으로 결합 및 억제할 수 있도록 설계되어, 체내에서 장기간 작용하며, 상대적으로 적은 용량으로도 치료 효과를 유지할 수 있는 것이 특징이다.크로발리맙은 보체 연쇄 반응의 말단인 C5를 표적으로 결합하여 C5a 및 C5b의 생성을 차단함으로써 MAC 형성을 억제하고, 빠르고 지속적인 보체 억제를 유도한다. 특히 혈중에서 FcRn 매개 항체 재활용 기전을 통해 반복적으로 작용할 수 있어, 4주 간격 투여가 가능하다.기존 치료제는 모두 C5의 α-사슬을 표적으로 하는 반면, 크로발리맙은 C5의 β-사슬에 결합하여 작용한다. 이로 인해 R885H와 같은 특정 C5 유전자 변이 보유 환자에서 기존 치료제에 비해 더 높은 결합력과 억제 효과를 나타낼 수 있어, 기존 치료제에 반응하지 않는 환자군에 대한 새로운 치료 옵션으로 제시된다.한편, 크로발리맙과 기존 치료제를 병용하거나, 교체 투여 중 두 약제가 동시에 투여되는 경우, 각기 다른 C5 에피토프에 결합하는 항체들 사이에서 약물–표적–약물 복합체(drug–target–drug complex, DTDC)가 형성될 수 있다. 이 복합체는 면역복합체의 일종으로 간주될 수 있으며, 교체 기간 중 약물의 안전성 및 유효성에 영향을 줄 가능성이 제기된다. 이에 따라, C5 억제제 간 전환 시에는 신중한 임상적 고려와 면밀한 환자 모니터링이 필요하다.크로발리맙은 자가 투여 가능한 피하주사 기반 PNH 치료제로, 정맥 주사 기반의 기존 치료제와 비교해 환자와 보호자의 치료 부담을 경감시킬 수 있다. 특히, 의료기관 방문의 빈도 감소와 자가 관리 가능성은 장기 치료가 필요한 PNH 환자에게 실질적인 삶의 질 향상을 제공할 수 있다.결론적으로, 크로발리맙(PiaSkyⓇ)은 C5 억제를 통한 기존 치료제의 보체 억제 전략의 유효성을 유지하면서도, 투여 경로의 간편화, 투여 간격의 연장, 특정 유전자 변이에 대한 대응력 등의 특성을 갖춘 차세대 보체 억제제로 평가된다. 이는 PNH 치료의 편의성과 맞춤화를 동시에 실현하는 전환점을 마련한 약제라 할 수 있다.참고문헌 1. Robert A. Brodsky “Paroxysmal nocturnal hemoglobinuria withoutGPI-anchor deficiency” J Clin Invest. 2019;129(12):5074-5076. 2. Peter Hillmen, Regina Horneff, Michael Yeh, Martin Kolev  and Pascal Deschatelets “Navigating the Complement Pathway to Optimize PNH Treatment with Pegcetacoplan and Other Currently Approved Complement Inhibitors“ Int. J. Mol. Sci. 2024, 25, 9477. 3. Carmelo Gurnari, Ishani Nautiyal, Simona Pagliuca. “Current Opinions on the Clinical Utility of Ravulizumab for the Treatment of ParoxysmalNocturnal Hemoglobinuria” Therapeutics and Clinical Risk Management 2021:17 1343–1351. 4. Regina Horneff, Barbara Czech, Michael Yeh andElena Surova. “Three Years On: The Role of Pegcetacoplan in Paroxysmal Nocturnal Hemoglobinuria (PNH) since Its Initial Approval” Int. J. Mol. Sci. 2024, 25(16), 8698. 5. Alexander Röth 1, Jun-ichi Nishimura 2, Zsolt Nagy 3, et al, “The complement C5 inhibitor crovalimab in paroxysmal nocturnal hemoglobinuria” Blood. 2020 Jan 24;135(12):912–920. 6. Melissa A. Colden, Melissa A. Colden, Sushant Kumar, et al “Insights Into the Emergence of Paroxysmal Nocturnal Hemoglobinuria” Front. Immunol., 2022 Volume 12 – 2021. 7. 기타 인터넷 자료(보도 자료, 제품 설명서 등)2025-05-13 18:10:35최병철 박사 -
 AZ 울토미리스, aHUS 급여적용에 교체투여 가속화[데일리팜=이탁순 기자] 비정형 용혈성 요독 증후군(atypical Hemolytic Uremic Syndrome, aHUS) 치료제 교체 투여가 이어지고 있다.올해 1월부터 기존 유일한 급여 적용 치료제였던 솔리리스(에쿨리주맙)에 이어 울토리미스(라불리주맙)가 급여 적용되면서 솔리리스를 쓰던 환자들이 울토미리스로 바꾸고 있는 것이다. 두 약은 모두 사전심사 약제로, 아스트라제네카가 공급한다.30일 업계에 따르면 심평원 진료심사평가위원회가 최근 공개한 솔리리스·울토리미스 2~3월 사전심사 심의 건수는 15개 사례로 나타났다.이 가운데 울토미리스 사전심사 신청 사례가 10개나 된다. 울토리미리스 10개 사례 중 9개는 승인, 1개는 불승인됐다.솔리리스 2개는 투여 종료 건이며, 2개는 승인, 1개는 불승인된 사례다.aHUS은 만성적으로 제어되지 않는 보체의 활동으로 혈전과 염증이 몸 전체에 있는 작은 혈관에 지속적으로 손상을 입히는 혈전성 미세혈관병증(Thrombotic Microangiopathy, TMA)이 발생하는 희귀질환으로, 환자의 약 79%가 발병 후 3년 내 사망하거나 투석이 필요하며 영구적인 신장 손상이 발생하는 것으로 알려졌다.유일한 치료제인 솔리리스가 2018년 7월부터 건강보험 급여 적용됐다. 다만, 고가 약제로 급여 관리 차원에서 사전 심사를 통해 급여 적용여부를 결정하고 있다. 문제는 사전 심사 승인율이 30~40%대로 낮아 환자 접근성을 위해서는 사전심사 요건을 완화하든지, 사후심사로 전환해야 한다는 주장이 나오고 있다.이런 가운데 솔리리스보다 업그레이드된 울토미리스가 올해 1월부터 aHUS 질환에 급여 적용된 것이다. 울토미리스는 솔리리스 대비 반감기가 약 4배 늘어난 차세대 C5 보체 억제제로, 솔리리스가 2주 간격으로 투여가 필요한 반면, 울토미리스는 8주로 투여 간격을 늘려 편의성을 개선한 점이 특징이다.투여 편의성이 크게 나아진만큼 기존 솔리리스를 쓰던 환자들도 울토미리스로 교체하는 분위기다. 이번에 공개된 10개 사례 모두 교체 투여 건이었다.9개 승인 사례를 보면 솔리리스 투여 시기가 2024년 3건, 2023년 2건, 2022년 2건, 2021년 1건, 2018년 1건으로, 울토미리스 교체투여를 위해 요양급여 대상을 신청해 조건이 맞아 승인됐다. 불승인 1건 사례는 2022년 솔리리스를 사용했는데, 증상이 호전되어 투여중지가 필요하다는 위원회 의견에 따라 불승인됐다.앞으로도 기존 솔리리스 투여 환자가 울토미리스로 교체 투여하는 사례는 더욱 늘어날 전망이다. 복지부는 울토리미스 급여기준을 마련하면서 교체투여 기준도 명확히 했다.기존 솔리리스를 투여 중인 환자가 울토미리스로 교체투여 하는 경우, 울토미리스 급여기준에 따라 투여유지 기준에 부합해야 하며, 중단기준에 해당되지 않아야 한다고 명시했다. 또한 동시에 치료 효과 평가를 위한 모니터링 및 투여기간 기산 시점은 솔리리스가 투여된 시점으로 산정한다는 내용을 공지했다.다만, 울토미리스 급여 적용으로 aHUS 환자의 사전 심사율이 오를지는 아직 미지수다. 여전히 신규 환자에서는 불승인 사례가 더 나오고 있기 때문이다.업계 관계자는 "작년 11월부터 PNH(야간혈색소뇨증) 질환에 솔리리스·울토미리스 투여 시 진행했던 급여 사전심사를 일반심사로 전환했는데, 환자 치료를 위해서는 aHUS 질환에 대해서도 사전심사를 폐지해야 한다"고 목소리를 높였다.2025-04-30 21:15:08이탁순
AZ 울토미리스, aHUS 급여적용에 교체투여 가속화[데일리팜=이탁순 기자] 비정형 용혈성 요독 증후군(atypical Hemolytic Uremic Syndrome, aHUS) 치료제 교체 투여가 이어지고 있다.올해 1월부터 기존 유일한 급여 적용 치료제였던 솔리리스(에쿨리주맙)에 이어 울토리미스(라불리주맙)가 급여 적용되면서 솔리리스를 쓰던 환자들이 울토미리스로 바꾸고 있는 것이다. 두 약은 모두 사전심사 약제로, 아스트라제네카가 공급한다.30일 업계에 따르면 심평원 진료심사평가위원회가 최근 공개한 솔리리스·울토리미스 2~3월 사전심사 심의 건수는 15개 사례로 나타났다.이 가운데 울토미리스 사전심사 신청 사례가 10개나 된다. 울토리미리스 10개 사례 중 9개는 승인, 1개는 불승인됐다.솔리리스 2개는 투여 종료 건이며, 2개는 승인, 1개는 불승인된 사례다.aHUS은 만성적으로 제어되지 않는 보체의 활동으로 혈전과 염증이 몸 전체에 있는 작은 혈관에 지속적으로 손상을 입히는 혈전성 미세혈관병증(Thrombotic Microangiopathy, TMA)이 발생하는 희귀질환으로, 환자의 약 79%가 발병 후 3년 내 사망하거나 투석이 필요하며 영구적인 신장 손상이 발생하는 것으로 알려졌다.유일한 치료제인 솔리리스가 2018년 7월부터 건강보험 급여 적용됐다. 다만, 고가 약제로 급여 관리 차원에서 사전 심사를 통해 급여 적용여부를 결정하고 있다. 문제는 사전 심사 승인율이 30~40%대로 낮아 환자 접근성을 위해서는 사전심사 요건을 완화하든지, 사후심사로 전환해야 한다는 주장이 나오고 있다.이런 가운데 솔리리스보다 업그레이드된 울토미리스가 올해 1월부터 aHUS 질환에 급여 적용된 것이다. 울토미리스는 솔리리스 대비 반감기가 약 4배 늘어난 차세대 C5 보체 억제제로, 솔리리스가 2주 간격으로 투여가 필요한 반면, 울토미리스는 8주로 투여 간격을 늘려 편의성을 개선한 점이 특징이다.투여 편의성이 크게 나아진만큼 기존 솔리리스를 쓰던 환자들도 울토미리스로 교체하는 분위기다. 이번에 공개된 10개 사례 모두 교체 투여 건이었다.9개 승인 사례를 보면 솔리리스 투여 시기가 2024년 3건, 2023년 2건, 2022년 2건, 2021년 1건, 2018년 1건으로, 울토미리스 교체투여를 위해 요양급여 대상을 신청해 조건이 맞아 승인됐다. 불승인 1건 사례는 2022년 솔리리스를 사용했는데, 증상이 호전되어 투여중지가 필요하다는 위원회 의견에 따라 불승인됐다.앞으로도 기존 솔리리스 투여 환자가 울토미리스로 교체 투여하는 사례는 더욱 늘어날 전망이다. 복지부는 울토리미스 급여기준을 마련하면서 교체투여 기준도 명확히 했다.기존 솔리리스를 투여 중인 환자가 울토미리스로 교체투여 하는 경우, 울토미리스 급여기준에 따라 투여유지 기준에 부합해야 하며, 중단기준에 해당되지 않아야 한다고 명시했다. 또한 동시에 치료 효과 평가를 위한 모니터링 및 투여기간 기산 시점은 솔리리스가 투여된 시점으로 산정한다는 내용을 공지했다.다만, 울토미리스 급여 적용으로 aHUS 환자의 사전 심사율이 오를지는 아직 미지수다. 여전히 신규 환자에서는 불승인 사례가 더 나오고 있기 때문이다.업계 관계자는 "작년 11월부터 PNH(야간혈색소뇨증) 질환에 솔리리스·울토미리스 투여 시 진행했던 급여 사전심사를 일반심사로 전환했는데, 환자 치료를 위해서는 aHUS 질환에 대해서도 사전심사를 폐지해야 한다"고 목소리를 높였다.2025-04-30 21:15:08이탁순 -
 "PNH 치료 패러다임 변화…경구제 파발타 역할 확대될 것"고영일 서울대병원 혈액종양내과 교수[데일리팜=손형민 기자] “야간발작성혈색소뇨증(PNH) 치료환경이 많은 발전을 이뤄왔지만, 여전한 미충족 수요가 존재합니다. 환자 연령이 비교적 낮은 만큼 단순한 생존뿐 아니라 빈혈 개선과 일상 회복을 가능하게 하는 치료 전략의 필요성이 더욱 강조되고 있습니다. 이에 투여 편의성을 개선하고 빈혈 개선 효과를 보인 파발타의 활용도가 높아질 것으로 생각합니다.”고영일 서울대병원 혈액종양내과 교수는 최근 데일리팜과 만난 자리에서 PNH 치료 패러다임이 변화할 것이라고 강조했다.PNH는 후천적인 유전자 돌연변이에 의해 발생하는 희귀질환이다. 일반적으로 ‘후천성 돌연변이’라고 하면 암을 떠올리기 쉽지만, PNH는 혈액암이 아닌 ‘클론성 조혈증’의 일종으로 분류된다. 조혈모세포에 다수의 돌연변이가 생길 경우 혈액암으로 발전할 수 있지만, X염색체 유전자인 PIGA 유전자 하나에만 돌연변이가 발생할 경우 PNH가 발생한다.PNH는 현재까지 근본적인 치료법이 없는 질환으로 알려져 있다. 하지만 과학의 발전에 따라 보체 시스템의 활성을 억제하는 방식의 치료제가 개발되면서 치료 접근 방식이 바뀌고 있다. 보체 시스템은 선천 면역(innate immunity)의 핵심 요소로, 병원체를 직접 공격하고 파괴하는 강력한 방어 체계다. 이 시스템은 C3, C5 등 여러 경로로 구성돼 있으며, 최종적으로는 ‘막공격복합체(Membrane Attack Complex, MAC)’를 형성해 적혈구를 파괴하는 역할을 한다.그동안은 보체 시스템의 말단 경로에 위치한 C5를 억제하는 치료제가 주로 사용돼 왔다. 대표적으로 2주 간격으로 투여하는 주사제 솔리리스 이후 8주 간격으로 투여가능한 주사제 울토미리스가 도입되면서 치료 환경이 개선됐다. 현재까지도 많은 환자들이 이 치료제를 기반으로 질환을 관리하고 있다.다만 여전히 치료를 받고 있는 PNH 환자들 중 일부는 지속적인 피로감, 불충분한 증상 개선, 수혈 의존성 등의 미충족 수요가 존재한다. 특히 C5를 억제해도 상위 단계 C3의 활성화가 이어지면서, 결국 적혈구가 간·비장에서 조기 제거돼 수혈이 필요한 상황이 반복됐다.고 교수는 “통계적으로 C5 억제제만으로 증상이 충분히 조절돼 일상생활이 가능한 환자는 전체 PNH 환자의 약 20% 정도에 불과한 것으로 보고된다. 나머지 80%의 환자들은 증상이 완전히 조절되지 않으며, 이 중 절반 정도는 다른 치료 옵션의 필요성이 분명하게 드러나고 있다”고 평가했다.이어 “보체 시스템은 여러 경로로 구성되어 있으며, 상위 단계에 C3, 하위 단계에 C5가 위치한다. 기존의 C5 억제제는 하위 단계를 차단하는 방식으로 작용해왔지만, 실제 임상에서는 C5만 억제할 경우 위쪽 단계인 C3의 활성화가 여전히 문제로 작용할 수 있다는 점이 확인됐다”고 말했다.파발타, 경구옵션으로 첫 등장파발타는 이러한 문제를 해결하기 위해 개발된 치료제로, C3 활성화에 중요한 역할을 하는 B 인자를 억제하는 기전을 가진다. C3가 과활성화되는 것을 조절함으로써, 기존 C5 치료제에서 해결되지 않던 부분에 대한 새로운 치료 접근이 가능해진 것이다.이러한 기전을 바탕으로, 파발타는 기존 C5 억제제만으로는 해결되지 않았던 미충족 수요를 보완할 수 있는 새로운 치료 옵션으로 주목받고 있다. 특히 이 치료제는 빈혈과 혈관외 용혈 등에 효과를 보일 수 있다는 강점이 있다.파발타는 6개월 이상 C5 억제제를 투여받았음에도 잔류 빈혈(평균 헤모글로빈 수치 10g/dL 미만)이 있는 18세 이상의 성인 PNH 환자 97명을 대상으로 진행된 APPLY-PNH 임상3상 연구에서 효능을 확인했다. 무작위 배정을 통해 97명 중 35명은 C5 억제제 치료를 유지하고, 나머지 62명은 파발타로 전환해 24주간 치료 결과의 영향을 평가했다.임상 결과, 파발타로 치료를 변경한 환자들은 4주차부터 헤모글로빈 수치가 정상화됐으며, 이는 24주차까지 효과가 이어졌다. 약 3명 중 2명에서 이런 헤모글로빈 정상화가 확인됐다. 또 5명 중 4명은 임상적으로 유의한 헤모글로빈 수 증가를 보였으며, 95%의 환자가 수혈 의존성을 극복했다.파발타 복용으로 인해 치료를 중단해야 하는 이상반응은 발생하지 않았다. C5 억제제보다 돌발성 용혈 발생률이 유의하게 낮았으며 두통·설사·오심이 발생했으나 대체로 경미하고 1주 이내에 해소됐다고 교수는 “이 임상의 주요 목적은 빈혈 개선 효과를 확인하는 것이었으며, 파발타 투여군에서 헤모글로빈 수치 개선 비율이 80% 이상, 수혈을 회피한 경우는 약 90%에 달하는 결과를 보였다. 반면 기존 C5 억제제만 투여한 환자군에서는 이러한 개선 효과가 나타나지 않았다”고 전했다.이어 “이러한 결과는 파발타가 기존 치료제로는 해결되지 않았던 빈혈 문제를 개선하고, 수혈 의존도를 현저히 낮출 수 있는 치료 옵션임을 임상적으로 입증한 것으로 평가된다”고 덧붙였다.파발타의 강점은 제형이다. 경구제인 파발타는 기존 정맥주사 제형인 솔리리스, 울토미리스 대비 투약 편의성을 가져갈 수 있다. 실제로 임상현장에서 많은 환자들이 파발타가 보험 급여가 되면 약제를 바꾸고 싶다는 의사를 보이고 있으며, 헤모글로빈 수치 개선뿐만 아니라 경구제로 전환된다는 점에서 환자의 치료 만족도가 높아질 것이라는 게 고 교수의 설명이다.고 교수는 “PNH는 평균 발병 연령이 40대 초반으로, 비교적 젊은 연령층에서 많이 발생한다. 실제 진료 현장에서도 직장생활을 유지하며 치료를 받는 환자들이 많다”라며 “기존 치료제 중 하나인 울토미리스는 두 달에 한 번 투여하는 주사제로, 이전에 솔리리스에 비해 병원 방문 부담이 줄면서 환자들의 만족도가 크게 높아졌다. 이런 경험에서 볼 때, 파발타는 병원에 방문하지 않고도 복용할 수 있는 최초의 경구제로 복용 방식 자체만으로도 환자에게는 큰 변화로 볼 수 있다”라고 평가했다.여전한 미충족 수요 존재…치료환경 개선돼야”고 교수는 현재 다양한 보체 억제 기전을 기반으로 한 치료제들이 개발되고 있는 상황을 긍정적으로 평가했다. 기존 C5 억제제만으로는 해결되지 않았던 미충족 수요를 다양한 방식으로 보완할 수 있다는 점에서 의미가 크기 때문이다.일례로 파발타는 B 인자를, 한독의 엠파벨리(페그세타코플란)는 C3 인자를, 아스트라제네카의 보이데야(다니코판)는 D 인자를 억제하는 기전을 갖고 있으며, 약제마다 작용 위치가 다르기 때문에 각기 다른 치료 프로파일을 보인다.고 교수는 “이들 치료제는 모두 미충족 수요를 충족시키는 데 효과적일 수 있지만, 투약 방식이나 병용 여부에 따라 장단점이 뚜렷하다. 엠파벨리의 경우 주 2회 피하주사를 맞아야 하기 때문에 투약 부담이 있는 편이지만, 주사에 대한 거부감이 적은 환자에게는 충분히 효과적인 옵션이 될 수 있다. 반면 보이데야는 C5 억제제와 병용 투여가 필요해 복약 부담이 크지만, 병용 주사제를 통해 오히려 순응도 관리는 더 용이할 수 있다는 장점도 있다”라고 말했다.이어 ”다만 국내 급여 기준상 초기 치료는 여전히 C5 억제제로 시작할 수밖에 없는 구조이기 때문에, 실제 진료 현장에서는 빈혈 등 미충족 수요가 발생했을 때 어떤 약제로 전환할지를 두고 환자와 상의하는 경우가 많다”라고 전했다.현재 한국노바티스는 보험급여 마지막 관문인 국민건강보험공단과의 약가협상을 진행하고 있다.고 교수는 “환자들과 논의하다 보면 파발타의 급여 적용을 기다리는 경우가 상당수 존재한다. 일부 환자에게는 엠파벨리를 권유하기도 했지만, 주 2회 주사라는 점에서 부담을 느껴 지금은 불편하지만 경구제 보험 적용 이후 전환하겠다는 의사를 밝히는 사례도 적지 않다. 특히 이러한 경향은 사회활동이 활발한 젊은 환자들에서 더 두드러진다”라고 말했다.이어 “파발타는 1차 치료옵션으로서도 가능성을 보였다. 향후에는 현재 개발된 신규 기전의 치료제들이 1차 치료제로 채택될 수 있어야, PNH 환자들이 보다 실질적이고 완전한 치료 환경 속에서 관리 받고 있다고 말할 수 있을 것”이라고 강조했다.2025-04-29 06:00:00손형민
"PNH 치료 패러다임 변화…경구제 파발타 역할 확대될 것"고영일 서울대병원 혈액종양내과 교수[데일리팜=손형민 기자] “야간발작성혈색소뇨증(PNH) 치료환경이 많은 발전을 이뤄왔지만, 여전한 미충족 수요가 존재합니다. 환자 연령이 비교적 낮은 만큼 단순한 생존뿐 아니라 빈혈 개선과 일상 회복을 가능하게 하는 치료 전략의 필요성이 더욱 강조되고 있습니다. 이에 투여 편의성을 개선하고 빈혈 개선 효과를 보인 파발타의 활용도가 높아질 것으로 생각합니다.”고영일 서울대병원 혈액종양내과 교수는 최근 데일리팜과 만난 자리에서 PNH 치료 패러다임이 변화할 것이라고 강조했다.PNH는 후천적인 유전자 돌연변이에 의해 발생하는 희귀질환이다. 일반적으로 ‘후천성 돌연변이’라고 하면 암을 떠올리기 쉽지만, PNH는 혈액암이 아닌 ‘클론성 조혈증’의 일종으로 분류된다. 조혈모세포에 다수의 돌연변이가 생길 경우 혈액암으로 발전할 수 있지만, X염색체 유전자인 PIGA 유전자 하나에만 돌연변이가 발생할 경우 PNH가 발생한다.PNH는 현재까지 근본적인 치료법이 없는 질환으로 알려져 있다. 하지만 과학의 발전에 따라 보체 시스템의 활성을 억제하는 방식의 치료제가 개발되면서 치료 접근 방식이 바뀌고 있다. 보체 시스템은 선천 면역(innate immunity)의 핵심 요소로, 병원체를 직접 공격하고 파괴하는 강력한 방어 체계다. 이 시스템은 C3, C5 등 여러 경로로 구성돼 있으며, 최종적으로는 ‘막공격복합체(Membrane Attack Complex, MAC)’를 형성해 적혈구를 파괴하는 역할을 한다.그동안은 보체 시스템의 말단 경로에 위치한 C5를 억제하는 치료제가 주로 사용돼 왔다. 대표적으로 2주 간격으로 투여하는 주사제 솔리리스 이후 8주 간격으로 투여가능한 주사제 울토미리스가 도입되면서 치료 환경이 개선됐다. 현재까지도 많은 환자들이 이 치료제를 기반으로 질환을 관리하고 있다.다만 여전히 치료를 받고 있는 PNH 환자들 중 일부는 지속적인 피로감, 불충분한 증상 개선, 수혈 의존성 등의 미충족 수요가 존재한다. 특히 C5를 억제해도 상위 단계 C3의 활성화가 이어지면서, 결국 적혈구가 간·비장에서 조기 제거돼 수혈이 필요한 상황이 반복됐다.고 교수는 “통계적으로 C5 억제제만으로 증상이 충분히 조절돼 일상생활이 가능한 환자는 전체 PNH 환자의 약 20% 정도에 불과한 것으로 보고된다. 나머지 80%의 환자들은 증상이 완전히 조절되지 않으며, 이 중 절반 정도는 다른 치료 옵션의 필요성이 분명하게 드러나고 있다”고 평가했다.이어 “보체 시스템은 여러 경로로 구성되어 있으며, 상위 단계에 C3, 하위 단계에 C5가 위치한다. 기존의 C5 억제제는 하위 단계를 차단하는 방식으로 작용해왔지만, 실제 임상에서는 C5만 억제할 경우 위쪽 단계인 C3의 활성화가 여전히 문제로 작용할 수 있다는 점이 확인됐다”고 말했다.파발타, 경구옵션으로 첫 등장파발타는 이러한 문제를 해결하기 위해 개발된 치료제로, C3 활성화에 중요한 역할을 하는 B 인자를 억제하는 기전을 가진다. C3가 과활성화되는 것을 조절함으로써, 기존 C5 치료제에서 해결되지 않던 부분에 대한 새로운 치료 접근이 가능해진 것이다.이러한 기전을 바탕으로, 파발타는 기존 C5 억제제만으로는 해결되지 않았던 미충족 수요를 보완할 수 있는 새로운 치료 옵션으로 주목받고 있다. 특히 이 치료제는 빈혈과 혈관외 용혈 등에 효과를 보일 수 있다는 강점이 있다.파발타는 6개월 이상 C5 억제제를 투여받았음에도 잔류 빈혈(평균 헤모글로빈 수치 10g/dL 미만)이 있는 18세 이상의 성인 PNH 환자 97명을 대상으로 진행된 APPLY-PNH 임상3상 연구에서 효능을 확인했다. 무작위 배정을 통해 97명 중 35명은 C5 억제제 치료를 유지하고, 나머지 62명은 파발타로 전환해 24주간 치료 결과의 영향을 평가했다.임상 결과, 파발타로 치료를 변경한 환자들은 4주차부터 헤모글로빈 수치가 정상화됐으며, 이는 24주차까지 효과가 이어졌다. 약 3명 중 2명에서 이런 헤모글로빈 정상화가 확인됐다. 또 5명 중 4명은 임상적으로 유의한 헤모글로빈 수 증가를 보였으며, 95%의 환자가 수혈 의존성을 극복했다.파발타 복용으로 인해 치료를 중단해야 하는 이상반응은 발생하지 않았다. C5 억제제보다 돌발성 용혈 발생률이 유의하게 낮았으며 두통·설사·오심이 발생했으나 대체로 경미하고 1주 이내에 해소됐다고 교수는 “이 임상의 주요 목적은 빈혈 개선 효과를 확인하는 것이었으며, 파발타 투여군에서 헤모글로빈 수치 개선 비율이 80% 이상, 수혈을 회피한 경우는 약 90%에 달하는 결과를 보였다. 반면 기존 C5 억제제만 투여한 환자군에서는 이러한 개선 효과가 나타나지 않았다”고 전했다.이어 “이러한 결과는 파발타가 기존 치료제로는 해결되지 않았던 빈혈 문제를 개선하고, 수혈 의존도를 현저히 낮출 수 있는 치료 옵션임을 임상적으로 입증한 것으로 평가된다”고 덧붙였다.파발타의 강점은 제형이다. 경구제인 파발타는 기존 정맥주사 제형인 솔리리스, 울토미리스 대비 투약 편의성을 가져갈 수 있다. 실제로 임상현장에서 많은 환자들이 파발타가 보험 급여가 되면 약제를 바꾸고 싶다는 의사를 보이고 있으며, 헤모글로빈 수치 개선뿐만 아니라 경구제로 전환된다는 점에서 환자의 치료 만족도가 높아질 것이라는 게 고 교수의 설명이다.고 교수는 “PNH는 평균 발병 연령이 40대 초반으로, 비교적 젊은 연령층에서 많이 발생한다. 실제 진료 현장에서도 직장생활을 유지하며 치료를 받는 환자들이 많다”라며 “기존 치료제 중 하나인 울토미리스는 두 달에 한 번 투여하는 주사제로, 이전에 솔리리스에 비해 병원 방문 부담이 줄면서 환자들의 만족도가 크게 높아졌다. 이런 경험에서 볼 때, 파발타는 병원에 방문하지 않고도 복용할 수 있는 최초의 경구제로 복용 방식 자체만으로도 환자에게는 큰 변화로 볼 수 있다”라고 평가했다.여전한 미충족 수요 존재…치료환경 개선돼야”고 교수는 현재 다양한 보체 억제 기전을 기반으로 한 치료제들이 개발되고 있는 상황을 긍정적으로 평가했다. 기존 C5 억제제만으로는 해결되지 않았던 미충족 수요를 다양한 방식으로 보완할 수 있다는 점에서 의미가 크기 때문이다.일례로 파발타는 B 인자를, 한독의 엠파벨리(페그세타코플란)는 C3 인자를, 아스트라제네카의 보이데야(다니코판)는 D 인자를 억제하는 기전을 갖고 있으며, 약제마다 작용 위치가 다르기 때문에 각기 다른 치료 프로파일을 보인다.고 교수는 “이들 치료제는 모두 미충족 수요를 충족시키는 데 효과적일 수 있지만, 투약 방식이나 병용 여부에 따라 장단점이 뚜렷하다. 엠파벨리의 경우 주 2회 피하주사를 맞아야 하기 때문에 투약 부담이 있는 편이지만, 주사에 대한 거부감이 적은 환자에게는 충분히 효과적인 옵션이 될 수 있다. 반면 보이데야는 C5 억제제와 병용 투여가 필요해 복약 부담이 크지만, 병용 주사제를 통해 오히려 순응도 관리는 더 용이할 수 있다는 장점도 있다”라고 말했다.이어 ”다만 국내 급여 기준상 초기 치료는 여전히 C5 억제제로 시작할 수밖에 없는 구조이기 때문에, 실제 진료 현장에서는 빈혈 등 미충족 수요가 발생했을 때 어떤 약제로 전환할지를 두고 환자와 상의하는 경우가 많다”라고 전했다.현재 한국노바티스는 보험급여 마지막 관문인 국민건강보험공단과의 약가협상을 진행하고 있다.고 교수는 “환자들과 논의하다 보면 파발타의 급여 적용을 기다리는 경우가 상당수 존재한다. 일부 환자에게는 엠파벨리를 권유하기도 했지만, 주 2회 주사라는 점에서 부담을 느껴 지금은 불편하지만 경구제 보험 적용 이후 전환하겠다는 의사를 밝히는 사례도 적지 않다. 특히 이러한 경향은 사회활동이 활발한 젊은 환자들에서 더 두드러진다”라고 말했다.이어 “파발타는 1차 치료옵션으로서도 가능성을 보였다. 향후에는 현재 개발된 신규 기전의 치료제들이 1차 치료제로 채택될 수 있어야, PNH 환자들이 보다 실질적이고 완전한 치료 환경 속에서 관리 받고 있다고 말할 수 있을 것”이라고 강조했다.2025-04-29 06:00:00손형민 -
 JW중외·한독, 나란히 ITP 도입신약 공단 협상…급여 임박[데일리팜=이탁순 기자] JW중외제약과 한독이 도입한 만성 면역 혈소판 감소증(ITP) 치료제가 건강보험공단과 협상을 진행하고 있어 급여 등재에 파란불이 켜졌다.노바티스의 발작성 약간 혈색소뇨증(PNH) 신약도 협상 단계를 밟고 있다.21일 업계에 따르면 건보공단은 최근 이같은 협상 진행 사실을 홈페에지에 업데이트했다. 공단은 신약과 약가협상 생략 약제, 사용범위 확대 약제에 대한 협상 진행 사실을 홈페이지에 공개하고 있다.이번에 업데이트된 약제는 한독 '도프텔렛정20mg(아바트롬보팍말레산염)', 한국노바티스 '파발타캡슐200mg(입타코판염산염수화물)', JW중외제약 '타발리스정(포스타마티닙나트륨수화물)' 등 3개 품목이다.이들 약제는 지난 3월초 열린 약제급여평가위원회 심의를 받았다. 당시 도프텔렛과 타발리스는 평가금액 이하 수용시 급여의 적정성이 있다는 결과가 나왔는데, 제약사들이 결과를 수용하면서 협상 단계로 넘어온 것으로 풀이된다.특히, 대체약제 가중평균가의 90%를 수용하면 약가협상이 생략되기 때문에 두 약제는 공단과 예상청구금액 협상만 진행할 가능성이 높다는 분석이다.파발타캡슐은 약평위에서 급여 적정성을 인정받고, 곧바로 공단 협상 단계로 넘어왔다. 도프텔렛과 타발리스는 똑같이 ITP 적응증으로 급여 적정성을 인정받았다. ITP는 면역체계가 혈소판을 바이러스로 오인해 공격하는 자가면역질환으로 혈소판 수치가 정상 범위 이하로 감소하면서 출혈 위험이 증가하는 질환이다. 이에 환자는 멍이 쉽게 들고 출혈이 잦으며 심한 경우 뇌출혈이나 위장 출혈로 이어질 수 있다.대한혈액학회 ITP 임상진료지침에 따르면 1차 치료제로 스테로이드와 면역글로불린이 권장, 만성 ITP 환자의 경우 2차 치료제로 비장절제술이나 혈소판 작용체 수용제(TPO-RA)가 사용되고 있다.타발리스정은 ‘비장 티로신 인산화효소(Spleen Tyrosine Kinase, SYK)’를 억제해 혈소판 파괴를 저해하는 기전의 퍼스트인클래스 신약으로, 면역 반응을 조절하는 Fc 감마(γ) 수용체의 활성화를 차단해 과도한 면역 반응을 억제하며 이를 통해 혈소판 감소를 방지하는 효과가 있다.미국 제약사 라이젤 파마슈티컬이 개발한 이 약은 일본 킷세이제약이 상업화 권리를 갖고 있으며, JW중외제약이 국내 판권을 확보했다.도프텔렛은 혈소판생성인자 수용체 작용제(TPO-RA)로 경구제로, 골수 전구 세포로부터 거대핵세포의 증식과 분화를 자극해 혈소판 수를 증가시키는 기전을 갖고 있다.한독이 글로벌 바이오제약기업 소비(sobi)로부터 도입했다.현재 국내 사용되고 있는 ITP 치료제로는 노바티스 '레볼레이드'와 쿄와기린 '로미플레이트주'가 있다. 레보레이드는 작년 유비스트 기준 원외처방액 49억원을 기록했다.한편, 파발타가 적응증을 갖고 있는 PNH 치료제로는 솔리리스, 울토미리스, 엠파벨리 등이 국내 출시돼 있다.2025-04-21 10:25:48이탁순
JW중외·한독, 나란히 ITP 도입신약 공단 협상…급여 임박[데일리팜=이탁순 기자] JW중외제약과 한독이 도입한 만성 면역 혈소판 감소증(ITP) 치료제가 건강보험공단과 협상을 진행하고 있어 급여 등재에 파란불이 켜졌다.노바티스의 발작성 약간 혈색소뇨증(PNH) 신약도 협상 단계를 밟고 있다.21일 업계에 따르면 건보공단은 최근 이같은 협상 진행 사실을 홈페에지에 업데이트했다. 공단은 신약과 약가협상 생략 약제, 사용범위 확대 약제에 대한 협상 진행 사실을 홈페이지에 공개하고 있다.이번에 업데이트된 약제는 한독 '도프텔렛정20mg(아바트롬보팍말레산염)', 한국노바티스 '파발타캡슐200mg(입타코판염산염수화물)', JW중외제약 '타발리스정(포스타마티닙나트륨수화물)' 등 3개 품목이다.이들 약제는 지난 3월초 열린 약제급여평가위원회 심의를 받았다. 당시 도프텔렛과 타발리스는 평가금액 이하 수용시 급여의 적정성이 있다는 결과가 나왔는데, 제약사들이 결과를 수용하면서 협상 단계로 넘어온 것으로 풀이된다.특히, 대체약제 가중평균가의 90%를 수용하면 약가협상이 생략되기 때문에 두 약제는 공단과 예상청구금액 협상만 진행할 가능성이 높다는 분석이다.파발타캡슐은 약평위에서 급여 적정성을 인정받고, 곧바로 공단 협상 단계로 넘어왔다. 도프텔렛과 타발리스는 똑같이 ITP 적응증으로 급여 적정성을 인정받았다. ITP는 면역체계가 혈소판을 바이러스로 오인해 공격하는 자가면역질환으로 혈소판 수치가 정상 범위 이하로 감소하면서 출혈 위험이 증가하는 질환이다. 이에 환자는 멍이 쉽게 들고 출혈이 잦으며 심한 경우 뇌출혈이나 위장 출혈로 이어질 수 있다.대한혈액학회 ITP 임상진료지침에 따르면 1차 치료제로 스테로이드와 면역글로불린이 권장, 만성 ITP 환자의 경우 2차 치료제로 비장절제술이나 혈소판 작용체 수용제(TPO-RA)가 사용되고 있다.타발리스정은 ‘비장 티로신 인산화효소(Spleen Tyrosine Kinase, SYK)’를 억제해 혈소판 파괴를 저해하는 기전의 퍼스트인클래스 신약으로, 면역 반응을 조절하는 Fc 감마(γ) 수용체의 활성화를 차단해 과도한 면역 반응을 억제하며 이를 통해 혈소판 감소를 방지하는 효과가 있다.미국 제약사 라이젤 파마슈티컬이 개발한 이 약은 일본 킷세이제약이 상업화 권리를 갖고 있으며, JW중외제약이 국내 판권을 확보했다.도프텔렛은 혈소판생성인자 수용체 작용제(TPO-RA)로 경구제로, 골수 전구 세포로부터 거대핵세포의 증식과 분화를 자극해 혈소판 수를 증가시키는 기전을 갖고 있다.한독이 글로벌 바이오제약기업 소비(sobi)로부터 도입했다.현재 국내 사용되고 있는 ITP 치료제로는 노바티스 '레볼레이드'와 쿄와기린 '로미플레이트주'가 있다. 레보레이드는 작년 유비스트 기준 원외처방액 49억원을 기록했다.한편, 파발타가 적응증을 갖고 있는 PNH 치료제로는 솔리리스, 울토미리스, 엠파벨리 등이 국내 출시돼 있다.2025-04-21 10:25:48이탁순 -
 노바티스, 먹는 PNH 신약 '파발타' 약가협상 돌입[데일리팜=어윤호 기자] 먹는 PNH 신약 '파발타'가 보험급여로 향하는 마지막 관문에 돌입했다.관련 업계에 따르면 한국노바티스는 국민건강보험공단과 경구용 발작성혈색소뇨증(PNH, Paroxysmal Nocturnal Hemoglobinuria)치료제 파발타(입타코판)에 대한 약가협상을 진행 중이다.이에 따라, 또 하나의 PNH 치료옵션이 탄생할 수 있을지 귀추가 주목된다.PNH는 전 세계적으로 100만명 당 약 1.5명 정도가 발생하는 것으로 추정되는 희귀질환이다.이 질환의 치료는 그간 C5억제제에 의존했다. 2010년 '솔리리스(에쿨리주맙)'가 국내 처음 허가됐고, 2022년 '울토미리스(라불리주맙)'가 허가돼 PNH 치료에 사용돼 왔다. 두 치료옵션 모두 체내 면역에 관여하는 보체 시스템의 대체 경로 안에서 말단에 위치한 C5를 억제하는 기전인 C5 억제제이며 정맥주사제다.그러다 지난해 4월, C3 및 C3b에 결합해 보체연쇄반응을 억제하는 기전의 피하주사제 '엠파벨리(페그세타코플란)'가 허가됐고, 8월에는 B인자를 억제하는 기전의 경구제 파발타가 등장했다.C5 억제제의 기전적 한계로 남은 PNH 미충족 수요, 혈관 외 용혈(EVH)’ PNH는 적혈구에 유전적 결핍이 생기면서 시작되는데 이로 인해 혈관 내 용혈(IVH, Intravascular Hemolysis)과 혈관 외 용혈(EVH, Extravascular Hemolysis)이 발생한다.이런 용혈은 곧 혈전증, 골수부전을 야기해 생명을 위태롭게 만든다. 때문에 PNH 치료는 용혈을 조절하는 것이 중요한데 현재 PNH의 표준치료법인 C5 억제제는 IVH는 유의하게 조절하지만, 기전적으로 EVH는 조절하는데 한계가 있다.B인자억제제 파발타의 급여 등재에 관심이 모이는 이유다. B인자는 C5 뿐만 아니라 C3 및 C3b보다 대체 경로 내 상위에 존재하는 인자로 이를 억제할 경우 IVH 뿐만 아니라 EVH까지도 포괄적으로 조절할 수 있다.실제 파발타는 치료 경험이 없는 환자 대상에게 유효성을 보였다. 치료 경험이 없는 PNH 환자를 대상으로 한 APPOINT-PNH 연구에 따르면 환자 33명 중 19명은 적혈구 수혈 없이 헤모글로빈 수치가 12g/dL 이상에 도달했다.또한 92% 환자가 임상적으로 유의한 헤모글로빈 수 2g/dL 이상 증가를 보였으며, 수혈 없이 헤모글로빈 수치가 12g/dL 이상 지속된 환자는 63%였다. 연구 기간인 24주동안 헤모글로빈 수치가 지속적으로 증가하는 추세를 보였으며, 20주차부터는 헤모글로빈 정상화 수치에 도달해 24주 차까지 지속됐다. 또한 98%가 수혈 의존성을 극복했다.장준호 삼성서울병원 혈액내과 교수는 "C5 억제제가 처음 등장했을 당시, 전문가들은 PNH 치료의 패러다임이 전환됐다. 그러나 C5 억제제는 여전히 혈관 외 용혈(EVH)을 조절하는데 한계가 있다"고 말했다.아울러 "파발타는 PNH 치료의 또 한번의 패러다임 전환을 주도할 신약이다. B인자 억제라는 기전은 대체 경로의 상단에 위치한 B인자에 관여하기 때문에 혈관 내외 용혈을 모두 조절할 수 있으며 임상을 통해 고무적인 결과를 보였다"고 강조했다.2025-04-10 06:00:07어윤호
노바티스, 먹는 PNH 신약 '파발타' 약가협상 돌입[데일리팜=어윤호 기자] 먹는 PNH 신약 '파발타'가 보험급여로 향하는 마지막 관문에 돌입했다.관련 업계에 따르면 한국노바티스는 국민건강보험공단과 경구용 발작성혈색소뇨증(PNH, Paroxysmal Nocturnal Hemoglobinuria)치료제 파발타(입타코판)에 대한 약가협상을 진행 중이다.이에 따라, 또 하나의 PNH 치료옵션이 탄생할 수 있을지 귀추가 주목된다.PNH는 전 세계적으로 100만명 당 약 1.5명 정도가 발생하는 것으로 추정되는 희귀질환이다.이 질환의 치료는 그간 C5억제제에 의존했다. 2010년 '솔리리스(에쿨리주맙)'가 국내 처음 허가됐고, 2022년 '울토미리스(라불리주맙)'가 허가돼 PNH 치료에 사용돼 왔다. 두 치료옵션 모두 체내 면역에 관여하는 보체 시스템의 대체 경로 안에서 말단에 위치한 C5를 억제하는 기전인 C5 억제제이며 정맥주사제다.그러다 지난해 4월, C3 및 C3b에 결합해 보체연쇄반응을 억제하는 기전의 피하주사제 '엠파벨리(페그세타코플란)'가 허가됐고, 8월에는 B인자를 억제하는 기전의 경구제 파발타가 등장했다.C5 억제제의 기전적 한계로 남은 PNH 미충족 수요, 혈관 외 용혈(EVH)’ PNH는 적혈구에 유전적 결핍이 생기면서 시작되는데 이로 인해 혈관 내 용혈(IVH, Intravascular Hemolysis)과 혈관 외 용혈(EVH, Extravascular Hemolysis)이 발생한다.이런 용혈은 곧 혈전증, 골수부전을 야기해 생명을 위태롭게 만든다. 때문에 PNH 치료는 용혈을 조절하는 것이 중요한데 현재 PNH의 표준치료법인 C5 억제제는 IVH는 유의하게 조절하지만, 기전적으로 EVH는 조절하는데 한계가 있다.B인자억제제 파발타의 급여 등재에 관심이 모이는 이유다. B인자는 C5 뿐만 아니라 C3 및 C3b보다 대체 경로 내 상위에 존재하는 인자로 이를 억제할 경우 IVH 뿐만 아니라 EVH까지도 포괄적으로 조절할 수 있다.실제 파발타는 치료 경험이 없는 환자 대상에게 유효성을 보였다. 치료 경험이 없는 PNH 환자를 대상으로 한 APPOINT-PNH 연구에 따르면 환자 33명 중 19명은 적혈구 수혈 없이 헤모글로빈 수치가 12g/dL 이상에 도달했다.또한 92% 환자가 임상적으로 유의한 헤모글로빈 수 2g/dL 이상 증가를 보였으며, 수혈 없이 헤모글로빈 수치가 12g/dL 이상 지속된 환자는 63%였다. 연구 기간인 24주동안 헤모글로빈 수치가 지속적으로 증가하는 추세를 보였으며, 20주차부터는 헤모글로빈 정상화 수치에 도달해 24주 차까지 지속됐다. 또한 98%가 수혈 의존성을 극복했다.장준호 삼성서울병원 혈액내과 교수는 "C5 억제제가 처음 등장했을 당시, 전문가들은 PNH 치료의 패러다임이 전환됐다. 그러나 C5 억제제는 여전히 혈관 외 용혈(EVH)을 조절하는데 한계가 있다"고 말했다.아울러 "파발타는 PNH 치료의 또 한번의 패러다임 전환을 주도할 신약이다. B인자 억제라는 기전은 대체 경로의 상단에 위치한 B인자에 관여하기 때문에 혈관 내외 용혈을 모두 조절할 수 있으며 임상을 통해 고무적인 결과를 보였다"고 강조했다.2025-04-10 06:00:07어윤호 -
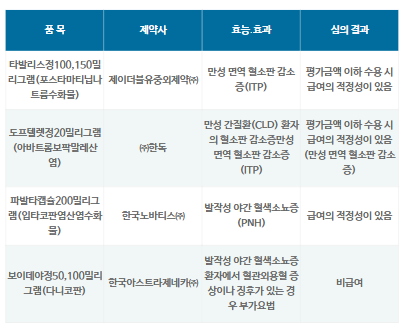 PNH 신약 '파발타', 약평위 통과...급여 적정성 인정[데일리팜=이혜경 기자] 노바티스의 입타코판 성분 발작성 야간 혈색소뇨증(PNH) 치료제 '파발타캡슐200mg(입타코판염산염수화물)'이 급여 첫 관문을 넘었다.건강보험심사평가원(원장 강중구)은 6일 '2025년 제3차 약제급여평가위원회'에서 심의한 결정신청 약제의 요양급여 적정성 결과를 공개했다.결정신청 약제의 요양급여 적정성 심의결과. 이번에 신청된 4개 약제 중 급여 적정성을 인정 받은 건 파발타가 유일하다. 파발타는 세계 최초의 경구용 PNH 치료제로, 그동안 '솔리리스(에쿨리주맙)', '울토미리스(라불리주맙)' 등 정맥 주사제에 의존하던 환자들의 복용 편의성이 높아질 것으로 보인다.제이더블유중외제약의 '타발리스정100, 150mg(포스타마티닙나트륨수화물)', 한독의 '도프텔렛정20mg(아바트롬보팍말레산염)'은 평가금액 이하를 수용해야 약평위 다음 단계로 넘어가게 된다.다만 도프텔렛은 한독이 신청한 ▲만성 간질환(CLD) 환자의 혈소판 감소증 ▲만성 면역 혈소판 감소증(ITP) 중 만성 면역 혈소판 감소증에서만 평가금액 이하 수용시 급여 적정성을 인정 받았다.한국아스트라제네카의 발작성 야간 혈색소뇨증 환자에서 혈관외용혈 증상이나 징후가 있는 경우 부가요법 치료제인 '보이데야정 50, 100mg(다니코판)'은 비급여 판정을 받았다.한편 위험분담계약 약제의 사용범위 확대 적정성 심의결과, 글락소스미스클라인의 '벤리스타주120, 400mg(벨리무맙)'은 성인 활동성 전신홍반루푸스 치료제까지 급여범위 확대하는데 적정성이 있다고 결정됐다.2025-03-06 19:34:52이혜경
PNH 신약 '파발타', 약평위 통과...급여 적정성 인정[데일리팜=이혜경 기자] 노바티스의 입타코판 성분 발작성 야간 혈색소뇨증(PNH) 치료제 '파발타캡슐200mg(입타코판염산염수화물)'이 급여 첫 관문을 넘었다.건강보험심사평가원(원장 강중구)은 6일 '2025년 제3차 약제급여평가위원회'에서 심의한 결정신청 약제의 요양급여 적정성 결과를 공개했다.결정신청 약제의 요양급여 적정성 심의결과. 이번에 신청된 4개 약제 중 급여 적정성을 인정 받은 건 파발타가 유일하다. 파발타는 세계 최초의 경구용 PNH 치료제로, 그동안 '솔리리스(에쿨리주맙)', '울토미리스(라불리주맙)' 등 정맥 주사제에 의존하던 환자들의 복용 편의성이 높아질 것으로 보인다.제이더블유중외제약의 '타발리스정100, 150mg(포스타마티닙나트륨수화물)', 한독의 '도프텔렛정20mg(아바트롬보팍말레산염)'은 평가금액 이하를 수용해야 약평위 다음 단계로 넘어가게 된다.다만 도프텔렛은 한독이 신청한 ▲만성 간질환(CLD) 환자의 혈소판 감소증 ▲만성 면역 혈소판 감소증(ITP) 중 만성 면역 혈소판 감소증에서만 평가금액 이하 수용시 급여 적정성을 인정 받았다.한국아스트라제네카의 발작성 야간 혈색소뇨증 환자에서 혈관외용혈 증상이나 징후가 있는 경우 부가요법 치료제인 '보이데야정 50, 100mg(다니코판)'은 비급여 판정을 받았다.한편 위험분담계약 약제의 사용범위 확대 적정성 심의결과, 글락소스미스클라인의 '벤리스타주120, 400mg(벨리무맙)'은 성인 활동성 전신홍반루푸스 치료제까지 급여범위 확대하는데 적정성이 있다고 결정됐다.2025-03-06 19:34:52이혜경 -
 제약업계, 도입신약 상업화 속도…미개척 시장 정조준[데일리팜=손형민 기자] 국내 제약바이오업계가 도입신약을 통해 미개척 시장 진출에 적극 나서고 있다. 최근 한독은 벨기에 아르젠엑스로부터 도입한 비브가트를 국내 허가받으며 중증근무력증 치료제를 확보했다. 이 회사는 아르젠엑스뿐만 아니라 미국 인사이트, 스웨덴 소비 등과의 협업을 통해 희귀질환 신약을 국내 도입하고 있다.도입신약은 수익성이 떨어지지만 암, 희귀질환 등 개척되지 않은 분야로 진출이 용이하다. 특히 국내 도입된 신약들은 글로벌 규제기관으로부터 효과를 인정받았기에 추가 임상이 필요하지 않다는 강점이 있다. 한독뿐만 아니라 제일약품, 보령 등 여러 국내사들이 글로벌 시장에서 검증된 신약 도입에 적극 나서고 있다.한독, 도입신약 적극 모색…솔리리스·울토미리스 공백 매우나25일 관련 업계에 따르면 식품의약품안전처는 최근 한독이 도입한 중증근무력증 치료제 ‘비브가트’를 허가 승인했다. 한독은 지난해 8월 비브가트 원 개발사인 아르젠엑스와 계약을 체결해 국내 허가 등록과 급여 진행, 독점 유통을 담당하게 됐다.비브가트는 면역글로불린G(IgG)의 방어수용체인 Fc 수용체(FcRn)를 차단하는 새로운 기전이다. 해당 기전은 질병을 유발하는 면역글로불린G 항체를 감소시키고 이를 재순환하는 과정을 차단한다. FcRn과 결합해 IgG 항체가 분해되지 않도록 하는 것이다. 비브가트는 현재 미국과 유럽, 영국, 이스라엘, 중국에서 전신 중증근무력증 성인 환자의 치료제로 승인된 바 있다.전신 중증근무력증은 신경이 근육에 신호를 전달하지 못해 골격근이 약화되는 만성 자가면역 희귀질환이다. 이 질환은 전신 근육의 변동적인 약화를 촉진하며 서있거나 삼키기, 숨쉬기 같은 일상 활동에도 영향을 미칠 수 있다고 알려진다.ADAPT로 명명된 임상3상에서 비브가트는 중증근무력증 일상생활 수행 능력 평가 척도인 ‘MG-ADL(Myasthenia Gravis-Activities of Daily Living)’ 기준 반응자 비율 68%를 기록하며 위약군 30% 대비 더 높았다. 비브가트 투여군은 정량적 중증근무력증(QMG) 척도 기준 반응자 비율에서도 위약군 대비 개선된 수치를 나타냈다.한독은 신약 도입을 통해 희귀질환 치료제 확보에 적극 나서고 있다. 2020년 12월 아스트라제네카가 알렉시온을 인수하면서 한독이 판매하던 솔리리스와 울토미리스 판권이 넘어가면서 희귀질환 영역에 공백이 생겼기 때문이다.한독은 2023년 미국 인사이트의 담관암 치료제 ‘페마자이레’와 미만성거대B세포림프종 치료제 ‘민쥬비’를 도입하며 국내 허가에도 성공했다.이어 한독은 지난해 4월 소비와 합작법인 '한독소비(Sobi-Handok)'를 공식 출범했다. 소비는 스웨덴에서 출범한 희귀질환 전문 글로벌 제약바이오 기업으로 혈액학, 면역학 치료 분야에서 혁신치료제를 제공하고 있다. 이후 한독은 면역성혈소판감소증 치료제 ‘도프텔렛’과 발작성혈색소뇨증 신약 ‘엠파벨리’를 국내 허가 받으며 희귀질환 파이프라인을 강화했다.한독은 소비의 희귀질환 파이프라인을 지속적으로 들여올 계획이다. 소비는 도프텔렛, 엠파벨리를 비롯해 혈우병 신약 '엘록타, 알프로릭스, 알투비오'와 원발성 혈구탐식성 림프조직구증 신약 '가미판트', 혈소판감소증 신약 '본조', 호흡기세포융합바이러스 치료제 '시나지스', 알캅톤뇨증 신약 '오르파딘', 항체약물접합체(ADC) '진론타', 류마티스관절염 신약 ‘키너렛’ 등을 보유하고 있다. 제일약품, 신약 도입…동아에스티 엑스코프리 허가 신청제일약품은 일본 시오노기의 신약을 통해 난치성 질환 시장에 도전장을 내밀었다. 최근 이 회사는 다제내성 그람음성균 감염 치료제 ‘페트로자’를 국내 허가받았다.시오노기가 개발한 페트로자는 사이드로포어 세팔로스포린 계열 항생제로, 철분과 결합한 후 박테리아의 자체 철분 포린 채널을 통해 세포 내부로 흡수되는 작용 기전을 갖고 있다.페트로자는 이번 국내 시판 허가에 앞서 미국, 유럽, 일본 등 전세계 10개국 이상에서 허가된 바 있다.제일약품은 지난 2022년에는 과민성방광 신약 ‘베오바’를 국내 도입했다. 해당 의약품은 방광의 베타-3(β-3) 교감신경 수용체에 선택적으로 작용해 방광 배뇨근을 이완시켜 빈뇨, 배뇨 절박감 등에 효과를 보이는 것으로 알려진다.제일약품은 국내 가교 임상3상을 통해 1,2차 평가변수로 설정한 1일 평균 배뇨횟수 변화량, 1일 평균 요절박 횟수, 절박성 요실금 횟수 등에서 위약 대비 유의한 효과를 보였다.제일약품은 페트로자, 베오바 이외에도 덱실란트, 액토스, 리피토, 리리카 등 도입신약을 통해 다양한 질환 시장 진출에 성공한 바 있다.보령은 도입신약을 통해 항암 파이프라인 확장에 나선다. 이 회사는 릴리로부터 도입한 항암제 젬자, 알림타 등을 도입했으며 소세포폐암 표적치료제 젭젤카도 스페인 파마마로부터 국내 판권을 확보한 바 있다.보령 도입신약 '젭젤카'젭젤카는 현재 백금 기반 화학요법 또는 그 이후에 질병 진행을 경험한 전이성 소세포폐암 환자의 치료를 위해 미국에서 허가됐다. 국내에선 2022년 9월 허가돼 지난해 3월 시장에 비급여 출시됐다.젭젤카는 이리노테칸 병용을 통해 소세포폐암 고위험 환자 특히 화학요법 치료 간격(CTFI)이 30일 이상인 환자에서 반응률을 나타냈다.또 젭젤카는 면역항암제 티쎈트릭과의 병용요법의 가능성도 확인 중이다. 최근 공개된 임상 결과에 따르면 젭젤카+티쎈트릭은 전체생존기간(OS)과 무진행생존기간(PFS) 등에서 단독요법과 비교했을 때 통계적으로 유의미한 개선을 보였다.젭젤카가 티쎈트릭과의 병용요법에서도 유효성을 확인하며 소세포폐암 치료제 시장에도 변화의 바람이 불어올 것으로 예측된다.비소세포폐암에는 다양한 표적치료제들이 등장해 생존율 개선에 성공했지만 환자 수가 적은 소세포폐암은 사실상 치료제 불모지나 다름 없었다. 면역항암제 티쎈트릭은 소세포폐암 환자의 생존기간을 2개월 연장시키는데 그쳤고 후발주자들은 제한적인 효과를 보였다.소세포폐암은 주로 폐 중심부 기도에서 처음 발병하며 진행 속도가 빠른 편에 속한다. 특히 전반적으로 악성도가 강해서 발견 당시에 이미 림프나 혈액의 순환을 통해 다른 장기나 반대편 폐, 혹은 종격동으로 전이돼 있는 경우가 대부분이다. 다만 치료옵션은 부족해 새로운 치료제에 대한 필요도가 높은 상황이다.소세포폐암의 생존율이 낮은 데는 치료제가 부족한 요인이 꼽힌다. 소세포폐암 치료에는 토포테칸, 벨로테칸, 이리노테칸과 같은 올드드럭들 외에 티쎈트릭 등 면역항암제 옵션이 등장했지만 생존율을 크게 개선하는 데는 실패했다.항암제부터 희귀질환 치료제까지2025-02-25 06:20:22손형민
제약업계, 도입신약 상업화 속도…미개척 시장 정조준[데일리팜=손형민 기자] 국내 제약바이오업계가 도입신약을 통해 미개척 시장 진출에 적극 나서고 있다. 최근 한독은 벨기에 아르젠엑스로부터 도입한 비브가트를 국내 허가받으며 중증근무력증 치료제를 확보했다. 이 회사는 아르젠엑스뿐만 아니라 미국 인사이트, 스웨덴 소비 등과의 협업을 통해 희귀질환 신약을 국내 도입하고 있다.도입신약은 수익성이 떨어지지만 암, 희귀질환 등 개척되지 않은 분야로 진출이 용이하다. 특히 국내 도입된 신약들은 글로벌 규제기관으로부터 효과를 인정받았기에 추가 임상이 필요하지 않다는 강점이 있다. 한독뿐만 아니라 제일약품, 보령 등 여러 국내사들이 글로벌 시장에서 검증된 신약 도입에 적극 나서고 있다.한독, 도입신약 적극 모색…솔리리스·울토미리스 공백 매우나25일 관련 업계에 따르면 식품의약품안전처는 최근 한독이 도입한 중증근무력증 치료제 ‘비브가트’를 허가 승인했다. 한독은 지난해 8월 비브가트 원 개발사인 아르젠엑스와 계약을 체결해 국내 허가 등록과 급여 진행, 독점 유통을 담당하게 됐다.비브가트는 면역글로불린G(IgG)의 방어수용체인 Fc 수용체(FcRn)를 차단하는 새로운 기전이다. 해당 기전은 질병을 유발하는 면역글로불린G 항체를 감소시키고 이를 재순환하는 과정을 차단한다. FcRn과 결합해 IgG 항체가 분해되지 않도록 하는 것이다. 비브가트는 현재 미국과 유럽, 영국, 이스라엘, 중국에서 전신 중증근무력증 성인 환자의 치료제로 승인된 바 있다.전신 중증근무력증은 신경이 근육에 신호를 전달하지 못해 골격근이 약화되는 만성 자가면역 희귀질환이다. 이 질환은 전신 근육의 변동적인 약화를 촉진하며 서있거나 삼키기, 숨쉬기 같은 일상 활동에도 영향을 미칠 수 있다고 알려진다.ADAPT로 명명된 임상3상에서 비브가트는 중증근무력증 일상생활 수행 능력 평가 척도인 ‘MG-ADL(Myasthenia Gravis-Activities of Daily Living)’ 기준 반응자 비율 68%를 기록하며 위약군 30% 대비 더 높았다. 비브가트 투여군은 정량적 중증근무력증(QMG) 척도 기준 반응자 비율에서도 위약군 대비 개선된 수치를 나타냈다.한독은 신약 도입을 통해 희귀질환 치료제 확보에 적극 나서고 있다. 2020년 12월 아스트라제네카가 알렉시온을 인수하면서 한독이 판매하던 솔리리스와 울토미리스 판권이 넘어가면서 희귀질환 영역에 공백이 생겼기 때문이다.한독은 2023년 미국 인사이트의 담관암 치료제 ‘페마자이레’와 미만성거대B세포림프종 치료제 ‘민쥬비’를 도입하며 국내 허가에도 성공했다.이어 한독은 지난해 4월 소비와 합작법인 '한독소비(Sobi-Handok)'를 공식 출범했다. 소비는 스웨덴에서 출범한 희귀질환 전문 글로벌 제약바이오 기업으로 혈액학, 면역학 치료 분야에서 혁신치료제를 제공하고 있다. 이후 한독은 면역성혈소판감소증 치료제 ‘도프텔렛’과 발작성혈색소뇨증 신약 ‘엠파벨리’를 국내 허가 받으며 희귀질환 파이프라인을 강화했다.한독은 소비의 희귀질환 파이프라인을 지속적으로 들여올 계획이다. 소비는 도프텔렛, 엠파벨리를 비롯해 혈우병 신약 '엘록타, 알프로릭스, 알투비오'와 원발성 혈구탐식성 림프조직구증 신약 '가미판트', 혈소판감소증 신약 '본조', 호흡기세포융합바이러스 치료제 '시나지스', 알캅톤뇨증 신약 '오르파딘', 항체약물접합체(ADC) '진론타', 류마티스관절염 신약 ‘키너렛’ 등을 보유하고 있다. 제일약품, 신약 도입…동아에스티 엑스코프리 허가 신청제일약품은 일본 시오노기의 신약을 통해 난치성 질환 시장에 도전장을 내밀었다. 최근 이 회사는 다제내성 그람음성균 감염 치료제 ‘페트로자’를 국내 허가받았다.시오노기가 개발한 페트로자는 사이드로포어 세팔로스포린 계열 항생제로, 철분과 결합한 후 박테리아의 자체 철분 포린 채널을 통해 세포 내부로 흡수되는 작용 기전을 갖고 있다.페트로자는 이번 국내 시판 허가에 앞서 미국, 유럽, 일본 등 전세계 10개국 이상에서 허가된 바 있다.제일약품은 지난 2022년에는 과민성방광 신약 ‘베오바’를 국내 도입했다. 해당 의약품은 방광의 베타-3(β-3) 교감신경 수용체에 선택적으로 작용해 방광 배뇨근을 이완시켜 빈뇨, 배뇨 절박감 등에 효과를 보이는 것으로 알려진다.제일약품은 국내 가교 임상3상을 통해 1,2차 평가변수로 설정한 1일 평균 배뇨횟수 변화량, 1일 평균 요절박 횟수, 절박성 요실금 횟수 등에서 위약 대비 유의한 효과를 보였다.제일약품은 페트로자, 베오바 이외에도 덱실란트, 액토스, 리피토, 리리카 등 도입신약을 통해 다양한 질환 시장 진출에 성공한 바 있다.보령은 도입신약을 통해 항암 파이프라인 확장에 나선다. 이 회사는 릴리로부터 도입한 항암제 젬자, 알림타 등을 도입했으며 소세포폐암 표적치료제 젭젤카도 스페인 파마마로부터 국내 판권을 확보한 바 있다.보령 도입신약 '젭젤카'젭젤카는 현재 백금 기반 화학요법 또는 그 이후에 질병 진행을 경험한 전이성 소세포폐암 환자의 치료를 위해 미국에서 허가됐다. 국내에선 2022년 9월 허가돼 지난해 3월 시장에 비급여 출시됐다.젭젤카는 이리노테칸 병용을 통해 소세포폐암 고위험 환자 특히 화학요법 치료 간격(CTFI)이 30일 이상인 환자에서 반응률을 나타냈다.또 젭젤카는 면역항암제 티쎈트릭과의 병용요법의 가능성도 확인 중이다. 최근 공개된 임상 결과에 따르면 젭젤카+티쎈트릭은 전체생존기간(OS)과 무진행생존기간(PFS) 등에서 단독요법과 비교했을 때 통계적으로 유의미한 개선을 보였다.젭젤카가 티쎈트릭과의 병용요법에서도 유효성을 확인하며 소세포폐암 치료제 시장에도 변화의 바람이 불어올 것으로 예측된다.비소세포폐암에는 다양한 표적치료제들이 등장해 생존율 개선에 성공했지만 환자 수가 적은 소세포폐암은 사실상 치료제 불모지나 다름 없었다. 면역항암제 티쎈트릭은 소세포폐암 환자의 생존기간을 2개월 연장시키는데 그쳤고 후발주자들은 제한적인 효과를 보였다.소세포폐암은 주로 폐 중심부 기도에서 처음 발병하며 진행 속도가 빠른 편에 속한다. 특히 전반적으로 악성도가 강해서 발견 당시에 이미 림프나 혈액의 순환을 통해 다른 장기나 반대편 폐, 혹은 종격동으로 전이돼 있는 경우가 대부분이다. 다만 치료옵션은 부족해 새로운 치료제에 대한 필요도가 높은 상황이다.소세포폐암의 생존율이 낮은 데는 치료제가 부족한 요인이 꼽힌다. 소세포폐암 치료에는 토포테칸, 벨로테칸, 이리노테칸과 같은 올드드럭들 외에 티쎈트릭 등 면역항암제 옵션이 등장했지만 생존율을 크게 개선하는 데는 실패했다.항암제부터 희귀질환 치료제까지2025-02-25 06:20:22손형민 -
 유럽 직판, 미국 우회...삼성 솔리리스 시밀러 맞춤전략[데일리팜=차지현 기자] 삼성바이오에피스가 다국적 제약사 테바 파마슈티컬 인더스트리와 희귀질환 치료제 바이오시밀러의 미국 상업화 파트너십을 체결했다. 삼성바이오에피스는 테바를 통해 해당 바이오시밀러를 올 상반기 미국 시장에 출시할 예정이다.직접 판매에 나섰던 유럽과 달리 미국에서는 파트너사를 활용한 우회 진출 전략을 택했다는 점이 눈에 띈다. 미국 의약품 시장이 민간 보험 중심 복잡한 구조인 데다 직판에 따른 비용 부담 등을 고려한 결정이라는 분석이 나온다.삼성바이오에피스, 테바와 에피스클리 상업화 파트너십…상반기 미국 출시삼성바이오에피스 희귀질환 치료제 '에피스클리'(자료: 삼성바이오에피스) 13일 바이오 업계에 따르면 삼성바이오에피스는 최근 테바와 희귀질환 치료제 '솔리리스'(성분명 에쿨리주맙) 바이오시밀러 '에피스클리'의 미국 시장 진출을 위한 상업화 파트너십 계약을 체결했다.솔리리스는 미국 희귀질환 치료제 전문 개발사 알렉시온이 개발한 의약품이다. 2007년 3월 미국 식품의약국(FDA), 같은 해 6월 유럽연합 집행위원회(EC)로부터 품목허가를 획득했다. 이후 2021년 아스트라제네카가 알렉시온을 인수하면서 솔리리스 판권도 넘겨받았다.솔리리스 적응증은 발작성 야간 혈색소뇨증(PNH), 비정형 용혈성 요독 증후군(aHUS), 시신경 척수염 범주 질환(NMOSD) 중증근무력증(gMG) 등 희귀질환이다. 솔리리스는 2023년 전 세계 매출 31억4500만달러(약 4조원)을 기록했다. 이 가운데 미국 시장이 약 2조3000억원, 유럽 시장이 약 1조원 규모로 추산된다.에피스클리는 삼성바이오에피스가 개발한 첫 혈액학 분야 바이오시밀러다. 삼성바이오에피스는 2023년 5월 PNH를 적응증으로 에피스클리 EC 품목허가를 획득, 같은 해 7월 유럽 시장에 출시했다. 국내에서도 지난해 1월 식품의약품안전처 허가를 받은 뒤 시판 중이다. 미국의 경우 지난해 7월 FDA가 PNH와 aHUS를 적응증으로 에피스클리 품목허가를 승인했다. 지난해 11월에는 FDA로부터 gMG 적응증을 추가로 승인받았다.이번 계약에 따라 삼성바이오에피스는 테바를 통해 에피스클리를 미국 시장에 출시할 계획이다. 출시 예상 시점은 올 상반기다. 삼성바이오에피스는 에피스클리의 생산과 공급을 담당한다. 테바는 미국 내 마케팅과 영업 활동을 맡을 예정이다.이번 계약 이후 삼성바이오에피스의 해외 파트너사는 총 4곳으로 늘어난다. 삼성바이오에피스는 현재 해외 시장에서 바이오젠, 오가논, 산도스와 상업화 관련 파트너십을 맺고 있다. 파트너사가 대상 지역 내에서 계약된 제품에 대해 독점적 판매권을 갖고 계약에 따른 마일스톤과 판매 수수료 로열티를 삼성바이오에피스에 지급하는 구조다.직판 유럽과 달리 미국은 파트너십 활용, 미국 의약품 구조·비용 등 고려에피스클리는 제품명에 회사 사명이 들어간 유일한 제품이자 삼성바이오에피스의 첫 직판 제품이다. 에피스클리 적응증인 PNH와 aHUS는 희귀질환 중에서도 환자 수가 매우 적은 초희귀질환에 속한다. 삼성바이오에피스는 적은 수의 영업사원으로도 충분히 영업 활동이 가능하다고 판단, 보유 제품 중 처음으로 직판 체제를 구축하기로 했다.파트너사를 통해 유통하지 않고 직판을 하면 수수료 지출이 줄어 수익성을 높일 수 있다. 해외 진출 시 국내 기업이 협력사에 지불하는 수수료는 평균 매출의 30~40%로 알려진다. 시장 통제력을 강화할 수 있다는 점도 장점이다.유럽 시장에서 직판 효과는 조금씩 가시화하고 있다. 지난해 3분기 기준 에피스클리는 독일과 이탈리아 지역에서 에쿨리주맙 성분 바이오시밀러 시장 점유율 1위를 차지했다. 프랑스 최대 구매조합(UniHA), 네덜란드 주정부 입찰도 수주했다.삼성바이오에피스 희귀질환 치료제 '에피스클리' 해외 진출 현황(자료: 삼성바이오에피스) 그럼에도 삼성바이오에피스가 미국에서 에피스클리를 직판하지 않기로 결정한 이유는 미국의 복잡한 의약품 구조와 초기 직판에 드는 비용 등을 고려한 결과로 풀이된다. 유럽 의약품 시장은 텐더(입찰) 방식이라 비교적 진입이 쉽다. 반면 미국 의약품 시장은 민간 보험 중심의 복잡한 구조이기 때문에 직판에 나서기 쉽지 않았을 것이라는 분석이다.초기 직판 체제를 구축하는 데 드는 비용도 부담으로 작용했을 것으로 보인다. 직판 체제는 판매하는 제품이 많을수록 수익성이 증가하는 구조지만 초기에는 현지 법인을 세우고 전문 영업·마케팅 인력을 채용하기 위해 막대한 고정비를 부담해야 한다.연간 4억 오리지널 대비 저렴한 약가·제품 경쟁력 앞세워 미국 공략 속도삼성바이오에피스는 에피스클리의 가격 경쟁력과 제품 경쟁력을 앞세워 미국 시장 공략에 속도를 낸다는 목표다.솔리리스는 연간 약값이 약 4억원에 달하는 초고가 의약품이다. 에피스클리의 국내 약값은 바이알(병)당 251만원으로 책정됐다. 기존 오리지널 의약품 가격 513만원의 절반 수준이다. 이는 지난해 4월부터 새롭게 적용된 솔리리스 약값 360만원에 비해서도 약 30% 낮은 금액이다. 가격 경쟁력으로 오리지널 대비 우위에 서는 동시에 환자 접근성을 확대하겠다는 구상이다.'솔비톨 프리'도 에피스클리의 경쟁력으로 꼽힌다. 솔비톨은 의약품 안정성 제고에 도움을 주는 물질이다. 하지만 하지만 과당이나 설탕 등 과당 전구물질을 소화할 수 없는 과당 불내증 환자에게 거부 반응을 일으킬 우려가 있다. 유럽에서는 과당 불내증 환자에게 솔비톨을 포함한 의약품 투여를 금지하고 있다.미국은 솔비톨 관련 투여를 금지하는 조항은 없다. 다만 솔비톨이 일부 환자군에 거부 반응을 일으킬 우려가 있는 만큼 의료 현장에서 솔비톨이 없는 제품을 선호할 가능성이 크다는 게 업계 전문가들의 시각이다. 에피스클리의 경쟁 약물인 암젠의 솔리리스 바이오시밀러 '비켐브'에는 솔비톨이 포함돼 있다.원개발사의 특허 방어 전략은 변수다. 알렉시온은 솔리리스의 투여 편의성을 개선, 8주에 한 번 투여하는 '울토미리스'를 판매 중이다. 솔리리스와 바이오시밀러 제품은 2주마다 정맥주사로 투여하는 방식이다. 이와 관련 삼성바이오에피스 측은 의료 현장에서 여전히 솔리리스 처방 수요가 존재하는 데다 울토미리스가 진입하지 못한 시장도 많은 만큼 시장성이 충분하다고 보고 있다.삼성바이오에피스 관계자는 "테바는 미국 시장에서 폭 넓은 영업과 마케팅 인프라를 지닌 제네릭·바이오시밀러 업체"라며 "미국 시장에서 상업화 경험과 전문성을 보유하고 있기 때문에 이번 에피스클리 미국 시장 상업화 파트너사로 선정하게 됐다"고 했다.이어 이 관계자는 "솔리리스 시장 규모는 유럽보다 미국이 훨씬 크다"면서 "유럽 시장에서 에피스클리가 선전을 하고 있기 때문에 앞으로 미국 시장에서 에피스클리 성과가 더욱 기대된다"고 했다.2025-01-13 06:19:36차지현
유럽 직판, 미국 우회...삼성 솔리리스 시밀러 맞춤전략[데일리팜=차지현 기자] 삼성바이오에피스가 다국적 제약사 테바 파마슈티컬 인더스트리와 희귀질환 치료제 바이오시밀러의 미국 상업화 파트너십을 체결했다. 삼성바이오에피스는 테바를 통해 해당 바이오시밀러를 올 상반기 미국 시장에 출시할 예정이다.직접 판매에 나섰던 유럽과 달리 미국에서는 파트너사를 활용한 우회 진출 전략을 택했다는 점이 눈에 띈다. 미국 의약품 시장이 민간 보험 중심 복잡한 구조인 데다 직판에 따른 비용 부담 등을 고려한 결정이라는 분석이 나온다.삼성바이오에피스, 테바와 에피스클리 상업화 파트너십…상반기 미국 출시삼성바이오에피스 희귀질환 치료제 '에피스클리'(자료: 삼성바이오에피스) 13일 바이오 업계에 따르면 삼성바이오에피스는 최근 테바와 희귀질환 치료제 '솔리리스'(성분명 에쿨리주맙) 바이오시밀러 '에피스클리'의 미국 시장 진출을 위한 상업화 파트너십 계약을 체결했다.솔리리스는 미국 희귀질환 치료제 전문 개발사 알렉시온이 개발한 의약품이다. 2007년 3월 미국 식품의약국(FDA), 같은 해 6월 유럽연합 집행위원회(EC)로부터 품목허가를 획득했다. 이후 2021년 아스트라제네카가 알렉시온을 인수하면서 솔리리스 판권도 넘겨받았다.솔리리스 적응증은 발작성 야간 혈색소뇨증(PNH), 비정형 용혈성 요독 증후군(aHUS), 시신경 척수염 범주 질환(NMOSD) 중증근무력증(gMG) 등 희귀질환이다. 솔리리스는 2023년 전 세계 매출 31억4500만달러(약 4조원)을 기록했다. 이 가운데 미국 시장이 약 2조3000억원, 유럽 시장이 약 1조원 규모로 추산된다.에피스클리는 삼성바이오에피스가 개발한 첫 혈액학 분야 바이오시밀러다. 삼성바이오에피스는 2023년 5월 PNH를 적응증으로 에피스클리 EC 품목허가를 획득, 같은 해 7월 유럽 시장에 출시했다. 국내에서도 지난해 1월 식품의약품안전처 허가를 받은 뒤 시판 중이다. 미국의 경우 지난해 7월 FDA가 PNH와 aHUS를 적응증으로 에피스클리 품목허가를 승인했다. 지난해 11월에는 FDA로부터 gMG 적응증을 추가로 승인받았다.이번 계약에 따라 삼성바이오에피스는 테바를 통해 에피스클리를 미국 시장에 출시할 계획이다. 출시 예상 시점은 올 상반기다. 삼성바이오에피스는 에피스클리의 생산과 공급을 담당한다. 테바는 미국 내 마케팅과 영업 활동을 맡을 예정이다.이번 계약 이후 삼성바이오에피스의 해외 파트너사는 총 4곳으로 늘어난다. 삼성바이오에피스는 현재 해외 시장에서 바이오젠, 오가논, 산도스와 상업화 관련 파트너십을 맺고 있다. 파트너사가 대상 지역 내에서 계약된 제품에 대해 독점적 판매권을 갖고 계약에 따른 마일스톤과 판매 수수료 로열티를 삼성바이오에피스에 지급하는 구조다.직판 유럽과 달리 미국은 파트너십 활용, 미국 의약품 구조·비용 등 고려에피스클리는 제품명에 회사 사명이 들어간 유일한 제품이자 삼성바이오에피스의 첫 직판 제품이다. 에피스클리 적응증인 PNH와 aHUS는 희귀질환 중에서도 환자 수가 매우 적은 초희귀질환에 속한다. 삼성바이오에피스는 적은 수의 영업사원으로도 충분히 영업 활동이 가능하다고 판단, 보유 제품 중 처음으로 직판 체제를 구축하기로 했다.파트너사를 통해 유통하지 않고 직판을 하면 수수료 지출이 줄어 수익성을 높일 수 있다. 해외 진출 시 국내 기업이 협력사에 지불하는 수수료는 평균 매출의 30~40%로 알려진다. 시장 통제력을 강화할 수 있다는 점도 장점이다.유럽 시장에서 직판 효과는 조금씩 가시화하고 있다. 지난해 3분기 기준 에피스클리는 독일과 이탈리아 지역에서 에쿨리주맙 성분 바이오시밀러 시장 점유율 1위를 차지했다. 프랑스 최대 구매조합(UniHA), 네덜란드 주정부 입찰도 수주했다.삼성바이오에피스 희귀질환 치료제 '에피스클리' 해외 진출 현황(자료: 삼성바이오에피스) 그럼에도 삼성바이오에피스가 미국에서 에피스클리를 직판하지 않기로 결정한 이유는 미국의 복잡한 의약품 구조와 초기 직판에 드는 비용 등을 고려한 결과로 풀이된다. 유럽 의약품 시장은 텐더(입찰) 방식이라 비교적 진입이 쉽다. 반면 미국 의약품 시장은 민간 보험 중심의 복잡한 구조이기 때문에 직판에 나서기 쉽지 않았을 것이라는 분석이다.초기 직판 체제를 구축하는 데 드는 비용도 부담으로 작용했을 것으로 보인다. 직판 체제는 판매하는 제품이 많을수록 수익성이 증가하는 구조지만 초기에는 현지 법인을 세우고 전문 영업·마케팅 인력을 채용하기 위해 막대한 고정비를 부담해야 한다.연간 4억 오리지널 대비 저렴한 약가·제품 경쟁력 앞세워 미국 공략 속도삼성바이오에피스는 에피스클리의 가격 경쟁력과 제품 경쟁력을 앞세워 미국 시장 공략에 속도를 낸다는 목표다.솔리리스는 연간 약값이 약 4억원에 달하는 초고가 의약품이다. 에피스클리의 국내 약값은 바이알(병)당 251만원으로 책정됐다. 기존 오리지널 의약품 가격 513만원의 절반 수준이다. 이는 지난해 4월부터 새롭게 적용된 솔리리스 약값 360만원에 비해서도 약 30% 낮은 금액이다. 가격 경쟁력으로 오리지널 대비 우위에 서는 동시에 환자 접근성을 확대하겠다는 구상이다.'솔비톨 프리'도 에피스클리의 경쟁력으로 꼽힌다. 솔비톨은 의약품 안정성 제고에 도움을 주는 물질이다. 하지만 하지만 과당이나 설탕 등 과당 전구물질을 소화할 수 없는 과당 불내증 환자에게 거부 반응을 일으킬 우려가 있다. 유럽에서는 과당 불내증 환자에게 솔비톨을 포함한 의약품 투여를 금지하고 있다.미국은 솔비톨 관련 투여를 금지하는 조항은 없다. 다만 솔비톨이 일부 환자군에 거부 반응을 일으킬 우려가 있는 만큼 의료 현장에서 솔비톨이 없는 제품을 선호할 가능성이 크다는 게 업계 전문가들의 시각이다. 에피스클리의 경쟁 약물인 암젠의 솔리리스 바이오시밀러 '비켐브'에는 솔비톨이 포함돼 있다.원개발사의 특허 방어 전략은 변수다. 알렉시온은 솔리리스의 투여 편의성을 개선, 8주에 한 번 투여하는 '울토미리스'를 판매 중이다. 솔리리스와 바이오시밀러 제품은 2주마다 정맥주사로 투여하는 방식이다. 이와 관련 삼성바이오에피스 측은 의료 현장에서 여전히 솔리리스 처방 수요가 존재하는 데다 울토미리스가 진입하지 못한 시장도 많은 만큼 시장성이 충분하다고 보고 있다.삼성바이오에피스 관계자는 "테바는 미국 시장에서 폭 넓은 영업과 마케팅 인프라를 지닌 제네릭·바이오시밀러 업체"라며 "미국 시장에서 상업화 경험과 전문성을 보유하고 있기 때문에 이번 에피스클리 미국 시장 상업화 파트너사로 선정하게 됐다"고 했다.이어 이 관계자는 "솔리리스 시장 규모는 유럽보다 미국이 훨씬 크다"면서 "유럽 시장에서 에피스클리가 선전을 하고 있기 때문에 앞으로 미국 시장에서 에피스클리 성과가 더욱 기대된다"고 했다.2025-01-13 06:19:36차지현 -
 울토미리스, 요독증후군 급여 적용…"치료접근성 개선"김진석 세브란스병원 혈액내과 교수 [데일리팜=손형민 기자] 울토미리스가 비정형 용혈성 요독증후군(aHUS)에 1월부터 본격 급여 적용됐다. 전문가들은 울토미리스의 급여를 환영하면서도, 사전심의를 거쳐야하는 등 까다로운 급여조건에 대한 제도적인 개선이 필요하다는 의견을 제기하고 있다.10일 한국아스트라제네카는 JW매리어트 동대문스퀘어 서울에서 울토미리스의 aHUS 국내 보험급여 적용을 기념하는 기자간담회를 개최했다.이달부터 울토미리스는 혈전성 미세혈관병증(TMA)과 신장 손상을 동반한 aHUS 환자에서 건강보험급여를 적용 받는다. 이를 통해 증상이 급격히 악화돼 말기 신장 질환(ESRD)으로 이어질 수 있는 aHUS 환자들의 치료 접근성이 개선될 것으로 기대되고 있다.울토미리스는 솔리리스 대비 반감기를 약 4배 연장한 차세대 C5 보체 억제제다. 솔리리스는 2주 간격으로 투여가 필요한 반면, 울토미리스는 8주로 투여 간격을 늘려 치료 편의성이 개선됐다.세균 표피에서 보체 5번이 활성화되면 세포막 공격 복합체가 생성돼 세포막에 구멍이 생기게 된다. 정상적인 면역쳬계인 보체 활성화 과정이 계속되게 되면 혈관내피세포에 문제가 생겨 관련 질환이 발생하게 된다. 울토미리스는 이를 억제하는 기전을 갖고 있다.aHUS는 면역 시스템의 보체가 유전적 결함으로 인해 과활성화되며 혈전성 미세혈관병증을 유발하는 급성 희귀질환이다. 이로 인해 여러 장기 특히 신장에 심각한 손상을 초래할 수 있다. aHUS는 용혈 요독증후군이 대장균과 관련 없이 발생하는 경우를 가리킨다.울토미리스는 보체 억제제 치료 경험이 없는 성인 환자를 대상으로 한 임상 3상 Study 311 연구에서 효능과 안전성이 확인됐다.임상 결과, 울토미리스는 치료 26주 차에 환자 53.6%에서 혈소판, LDH 수치 등 TMA 관련 지표의 개선이 확인됐다. 또 이 치료제는 혈청 free C5 농도를 0.5 μg/ml 미만으로 유지해 지속적인 말단 보체 억제 효과를 확인했다. 소아 환자를 대상으로 한 임상3상 Study 312 연구에서도 울토미리스는 치료 50주 차에 94.4%의 환자에서 TMA가 완전히 사라지는 결과를 보였다.김진석 세브란스병원 혈액내과 교수는 “솔리리스에서 울토미리스로 전환한 소아 aHUS 환자를 대상으로 한 연구에서도 1년간 신장, 혈액학적 지표가 안정적으로 유지돼 약제 전환의 유효성이 확인됐다. 새로운 치료 옵션인 울토미리스의 도입으로 의료진으로서 환자들에게 희망을 줄 수 있어 기쁘다”라고 강조했다.현재 aHUS에는 울토미리스와 솔리리스가 사용이 가능하지만, 두 약제 모두 사전심의제도를 통해 승인된 환자들만 사용이 가능하다. 적절한 투약시기를 놓쳐 환자의 상태가 악화될 수 있는 만큼, 의료진들은 사후심사로 전환하는 등 급여 조건 개선이 필요하다는 의견이 제기되고 있다.aHUS의 급여적용은 2018년 솔리리스의 등장으로 시행됐다. 다만 2018년 7월부터 지난해 10월까지 사전심의제도 결과를 분석한 결과, 321건 중 56건이 승인돼 평균 18% 승인율을 보이고 있다.김 교수는 “울토미리스가 급여적용됐지만, 솔리리스와 마찬가지로 치료제 사용을 위해 사전심의를 거쳐야 하는 제약이 있다. aHUS 환자들이 적시에 치료를 받을 수 있도록 제도적인 개선이 같이 수반됐으면 한다”라고 피력했다.2025-01-10 12:00:55손형민
울토미리스, 요독증후군 급여 적용…"치료접근성 개선"김진석 세브란스병원 혈액내과 교수 [데일리팜=손형민 기자] 울토미리스가 비정형 용혈성 요독증후군(aHUS)에 1월부터 본격 급여 적용됐다. 전문가들은 울토미리스의 급여를 환영하면서도, 사전심의를 거쳐야하는 등 까다로운 급여조건에 대한 제도적인 개선이 필요하다는 의견을 제기하고 있다.10일 한국아스트라제네카는 JW매리어트 동대문스퀘어 서울에서 울토미리스의 aHUS 국내 보험급여 적용을 기념하는 기자간담회를 개최했다.이달부터 울토미리스는 혈전성 미세혈관병증(TMA)과 신장 손상을 동반한 aHUS 환자에서 건강보험급여를 적용 받는다. 이를 통해 증상이 급격히 악화돼 말기 신장 질환(ESRD)으로 이어질 수 있는 aHUS 환자들의 치료 접근성이 개선될 것으로 기대되고 있다.울토미리스는 솔리리스 대비 반감기를 약 4배 연장한 차세대 C5 보체 억제제다. 솔리리스는 2주 간격으로 투여가 필요한 반면, 울토미리스는 8주로 투여 간격을 늘려 치료 편의성이 개선됐다.세균 표피에서 보체 5번이 활성화되면 세포막 공격 복합체가 생성돼 세포막에 구멍이 생기게 된다. 정상적인 면역쳬계인 보체 활성화 과정이 계속되게 되면 혈관내피세포에 문제가 생겨 관련 질환이 발생하게 된다. 울토미리스는 이를 억제하는 기전을 갖고 있다.aHUS는 면역 시스템의 보체가 유전적 결함으로 인해 과활성화되며 혈전성 미세혈관병증을 유발하는 급성 희귀질환이다. 이로 인해 여러 장기 특히 신장에 심각한 손상을 초래할 수 있다. aHUS는 용혈 요독증후군이 대장균과 관련 없이 발생하는 경우를 가리킨다.울토미리스는 보체 억제제 치료 경험이 없는 성인 환자를 대상으로 한 임상 3상 Study 311 연구에서 효능과 안전성이 확인됐다.임상 결과, 울토미리스는 치료 26주 차에 환자 53.6%에서 혈소판, LDH 수치 등 TMA 관련 지표의 개선이 확인됐다. 또 이 치료제는 혈청 free C5 농도를 0.5 μg/ml 미만으로 유지해 지속적인 말단 보체 억제 효과를 확인했다. 소아 환자를 대상으로 한 임상3상 Study 312 연구에서도 울토미리스는 치료 50주 차에 94.4%의 환자에서 TMA가 완전히 사라지는 결과를 보였다.김진석 세브란스병원 혈액내과 교수는 “솔리리스에서 울토미리스로 전환한 소아 aHUS 환자를 대상으로 한 연구에서도 1년간 신장, 혈액학적 지표가 안정적으로 유지돼 약제 전환의 유효성이 확인됐다. 새로운 치료 옵션인 울토미리스의 도입으로 의료진으로서 환자들에게 희망을 줄 수 있어 기쁘다”라고 강조했다.현재 aHUS에는 울토미리스와 솔리리스가 사용이 가능하지만, 두 약제 모두 사전심의제도를 통해 승인된 환자들만 사용이 가능하다. 적절한 투약시기를 놓쳐 환자의 상태가 악화될 수 있는 만큼, 의료진들은 사후심사로 전환하는 등 급여 조건 개선이 필요하다는 의견이 제기되고 있다.aHUS의 급여적용은 2018년 솔리리스의 등장으로 시행됐다. 다만 2018년 7월부터 지난해 10월까지 사전심의제도 결과를 분석한 결과, 321건 중 56건이 승인돼 평균 18% 승인율을 보이고 있다.김 교수는 “울토미리스가 급여적용됐지만, 솔리리스와 마찬가지로 치료제 사용을 위해 사전심의를 거쳐야 하는 제약이 있다. aHUS 환자들이 적시에 치료를 받을 수 있도록 제도적인 개선이 같이 수반됐으면 한다”라고 피력했다.2025-01-10 12:00:55손형민 -
 경구제 '파발타', 또 하나의 PNH 치료옵션으로 부상[데일리팜=어윤호 기자] 또 하나의 PNH 치료옵션이 탄생할 수 있을지 귀추가 주목된다.관련 업계에 따르면 한국노바티스는 경구용 발작성혈색소뇨증(PNH, Paroxysmal Nocturnal Hemoglobinuria)치료제 '파발타(입타코판)'의 보험급여 등재 신청을 제출, 절차를 진행중이다.PNH는 전 세계적으로 100만명 당 약 1.5명 정도가 발생하는 것으로 추정되는 희귀질환이다.이 질환의 치료는 그간 C5억제제에 의존했다. 2010년 '솔리리스(에쿨리주맙)'가 국내 처음 허가됐고, 2022년 '울토미리스(라불리주맙)'가 허가돼 PNH 치료에 사용돼 왔다. 두 치료옵션 모두 체내 면역에 관여하는 보체 시스템의 대체 경로 안에서 말단에 위치한 C5를 억제하는 기전인 C5 억제제이며 정맥주사제다.그러다 지난해 4월, C3 및 C3b에 결합해 보체연쇄반응을 억제하는 기전의 피하주사제 '엠파벨리(페그세타코플란)'가 허가됐고, 8월에는 B인자를 억제하는 기전의 경구제 파발타가 등장했다.C5 억제제의 기전적 한계로 남은 PNH 미충족 수요, ‘혈관 외 용혈(EVH)’ PNH는 적혈구에 유전적 결핍이 생기면서 시작되는데 이로 인해 혈관 내 용혈(IVH, Intravascular Hemolysis)과 혈관 외 용혈(EVH, Extravascular Hemolysis)이 발생한다.이런 용혈은 곧 혈전증, 골수부전을 야기해 생명을 위태롭게 만든다. 때문에 PNH 치료는 용혈을 조절하는 것이 중요한데 현재 PNH의 표준치료법인 C5 억제제는 IVH는 유의하게 조절하지만, 기전적으로 EVH는 조절하는데 한계가 있다.B인자억제제 파발타의 급여 등재에 관심이 모이는 이유다. B인자는 C5 뿐만 아니라 C3 및 C3b보다 대체 경로 내 상위에 존재하는 인자로 이를 억제할 경우 IVH 뿐만 아니라 EVH까지도 포괄적으로 조절할 수 있다.실제로 파발타는 치료 경험이 없는 환자 대상에게 유효성을 보였다. 치료 경험이 없는 PNH 환자를 대상으로 한 APPOINT-PNH 연구에 따르면 환자 33명 중 19명은 적혈구 수혈 없이 헤모글로빈 수치가 12g/dL 이상에 도달했다.또한 92% 환자가 임상적으로 유의한 헤모글로빈 수 2g/dL 이상 증가를 보였으며, 수혈 없이 헤모글로빈 수치가 12g/dL 이상 지속된 환자는 63%였다. 연구 기간인 24주동안 헤모글로빈 수치가 지속적으로 증가하는 추세를 보였으며, 20주차부터는 헤모글로빈 정상화 수치에 도달해 24주 차까지 지속됐다. 또한 98%가 수혈 의존성을 극복했다.장준호 삼성서울병원 혈액내과 교수는 "C5 억제제가 처음 등장했을 당시, 전문가들은 PNH 치료의 패러다임이 전환됐다고 평했다. 그러나 C5 억제제는 여전히 혈관 외 용혈(EVH)을 조절하는데 한계가 있다"고 말했다.아울러 "파발타는 PNH 치료의 또 한번의 패러다임 전환을 주도할 신약이다. B인자 억제라는 기전은 대체 경로의 상단에 위치한 B인자에 관여하기 때문에 혈관 내외 용혈을 모두 조절할 수 있으며 임상을 통해 고무적인 결과를 보였다"고 강조했다.2025-01-03 06:00:01어윤호
경구제 '파발타', 또 하나의 PNH 치료옵션으로 부상[데일리팜=어윤호 기자] 또 하나의 PNH 치료옵션이 탄생할 수 있을지 귀추가 주목된다.관련 업계에 따르면 한국노바티스는 경구용 발작성혈색소뇨증(PNH, Paroxysmal Nocturnal Hemoglobinuria)치료제 '파발타(입타코판)'의 보험급여 등재 신청을 제출, 절차를 진행중이다.PNH는 전 세계적으로 100만명 당 약 1.5명 정도가 발생하는 것으로 추정되는 희귀질환이다.이 질환의 치료는 그간 C5억제제에 의존했다. 2010년 '솔리리스(에쿨리주맙)'가 국내 처음 허가됐고, 2022년 '울토미리스(라불리주맙)'가 허가돼 PNH 치료에 사용돼 왔다. 두 치료옵션 모두 체내 면역에 관여하는 보체 시스템의 대체 경로 안에서 말단에 위치한 C5를 억제하는 기전인 C5 억제제이며 정맥주사제다.그러다 지난해 4월, C3 및 C3b에 결합해 보체연쇄반응을 억제하는 기전의 피하주사제 '엠파벨리(페그세타코플란)'가 허가됐고, 8월에는 B인자를 억제하는 기전의 경구제 파발타가 등장했다.C5 억제제의 기전적 한계로 남은 PNH 미충족 수요, ‘혈관 외 용혈(EVH)’ PNH는 적혈구에 유전적 결핍이 생기면서 시작되는데 이로 인해 혈관 내 용혈(IVH, Intravascular Hemolysis)과 혈관 외 용혈(EVH, Extravascular Hemolysis)이 발생한다.이런 용혈은 곧 혈전증, 골수부전을 야기해 생명을 위태롭게 만든다. 때문에 PNH 치료는 용혈을 조절하는 것이 중요한데 현재 PNH의 표준치료법인 C5 억제제는 IVH는 유의하게 조절하지만, 기전적으로 EVH는 조절하는데 한계가 있다.B인자억제제 파발타의 급여 등재에 관심이 모이는 이유다. B인자는 C5 뿐만 아니라 C3 및 C3b보다 대체 경로 내 상위에 존재하는 인자로 이를 억제할 경우 IVH 뿐만 아니라 EVH까지도 포괄적으로 조절할 수 있다.실제로 파발타는 치료 경험이 없는 환자 대상에게 유효성을 보였다. 치료 경험이 없는 PNH 환자를 대상으로 한 APPOINT-PNH 연구에 따르면 환자 33명 중 19명은 적혈구 수혈 없이 헤모글로빈 수치가 12g/dL 이상에 도달했다.또한 92% 환자가 임상적으로 유의한 헤모글로빈 수 2g/dL 이상 증가를 보였으며, 수혈 없이 헤모글로빈 수치가 12g/dL 이상 지속된 환자는 63%였다. 연구 기간인 24주동안 헤모글로빈 수치가 지속적으로 증가하는 추세를 보였으며, 20주차부터는 헤모글로빈 정상화 수치에 도달해 24주 차까지 지속됐다. 또한 98%가 수혈 의존성을 극복했다.장준호 삼성서울병원 혈액내과 교수는 "C5 억제제가 처음 등장했을 당시, 전문가들은 PNH 치료의 패러다임이 전환됐다고 평했다. 그러나 C5 억제제는 여전히 혈관 외 용혈(EVH)을 조절하는데 한계가 있다"고 말했다.아울러 "파발타는 PNH 치료의 또 한번의 패러다임 전환을 주도할 신약이다. B인자 억제라는 기전은 대체 경로의 상단에 위치한 B인자에 관여하기 때문에 혈관 내외 용혈을 모두 조절할 수 있으며 임상을 통해 고무적인 결과를 보였다"고 강조했다.2025-01-03 06:00:01어윤호 -
 새해 주요 약가정책은?…스티렌 재평가·국산신약 우대[데일리팜=이탁순 기자] 2025년 을사년 새해 약가제도는 정국 혼란으로 변동성이 클 것으로 전망된다. 해외 약가 비교 재평가, 기등재 경제성 평가 생략 약제 재평가 등이 작년 검토 또는 논의된 가운데 올해 닻을 올릴지도 관심사다.다만 '신약의 혁신가치 반영 및 보건안보를 위한 약가 제도개선' 세부방안들이 대부분 개정 완료되면서 올해 본격적으로 시행에 들어갈 것으로 보인다. 특히, 관련 내용이 가장 많이 담긴 '약제의 결정 및 조정 기준' 일부개정안(2024년 10월 행정예고)이 3월 이전에는 고시될 가능성이 높아 올해 국산신약 우대방안 등이 적용될 것으로 전망된다. 이를 포함해 올해 적용될 약가 정책과 제도를 모아봤다.2025년 약제 급여적정성 재평가2020년 시작된 약제 급여적정성 재평가가 올해도 이어진다. 올해 대상 성분은 올로파타딘염산염, 위령선·괄루근·하고초, 베포타스틴, 구형 흡착탄, 애엽추출물, 엘-오르티틴-엘-아스파르트산, 설글리코타이드, 케노데속시콜산-우르소데속시콜산삼수화물마그네슘염 등 8개 성분이다. 이 가운데 애엽 추출물 3년 평균 청구액이 1215억원으로 가장 높아 재평가 결과에 관심이 클 것으로 예상된다. 애엽 추출물은 오리지널약제인 동아에스티의 스티렌정을 포함해 142개 품목이나 급여 등재돼 있다. 올해 재평가에서 급여 적정성을 인정받지 못한다면 제약사들의 타격이 클 것으로 전망된다. 특히 애엽 추추물은 식약처 동등성 재평가도 진행하고 있어 이번 급여 적정성 재평가가 영향을 줄 것으로 보인다.이밖에 664억원 규모의 올로파타딘염산염, 548억원 규모의 베포타스틴 성분 약제의 급여적정성 결과도 관심이 모아진다. 급여적정성 재평가는 연초 건강보험정책심의위원회 보고를 거쳐 건강보험심사평가원이 3월부터 본격 심사에 들어갈 전망이다.사용량-약가 연동제 최대인하율 12.5%로 상향지난해 10월 복지부가 행정예고한 '약제의 결정 및 조정 기준' 일부 개정안에서는 사용량-약가 연동 대상 약제의 상한금액 최대인하율을 종전 10%에서 15%로 상향 조정하기로 했다. 하지만 2025년 12월 31일까지는 12.5%로, 시행 초기이라는 점을 감안해 조정율을 낮췄다. 이에 올해는 개정안이 고시되는 시점부터 최대 인하율이 12.5%가 적용될 전망이다.현재 최대인하율 10%보다 2.5%가 높아짐에 따라 약가인하에 따른 손실 강도는 더 커질 전망이다.혁신형제약 국내개발신약 약가우대마찬가지로 '약제의 결정 및 조정 기준' 일부 개정안이 고시되면 국내개발신약의 약가우대 방안이 적용된다.특히, 혁신형제약사의 비열등신약은 '대체약제 상한금액 중 최고가'와 '대체약제의 가중평균금액에서 가산(X100/53.55, 약 1.8배)된 금액' 중 '낮은 가격'으로 약가가 매겨지게 된다. 이는 현재 대체약제 가중평균가 이하 가격보다 크게 높아짐에 따라 해당 방안이 적용되는 약제는 이익률이 커질 것으로 전망된다. 신풍제약 '하이알플렉스주' 등이 해당 우대방안을 적용받을지 주목된다.한편, 국산신약은 이중가격제도를 협상 시 적용 가능하도록 해 보다 높은 가격으로 해외에 진출할 수 있는 발판이 마련될 전망이다.국산 원료 국가필수의약품 우대방안국산신약 우대방안과 더불어 국산 원료를 사용한 국가필수의약품 우대방안도 마련된다. 역시 복지부의 약제의 결정 및 조정 기준' 일부 개정안이 고시되면 적용된다. 구체적으로 국산 원료의약품을 사용한 국가필수의약품은 기준요건을 모두 충족한 것으로 간주하기로 했다.아울러 산정된 금액에 (68/53.55 - 1)×100%를 가산하기로 해 약가도 지금보다 높아지게 된다. 정부는 이 방안을 통해 국가필수의약품의 국내 자급율을 높일 것으로 기대하고 있다.혁신형 제약사 7개 제약사 신규 지정혁신형 제약사는 의약품 급여등재시 가산의 근거가 된다. 이에 혁신형 타이틀이 수익과 바로 연결된다. 올해는 동아ST, 암젠코리아, 온코닉테라퓨틱스, 큐로셀, 한올바이오파마, SK바이오사이언스, SK바이오팜이 신규 지정돼 총 49개사가 혁신형 제약기업으로 인정받게 된다. 반면 지난해 6월 혁신형제약기업 재인증 심사서 4개 제약사가 탈락됨에 따라 이들은 기존 혁신형제약사 약가 가산 등 인센티브를 받지 못하게 된다.정부는 올해 혁신형 제약기업 인증취소 기준 개선방안을 마련한다는 계획이다. 특히, 리베이트 관련 인증 요건을 완화할 것으로 보여 관심이 모아진다.약제 요양급여 사전심사 대상 추가정부는 최근 요양급여 사전심사를 받는 약제 대상 조정에 적극 나서면서 작년에는 스트렌식주와 솔리리스·울토미리스 PNH(발작성 야간 혈색소뇨증)' 적응증이 일반심사로 전환됐다.아울러 이달부터는 울토미리스주의 '비정형 용혈성 요독 증후군' 적응증 항목이 사전심사로 추가된다. 비정형 용혈성 요독 증후군 항목의 사전심사 약제는 솔리리스가 유일했었는데, 사전심사 승인율이 낮아 논란이 되고 있는 상황이다. 울토미리스주의 추가로 변화가 생길지 주목된다.이에따라 사전심사 약제 대상은 면역광용요법에 쓰이는 약제, 솔리리스, 울토미리스, 스핀라자, 졸겐스마, 크리스비타, 에브리스디, 럭스터나로, 이들 약제는 요양급여가 적용되려면 사전심사를 통과해야 한다.2025-01-01 17:23:28이탁순
새해 주요 약가정책은?…스티렌 재평가·국산신약 우대[데일리팜=이탁순 기자] 2025년 을사년 새해 약가제도는 정국 혼란으로 변동성이 클 것으로 전망된다. 해외 약가 비교 재평가, 기등재 경제성 평가 생략 약제 재평가 등이 작년 검토 또는 논의된 가운데 올해 닻을 올릴지도 관심사다.다만 '신약의 혁신가치 반영 및 보건안보를 위한 약가 제도개선' 세부방안들이 대부분 개정 완료되면서 올해 본격적으로 시행에 들어갈 것으로 보인다. 특히, 관련 내용이 가장 많이 담긴 '약제의 결정 및 조정 기준' 일부개정안(2024년 10월 행정예고)이 3월 이전에는 고시될 가능성이 높아 올해 국산신약 우대방안 등이 적용될 것으로 전망된다. 이를 포함해 올해 적용될 약가 정책과 제도를 모아봤다.2025년 약제 급여적정성 재평가2020년 시작된 약제 급여적정성 재평가가 올해도 이어진다. 올해 대상 성분은 올로파타딘염산염, 위령선·괄루근·하고초, 베포타스틴, 구형 흡착탄, 애엽추출물, 엘-오르티틴-엘-아스파르트산, 설글리코타이드, 케노데속시콜산-우르소데속시콜산삼수화물마그네슘염 등 8개 성분이다. 이 가운데 애엽 추출물 3년 평균 청구액이 1215억원으로 가장 높아 재평가 결과에 관심이 클 것으로 예상된다. 애엽 추출물은 오리지널약제인 동아에스티의 스티렌정을 포함해 142개 품목이나 급여 등재돼 있다. 올해 재평가에서 급여 적정성을 인정받지 못한다면 제약사들의 타격이 클 것으로 전망된다. 특히 애엽 추추물은 식약처 동등성 재평가도 진행하고 있어 이번 급여 적정성 재평가가 영향을 줄 것으로 보인다.이밖에 664억원 규모의 올로파타딘염산염, 548억원 규모의 베포타스틴 성분 약제의 급여적정성 결과도 관심이 모아진다. 급여적정성 재평가는 연초 건강보험정책심의위원회 보고를 거쳐 건강보험심사평가원이 3월부터 본격 심사에 들어갈 전망이다.사용량-약가 연동제 최대인하율 12.5%로 상향지난해 10월 복지부가 행정예고한 '약제의 결정 및 조정 기준' 일부 개정안에서는 사용량-약가 연동 대상 약제의 상한금액 최대인하율을 종전 10%에서 15%로 상향 조정하기로 했다. 하지만 2025년 12월 31일까지는 12.5%로, 시행 초기이라는 점을 감안해 조정율을 낮췄다. 이에 올해는 개정안이 고시되는 시점부터 최대 인하율이 12.5%가 적용될 전망이다.현재 최대인하율 10%보다 2.5%가 높아짐에 따라 약가인하에 따른 손실 강도는 더 커질 전망이다.혁신형제약 국내개발신약 약가우대마찬가지로 '약제의 결정 및 조정 기준' 일부 개정안이 고시되면 국내개발신약의 약가우대 방안이 적용된다.특히, 혁신형제약사의 비열등신약은 '대체약제 상한금액 중 최고가'와 '대체약제의 가중평균금액에서 가산(X100/53.55, 약 1.8배)된 금액' 중 '낮은 가격'으로 약가가 매겨지게 된다. 이는 현재 대체약제 가중평균가 이하 가격보다 크게 높아짐에 따라 해당 방안이 적용되는 약제는 이익률이 커질 것으로 전망된다. 신풍제약 '하이알플렉스주' 등이 해당 우대방안을 적용받을지 주목된다.한편, 국산신약은 이중가격제도를 협상 시 적용 가능하도록 해 보다 높은 가격으로 해외에 진출할 수 있는 발판이 마련될 전망이다.국산 원료 국가필수의약품 우대방안국산신약 우대방안과 더불어 국산 원료를 사용한 국가필수의약품 우대방안도 마련된다. 역시 복지부의 약제의 결정 및 조정 기준' 일부 개정안이 고시되면 적용된다. 구체적으로 국산 원료의약품을 사용한 국가필수의약품은 기준요건을 모두 충족한 것으로 간주하기로 했다.아울러 산정된 금액에 (68/53.55 - 1)×100%를 가산하기로 해 약가도 지금보다 높아지게 된다. 정부는 이 방안을 통해 국가필수의약품의 국내 자급율을 높일 것으로 기대하고 있다.혁신형 제약사 7개 제약사 신규 지정혁신형 제약사는 의약품 급여등재시 가산의 근거가 된다. 이에 혁신형 타이틀이 수익과 바로 연결된다. 올해는 동아ST, 암젠코리아, 온코닉테라퓨틱스, 큐로셀, 한올바이오파마, SK바이오사이언스, SK바이오팜이 신규 지정돼 총 49개사가 혁신형 제약기업으로 인정받게 된다. 반면 지난해 6월 혁신형제약기업 재인증 심사서 4개 제약사가 탈락됨에 따라 이들은 기존 혁신형제약사 약가 가산 등 인센티브를 받지 못하게 된다.정부는 올해 혁신형 제약기업 인증취소 기준 개선방안을 마련한다는 계획이다. 특히, 리베이트 관련 인증 요건을 완화할 것으로 보여 관심이 모아진다.약제 요양급여 사전심사 대상 추가정부는 최근 요양급여 사전심사를 받는 약제 대상 조정에 적극 나서면서 작년에는 스트렌식주와 솔리리스·울토미리스 PNH(발작성 야간 혈색소뇨증)' 적응증이 일반심사로 전환됐다.아울러 이달부터는 울토미리스주의 '비정형 용혈성 요독 증후군' 적응증 항목이 사전심사로 추가된다. 비정형 용혈성 요독 증후군 항목의 사전심사 약제는 솔리리스가 유일했었는데, 사전심사 승인율이 낮아 논란이 되고 있는 상황이다. 울토미리스주의 추가로 변화가 생길지 주목된다.이에따라 사전심사 약제 대상은 면역광용요법에 쓰이는 약제, 솔리리스, 울토미리스, 스핀라자, 졸겐스마, 크리스비타, 에브리스디, 럭스터나로, 이들 약제는 요양급여가 적용되려면 사전심사를 통과해야 한다.2025-01-01 17:23:28이탁순
오늘의 TOP 10
- 1상장 바이오 추정 순이익 '껑충'...비교군 한미약품 '최다'
- 2고환율에 복잡한 약가인하...사업계획 엄두 못내는 제약사들
- 3완강한 약무정책과장..."플랫폼 도매 허용 동의 힘들어"
- 4"근무약사 연봉 1억"...창고형약국, 파격 급여 제시
- 5플랫폼 도매금지법 간담회, 편파운영 논란…"복지부 협박하나"
- 6'마운자로', 당뇨병 급여 적정성 확인…약가협상 시험대
- 7"웰컴"...K-약국, 해외관광객 소비건수 1년새 67% 증가
- 8[2025 결산] 급여재평가 희비...건보재정 적자터널 진입
- 9사노피 '듀피젠트', 아토피피부염 넘어 천식 공략 눈앞
- 10"대통령, 중대사고 엄벌 주문…제약업계도 대비해야"
-
상품명최고최저평균
-
케토톱플라스타(34매)13,00013,00013,000
-
게보린(10정)4,0003,0003,620
-
노스카나겔(20g)22,00018,00020,703
-
베나치오에프액(75ml)1,0008001,000
-
비코그린에스(20정)5,0004,0004,417












![[리쥬올]리쥬올 PDRN 약국 1위 PDRN](https://cdn.platpharm.co.kr/2025/09/2509260220180000170.webp)
![[리쥬올]레티노 멜라세럼 저자극 레티놀](https://cdn.platpharm.co.kr/2025/09/2509260219360000145.webp)
![[SK케미칼] 트라스트패취 피록시캄 성분](https://cdn.platpharm.co.kr/2025/10/2510020656150002375.webp)
![[유한양행] 콘택콜드 걸렸구나 생각되면](https://cdn.platpharm.co.kr/2025/10/2510282252420008436.webp)
![[유한양행] 미녹펜겔 탈모스팟 집중케어](https://cdn.platpharm.co.kr/2025/09/2509220824180004563.webp)
![[종근당] 벤포벨에스 어른들의 피로회복제](https://cdn.platpharm.co.kr/2025/07/2507290841210004645.webp)
