- LOGIN
- MemberShip
- 2026-05-15 14:32:30
- Pharmaceuticals are focusing on domestic actions for NDMA
- by Chon, Seung-Hyun | translator Choi HeeYoung | 2020-02-06 06:30:22
Investigations have shown that Metformin's impurity content is safe in the US and EU.
In Korea, the Ministry of Food and Drug Safety has also begun inspections after deriving the test method.
The US Food and Drug Administration (FDA) announced on the website that some of the Metformin products sold under the FDA approval and carcinogenic substance 'N-nitrosodimethylamine (NDMA)' was detected, but the daily intake (96 ng) was not exceeded.
Of the 10 products examined, NDMA was detected only in six lots of two Metformin 1000mg ER & Metformin 500mg ER products by Actavis.
Detection amount was 0.01 ~ 0.02 microgram (mcg) per tablet.

In the near future, it will be posted on the website the method for detecting NDMA of Metformin used in the laboratory.
On December 6, last year, the European Medicines Agency (EMA) said on its homepage, “There are very few NDMA detected in some Metformin products sold outside of the EU.
Metformin products in the European Union have not yet been detected for NDMA detection".
In the near future, it is expected that the results of the investigation of Metformin NDMA detection will be released in Korea.
The risk of NDMA in metformin was triggered in Singapore.
On December 4, last year, the Singapore Health and Science Agency (HSA) surveyed 46 metformin products sold locally, recovering three products and detecting NDMA above the daily allowance.

The MFDS has received data on the production of pharmaceuticals containing Metformin hydrochloride and the systematic investigation of raw materials used until December 17 last year.
Pharmaceutical companies submitted the total number of drugs containing Metformin, items and number of production records, items and quantity without production record to the MFDS.
The Metformin lineage survey at the MFDS is a preliminary activity to prepare for the detection of impurities.
If a problem occurs in a particular drug substance or drug product, the intention is to follow up quickly and accurately based on the results of the systematic investigation submitted by the pharmaceutical company.
The MFDS unveiled Metformin's NDMA test on January 15, a month and a half after the Metformin NDMA risks were raised in Singapore.
It was suggested to test by Gas Chromatography (GC) method.
The industry is alert on the results of Metformin's NDMA inspection in Korea.
It is not easy for pharmaceutical companies to test whether they detect Metformin's NDMA.
That's because there aren't enough institutions with analyzers to make self-checks.
Some pharmaceutical companies are reportedly considering buying their own analyzers.
However, it costs ₩300 to 500 million for each analyzer and every year, ₩ tens of millions in management costs are inevitable.
Pharmaceutical companies fear that if Metformin is the case, with massive losses in Valsartan and Ranitidine, irreversible losses can occur.
Metformin is overwhelmingly larger than Valsartan and Ranitidine.
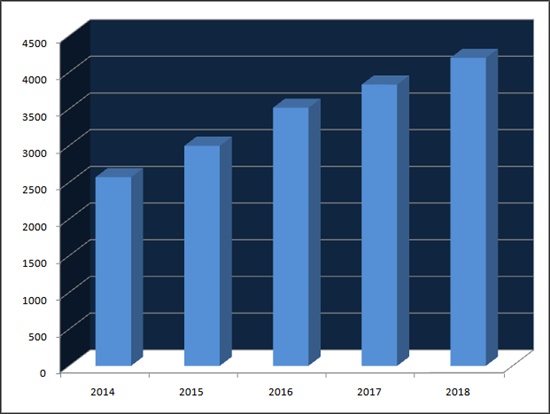
According to UBIST data of drug research institutes, the outpatient prescription market of Metformin-containing drugs in 2018 was estimated at ₩420 billion.
Ranitidine, which had been suspended from selling all its products, has formed a prescription scale of about ₩200 billion, which is more than double the market.
The unit price of Metformin is less than ₩100.
That's an overwhelming amount of ranitidine.
In the case of Valsartan, the MFDS discontinued the sale of drug products that used the ingredients in question at least once in January 2015.
Many products are likely to be discontinued even though they did not use the raw materials in question.
In the United States, only the products using the Zhejiang Huahai Pharmaceutical raw materials were recovered by manufacturing unit.
No action was taken to sell the entire item.
In Europe, the measure of action was similar.
All ranitidine products have been discontinued in Korea.
while in the US and Europe, pharmaceuticals were collected by their own lot numbers.
In the case of 13 items of Nizatidine have been discontinued, but some of the products have been recalled in Japan, and no products have been ordered in the United States and Europe.
An official from the MFDS said, "We are in the process of inspecting the Metformin NDMA test after deriving it".
-

- 0
댓글 운영방식은
댓글은 실명게재와 익명게재 방식이 있으며, 실명은 이름과 아이디가 노출됩니다. 익명은 필명으로 등록 가능하며, 대댓글은 익명으로 등록 가능합니다.
댓글 노출방식은
댓글 명예자문위원(팜-코니언-필기모양 아이콘)으로 위촉된 데일리팜 회원의 댓글은 ‘게시판형 보기’와 ’펼쳐보기형’ 리스트에서 항상 최상단에 노출됩니다. 새로운 댓글을 올리는 일반회원은 ‘게시판형’과 ‘펼쳐보기형’ 모두 팜코니언 회원이 쓴 댓글의 하단에 실시간 노출됩니다.
댓글의 삭제 기준은
다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입제한이 될 수도 있습니다.
-
저작권·인격권 등 타인의 권리를 침해하는 경우
상용 프로그램의 등록과 게재, 배포를 안내하는 게시물
타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
-
근거 없는 비방·명예를 훼손하는 게시물
특정 이용자 및 개인에 대한 인신 공격적인 내용의 글 및 직접적인 욕설이 사용된 경우
특정 지역 및 종교간의 감정대립을 조장하는 내용
사실 확인이 안된 소문을 유포 시키는 경우
욕설과 비어, 속어를 담은 내용
정당법 및 공직선거법, 관계 법령에 저촉되는 경우(선관위 요청 시 즉시 삭제)
특정 지역이나 단체를 비하하는 경우
특정인의 명예를 훼손하여 해당인이 삭제를 요청하는 경우
특정인의 개인정보(주민등록번호, 전화, 상세주소 등)를 무단으로 게시하는 경우
타인의 ID 혹은 닉네임을 도용하는 경우
-
게시판 특성상 제한되는 내용
서비스 주제와 맞지 않는 내용의 글을 게재한 경우
동일 내용의 연속 게재 및 여러 기사에 중복 게재한 경우
부분적으로 변경하여 반복 게재하는 경우도 포함
제목과 관련 없는 내용의 게시물, 제목과 본문이 무관한 경우
돈벌기 및 직·간접 상업적 목적의 내용이 포함된 게시물
게시물 읽기 유도 등을 위해 내용과 무관한 제목을 사용한 경우
-
수사기관 등의 공식적인 요청이 있는 경우
-
기타사항
각 서비스의 필요성에 따라 미리 공지한 경우
기타 법률에 저촉되는 정보 게재를 목적으로 할 경우
기타 원만한 운영을 위해 운영자가 필요하다고 판단되는 내용
-
사실 관계 확인 후 삭제
저작권자로부터 허락받지 않은 내용을 무단 게재, 복제, 배포하는 경우
타인의 초상권을 침해하거나 개인정보를 유출하는 경우
당사에 제공한 이용자의 정보가 허위인 경우 (타인의 ID, 비밀번호 도용 등)
※이상의 내용중 일부 사항에 적용될 경우 이용약관 및 관련 법률에 의해 제재를 받으실 수도 있으며, 민·형사상 처벌을 받을 수도 있습니다.
※위에 명시되지 않은 내용이더라도 불법적인 내용으로 판단되거나 데일리팜 서비스에 바람직하지 않다고 판단되는 경우는 선 조치 이후 본 관리 기준을 수정 공시하겠습니다.
※기타 문의 사항은 데일리팜 운영자에게 연락주십시오. 메일 주소는 dailypharm@dailypharm.com입니다.
- [Reporter's View] The dark side of improved diabetes med convenience
- Reporter's view | Son, Hyung Min
- [Reporter's View] Contradiction of "K-passing" and a new drug powerhouse
- Reporter's view | Lee, Jeong-Hwan






