- LOGIN
- MemberShip
- 2026-05-14 07:58:53
- Stomach ulcer drug rebamipide market makes over KRW 100 bln
- by An, Kyung-Jin | translator Byun Kyung A | 2021-02-03 06:10:23
The impurity contamination in ranitidine was discovered in 2019 has in turn expanded a gastritis treatment rebamipide market.
Although the market was sluggish for a long time, rebamipide prescription surged and broke through the 100 billion won point last year.
The impurity contamination incident impacted the entire stomach disorder drug market including H2 receptor antagonist, proton pump inhibitor (PPI) and wormwood-induced natural medicine.
A pharmaceutical market research firm UBIST reported on Feb.
2, the rebamipide prescription market last year generated 110.6 billion won, growing by 14.8 percent compared to the year before.
The market’s annual growth has been stagnating around 4 percent, marking 85.4 billion won, 88.2 billion won and 91.9 billion in year 2016 through 2018, respectively.
But the figure soared 20.4 percent last year compared to two years ago.
Rebamipide treats gastroduodenal ulcers by increasing the blood flow in the stomach mucous to protect them.
The substance is also indicated to treat stomach ulcer and enhance mucosal defense.
About three decades ago, Korea Otsuka Pharmaceutical released an original Mucosta, and 239 generics entered the market since 2003.
Regardless of the expanded options, the prescription volume did not change significantly.
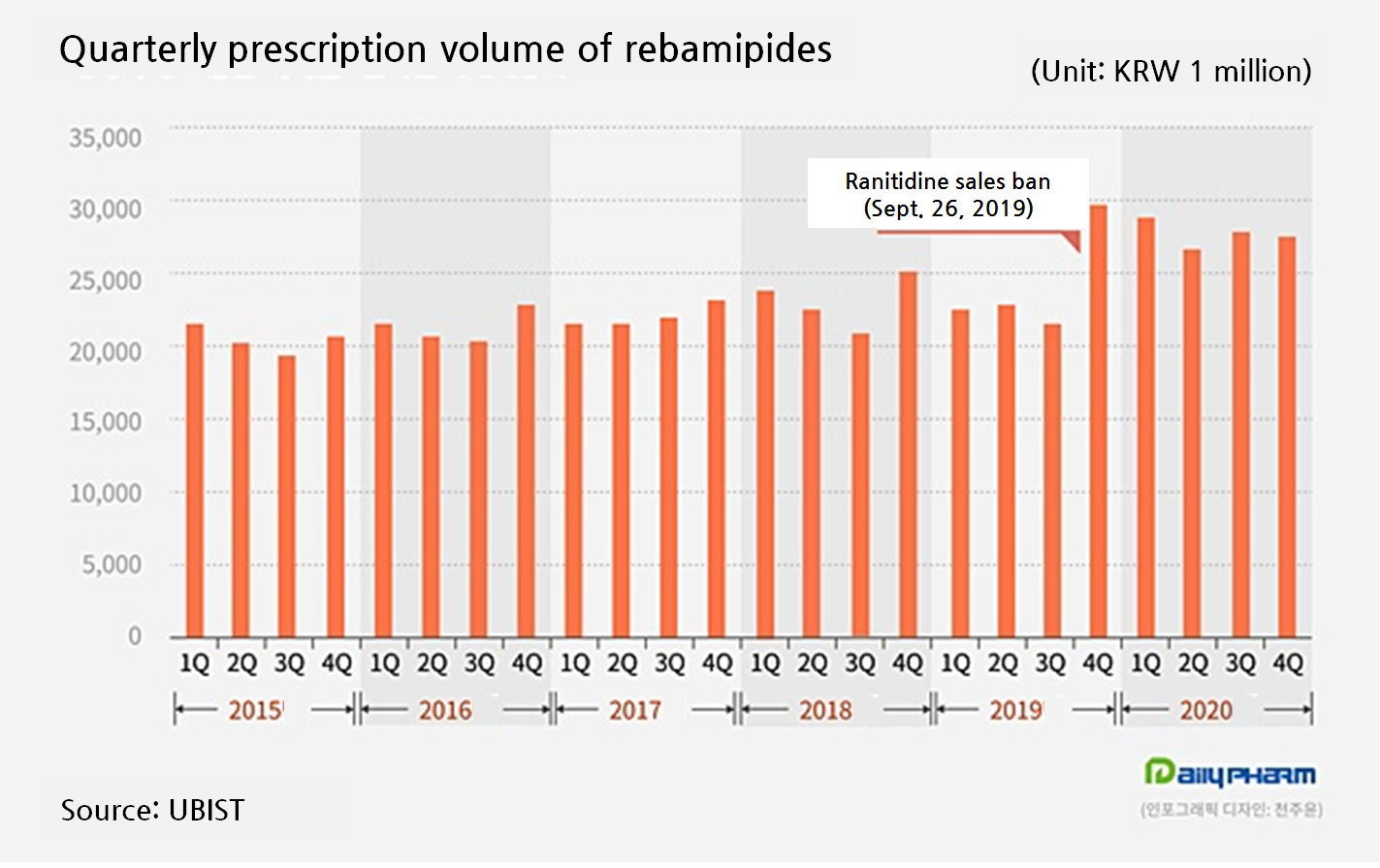
The South Korean Ministry of Food and Drug Safety (MFDS) banned the sales of all products of H2 receptor antagonizing antiulcer drug ranitidine due to unacceptable amount of cancerous N-Nitrosodimethylamine (NDMA) found in late September 2019.
Ranitidine drugs used to form a large market making about 180 billion won annually as of 2018.
But the overall sales ban drove the prescribers to seek after other drugs with similar indications.
The analysis on quarterly prescription volume of rebamipide found the volume started increasing from the fourth quarter of 2019.
In the third quarter of 2019, the rebamipide drug prescription generated 21.5 billion won only, but it leapt to 29.6 billion won as of 2019 fourth quarter.
Although patients avoided visiting hospitals amid COVID-19 last year and the general prescription volume faltered, the quarterly rebamipide prescription volume was maintained at around 27 billion won.
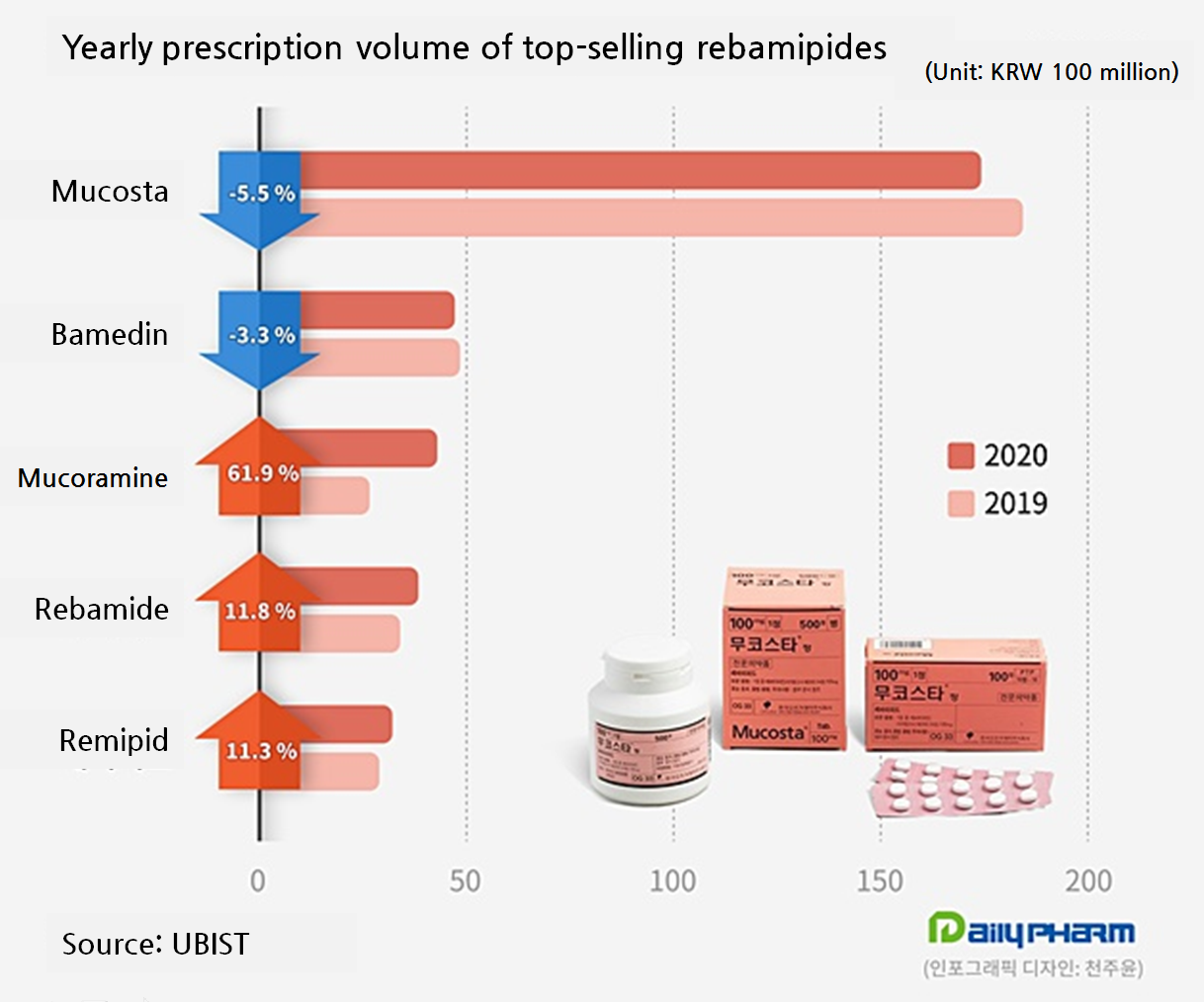
Generally, the generics had more significant increase in prescription.
The original Mucosta’s prescription fell 5.5 percent last year, despite making 17.3 billion won, compared to the year before.
The best-selling generic Samjin Pharm’s Bamedin prescription also fell by 3.3 percent last year compared to the previous year and marked 4.6 billion won.
Meanwhile, Huons’ Mucoramine prescription soared by 61.9 percent compared to the year before and narrowed the gap with Bamedin.
KyungDong Pharmaceutical’s Rebamide prescription volume grew 11.8 percent from the year before and marked 3.8 billion won, when CMG Pharmaceutical’s Remipid and Celltrion Pharm’s Rebat grew by 11.3 percent and 35.8 percent, respectively.
The industry projects the rebamipide market competition would get even more intensified this year with extended release products launching.
Four South Korean companies like Yuhan Corporation, GC Pharma, Daewoong Pharmaceutical and Daewon Pharmaceutical won the health authority’s approval on extended release rebamipides late last year.
And the authority also granted approval on Korea Otsuka Pharmaceutical’s Mucosta SR tablet last month.
Although some of their indications differ from each other a bit, the administration convenience improved from three times a day to twice-daily.
-

- 0
댓글 운영방식은
댓글은 실명게재와 익명게재 방식이 있으며, 실명은 이름과 아이디가 노출됩니다. 익명은 필명으로 등록 가능하며, 대댓글은 익명으로 등록 가능합니다.
댓글 노출방식은
댓글 명예자문위원(팜-코니언-필기모양 아이콘)으로 위촉된 데일리팜 회원의 댓글은 ‘게시판형 보기’와 ’펼쳐보기형’ 리스트에서 항상 최상단에 노출됩니다. 새로운 댓글을 올리는 일반회원은 ‘게시판형’과 ‘펼쳐보기형’ 모두 팜코니언 회원이 쓴 댓글의 하단에 실시간 노출됩니다.
댓글의 삭제 기준은
다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입제한이 될 수도 있습니다.
-
저작권·인격권 등 타인의 권리를 침해하는 경우
상용 프로그램의 등록과 게재, 배포를 안내하는 게시물
타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
-
근거 없는 비방·명예를 훼손하는 게시물
특정 이용자 및 개인에 대한 인신 공격적인 내용의 글 및 직접적인 욕설이 사용된 경우
특정 지역 및 종교간의 감정대립을 조장하는 내용
사실 확인이 안된 소문을 유포 시키는 경우
욕설과 비어, 속어를 담은 내용
정당법 및 공직선거법, 관계 법령에 저촉되는 경우(선관위 요청 시 즉시 삭제)
특정 지역이나 단체를 비하하는 경우
특정인의 명예를 훼손하여 해당인이 삭제를 요청하는 경우
특정인의 개인정보(주민등록번호, 전화, 상세주소 등)를 무단으로 게시하는 경우
타인의 ID 혹은 닉네임을 도용하는 경우
-
게시판 특성상 제한되는 내용
서비스 주제와 맞지 않는 내용의 글을 게재한 경우
동일 내용의 연속 게재 및 여러 기사에 중복 게재한 경우
부분적으로 변경하여 반복 게재하는 경우도 포함
제목과 관련 없는 내용의 게시물, 제목과 본문이 무관한 경우
돈벌기 및 직·간접 상업적 목적의 내용이 포함된 게시물
게시물 읽기 유도 등을 위해 내용과 무관한 제목을 사용한 경우
-
수사기관 등의 공식적인 요청이 있는 경우
-
기타사항
각 서비스의 필요성에 따라 미리 공지한 경우
기타 법률에 저촉되는 정보 게재를 목적으로 할 경우
기타 원만한 운영을 위해 운영자가 필요하다고 판단되는 내용
-
사실 관계 확인 후 삭제
저작권자로부터 허락받지 않은 내용을 무단 게재, 복제, 배포하는 경우
타인의 초상권을 침해하거나 개인정보를 유출하는 경우
당사에 제공한 이용자의 정보가 허위인 경우 (타인의 ID, 비밀번호 도용 등)
※이상의 내용중 일부 사항에 적용될 경우 이용약관 및 관련 법률에 의해 제재를 받으실 수도 있으며, 민·형사상 처벌을 받을 수도 있습니다.
※위에 명시되지 않은 내용이더라도 불법적인 내용으로 판단되거나 데일리팜 서비스에 바람직하지 않다고 판단되는 경우는 선 조치 이후 본 관리 기준을 수정 공시하겠습니다.
※기타 문의 사항은 데일리팜 운영자에게 연락주십시오. 메일 주소는 dailypharm@dailypharm.com입니다.
- [Reporter's View] Contradiction of "K-passing" and a new drug powerhouse
- Reporter's view | Lee, Jeong-Hwan





