- LOGIN
- MemberShip
- 2026-05-11 00:21:56
- Entresto's outpatient prescriptions exceed ₩30 billion
- by | translator Alice Kang | 2022-02-08 05:54:47

of Entresto Sales of Novartis’ chronic heart failure treatment ‘Entresto’ exceeded ₩30 billion only 5 years into its release.
In the midst of drug price cuts and domestic patent challenges, Entresto is seeking greater growth this year by expanding the scope of indications and reimbursement benefits.
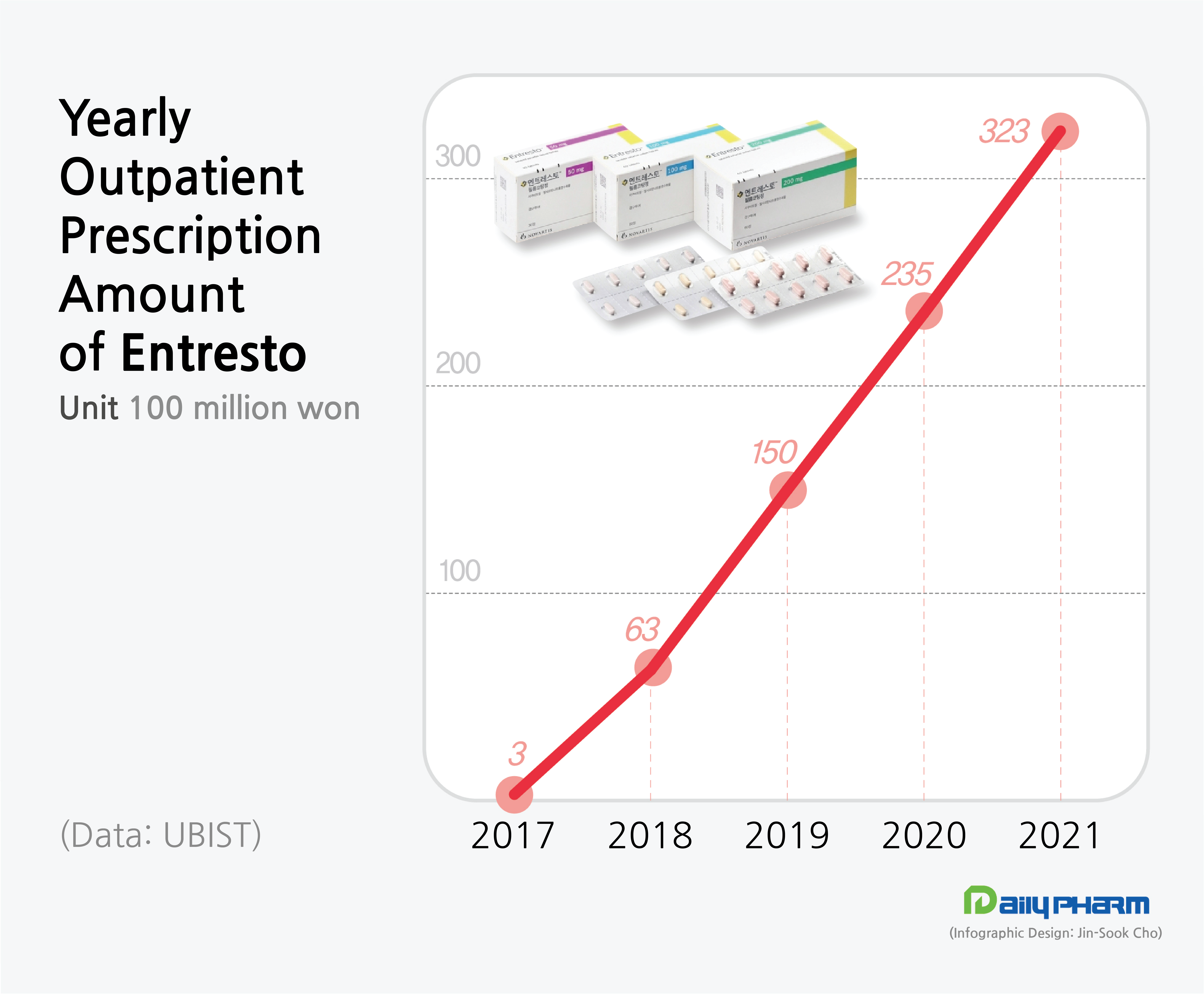
According to the market research institution UBIST on the 29th, outpatient prescription sales of Entresto recorded ₩32.3 billion, a 37.3% growth from the ₩23.5 billion made in the previous year.
The product made such growth in only 4 years since its release in October 2017.
Entresto is a first-in-class angiotensin receptor-neprilysin inhibitor (ARNI) that combines the angiotensin receptor blocker (ARB) valsartan and neprilysin inhibitor sacubitril.
The drug may be used as an alternative to an angiotensin receptor blocker (ARB) or an angiotensin-converting enzyme (ACE) inhibitor in patients with left ventricular (LV) dysfunction in combination with other heart failure treatments.
Entresto received marketing authorization in April 2016 and was officially launched with reimbursement in October 2017.
The drug demonstrated its efficacy and safety in acute heart failure in addition to chronic heart failure, and academic societies in Korea and abroad recommend Entresto as a standard of care.
Also, the American Heart Association recommended Entresto as the standard of care for heart failure with reduced ejection fraction (HFrEF).
Until now, ACE or ARB inhibitors were mainly used in patients with chronic heart failure.
Replacing this demand, Entresto quickly increased its share in the market.
Its outpatient prescription sales, which started at ₩300 million in 2017, increased 20 times to ₩6.3 billion the next year.
In 2019, its sales doubled once more to ₩15 billion, then rose to exceed ₩30 billion only 2 years since then.
To slow down such growth, pharmaceutical companies in Korea have aggressively set out to challenge Entresto’s patent.
13 domestic companies including Hanmi Pharmaceuticals and Chong Kun Dang filed patent challenges last year.
The Intellectual Property Trial and Appeal Board ruled in favor of the generic companies in the trial to confirm the passive scope of rights of Entresto’s crystalline patent.
By overcoming the key patent among 5 of Entresto’s patents, the domestic generic companies are speeding up their challenges.
Also, Entresto’s price will undergo additional price cuts.
The Ministry of Health and Welfare is working to cut Entresto’s price by 6.6% as of February 1st under the ‘‘Amendment to the drug reimbursement list and reimbursement ceiling price table.’ Entresto is subject to pricing cuts under the ‘Use amount-price linkage-type B’ where a product whose use increased over 10% in an amount over ₩5 billion undergo price cuts.
The price of Entresto, which was listed at ₩2,243 at the time of first listing, will be reduced to ₩1,910 through three pricing adjustments.
Novartis plans to continue its strong growth by adding indications and expanding Entresto’s reimbursement standards.
Its indication for HFpEF is one of the company’s key areas of interest.
Although around half of all patients with heart failure suffer HFpEF, which is defined as a left ventricular ejection fraction of 40% or higher, no appropriate treatment had existed for the condition yet.
Novartis demonstrated that Entresto can reduce the risk of hospitalization from heart failure and cardiovascular death through the PARAGON-HF trial.
The UF Food and Drug Administration additionally approved the HFpEF indication for Entresto in January last year.
In line with the added indication, Novartis is working to expand the scope of Entresto’s reimbursement to first-line therapy in HFrEF.
-

- 0
댓글 운영방식은
댓글은 실명게재와 익명게재 방식이 있으며, 실명은 이름과 아이디가 노출됩니다. 익명은 필명으로 등록 가능하며, 대댓글은 익명으로 등록 가능합니다.
댓글 노출방식은
댓글 명예자문위원(팜-코니언-필기모양 아이콘)으로 위촉된 데일리팜 회원의 댓글은 ‘게시판형 보기’와 ’펼쳐보기형’ 리스트에서 항상 최상단에 노출됩니다. 새로운 댓글을 올리는 일반회원은 ‘게시판형’과 ‘펼쳐보기형’ 모두 팜코니언 회원이 쓴 댓글의 하단에 실시간 노출됩니다.
댓글의 삭제 기준은
다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입제한이 될 수도 있습니다.
-
저작권·인격권 등 타인의 권리를 침해하는 경우
상용 프로그램의 등록과 게재, 배포를 안내하는 게시물
타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
-
근거 없는 비방·명예를 훼손하는 게시물
특정 이용자 및 개인에 대한 인신 공격적인 내용의 글 및 직접적인 욕설이 사용된 경우
특정 지역 및 종교간의 감정대립을 조장하는 내용
사실 확인이 안된 소문을 유포 시키는 경우
욕설과 비어, 속어를 담은 내용
정당법 및 공직선거법, 관계 법령에 저촉되는 경우(선관위 요청 시 즉시 삭제)
특정 지역이나 단체를 비하하는 경우
특정인의 명예를 훼손하여 해당인이 삭제를 요청하는 경우
특정인의 개인정보(주민등록번호, 전화, 상세주소 등)를 무단으로 게시하는 경우
타인의 ID 혹은 닉네임을 도용하는 경우
-
게시판 특성상 제한되는 내용
서비스 주제와 맞지 않는 내용의 글을 게재한 경우
동일 내용의 연속 게재 및 여러 기사에 중복 게재한 경우
부분적으로 변경하여 반복 게재하는 경우도 포함
제목과 관련 없는 내용의 게시물, 제목과 본문이 무관한 경우
돈벌기 및 직·간접 상업적 목적의 내용이 포함된 게시물
게시물 읽기 유도 등을 위해 내용과 무관한 제목을 사용한 경우
-
수사기관 등의 공식적인 요청이 있는 경우
-
기타사항
각 서비스의 필요성에 따라 미리 공지한 경우
기타 법률에 저촉되는 정보 게재를 목적으로 할 경우
기타 원만한 운영을 위해 운영자가 필요하다고 판단되는 내용
-
사실 관계 확인 후 삭제
저작권자로부터 허락받지 않은 내용을 무단 게재, 복제, 배포하는 경우
타인의 초상권을 침해하거나 개인정보를 유출하는 경우
당사에 제공한 이용자의 정보가 허위인 경우 (타인의 ID, 비밀번호 도용 등)
※이상의 내용중 일부 사항에 적용될 경우 이용약관 및 관련 법률에 의해 제재를 받으실 수도 있으며, 민·형사상 처벌을 받을 수도 있습니다.
※위에 명시되지 않은 내용이더라도 불법적인 내용으로 판단되거나 데일리팜 서비스에 바람직하지 않다고 판단되는 경우는 선 조치 이후 본 관리 기준을 수정 공시하겠습니다.
※기타 문의 사항은 데일리팜 운영자에게 연락주십시오. 메일 주소는 dailypharm@dailypharm.com입니다.
- [Reporter's View] Contradiction of "K-passing" and a new drug powerhouse
- Reporter's view | Lee, Jeong-Hwan
- [Reporter’s View] Medical Devices Act binds payment within 6 months
- Reporter's view | Hwang, byoung woo






