- LOGIN
- MemberShip
- 2026-05-06 14:01:18
- Companies in KOR and abroad compete in Eylea biosimilar mkt
- by Son, Hyung-Min | translator Kim, Jung-Ju | 2023-12-05 05:48:52
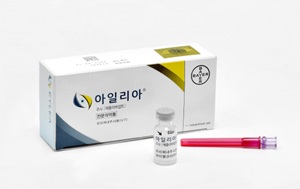
Not only domestic biosimilar companies like Celltrion and Samsung Bioepis but also traditional pharmaceutical companies such as Sam Chun Dang Pharm have thrown down the gauntlet.
Bayer and Regeneron, the original developers of Eylea, thus face fierce market competition not only with biosimilar developers but also with Roche's next-generation macular degeneration treatment, Vabysmo.
According to industry sources on the 3rd, among domestic companies, Sam Chun Dang Pharm, Celltrion, Samsung Bioepis, and Alteogen are currently developing Eylea (aflibercept) biosimilars.
All four companies have set their sights on the global market, preparing to receive approvals in the U.S.
and Europe in addition to the Korean market.
In the U.S., Celltrion, Amgen, and Sandoz are close to commercializing their biosimilars in the U.S.
These companies have now completed global Phase III clinical trials and applied for marketing authorization in the U.S.
and Europe.
Eylea’s U.S.
new drug exclusivity expires next May, and its European substance patent expires in November 2025.

The company applied for the marketing authorization of its Eylea biosimilar candidate ‘SCD411’ in two formulations - vial and prefilled syringe formulation – in Korea last month.
Sam Chung Dang Pharm is the first company to apply for the approval of a prefilled syringe formulation of Eylea.
The application was filed based on SCD411’s Phase III trial results.
The trial, which had been conducted on 576 patients, demonstrated SCD411’s bioequivalence to Eylea.
Based on the results, Sam Chung Dang Pharm is also preparing to apply for marketing approval of SCD411 in the United States and Europe as well.
Eylea to inevitably compete with biosimilars and Vabysmo
Eylea’s global sales were approximately USD 1.4 billion (KRW 1.9 trillion) in Q1 this year and USD 1.5 billion (KRW 2.373 trillion) in Q2 this year.
Eylea had posted the highest sales in the domestic macular degeneration market.
According to the pharmaceutical market research institution IQVIA, Eylea’s sales, which had been around KRW 46.8 billion in 2019, exceeded KRW 60 billion in 2020.
Sales continued to grow, and Eylea posted KRW 80.4 billion in sales last year.
However, sales generated by Eylea’s competitors last year, Novartis’ Lucentis (ranibizumab) and Beovu (brolucizumab) were only KRW 29.4 and KRW 14.5 billion, respectively.
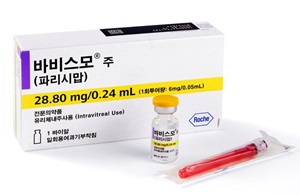
In addition to the challenges made by the biosimilar developers, Bayer’s Eylea is starting competition in earnest with Roche's macular degeneration drug Vabysmo (faricimab).
Unlike existing VEGF inhibitors like Lucentis, and Eylea, the drug’s dual mechanism of action allows for it to also block the angiopoietin-2 (Ang-2) pathway to inhibit neovascularization.
In particular, in clinical trials, Vabysmo improved visual acuity at a level non-inferior to that of Eylea, which is administered at 8-week intervals, when administered at intervals of up to 16 weeks.
Vabysmo was granted reimbursement and released in earnest in October last month.
Roche is also known to be planning to introduce a prefilled syringe formulation of Vabysmo next year.
-

- 0
댓글 운영방식은
댓글은 실명게재와 익명게재 방식이 있으며, 실명은 이름과 아이디가 노출됩니다. 익명은 필명으로 등록 가능하며, 대댓글은 익명으로 등록 가능합니다.
댓글 노출방식은
댓글 명예자문위원(팜-코니언-필기모양 아이콘)으로 위촉된 데일리팜 회원의 댓글은 ‘게시판형 보기’와 ’펼쳐보기형’ 리스트에서 항상 최상단에 노출됩니다. 새로운 댓글을 올리는 일반회원은 ‘게시판형’과 ‘펼쳐보기형’ 모두 팜코니언 회원이 쓴 댓글의 하단에 실시간 노출됩니다.
댓글의 삭제 기준은
다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입제한이 될 수도 있습니다.
-
저작권·인격권 등 타인의 권리를 침해하는 경우
상용 프로그램의 등록과 게재, 배포를 안내하는 게시물
타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
-
근거 없는 비방·명예를 훼손하는 게시물
특정 이용자 및 개인에 대한 인신 공격적인 내용의 글 및 직접적인 욕설이 사용된 경우
특정 지역 및 종교간의 감정대립을 조장하는 내용
사실 확인이 안된 소문을 유포 시키는 경우
욕설과 비어, 속어를 담은 내용
정당법 및 공직선거법, 관계 법령에 저촉되는 경우(선관위 요청 시 즉시 삭제)
특정 지역이나 단체를 비하하는 경우
특정인의 명예를 훼손하여 해당인이 삭제를 요청하는 경우
특정인의 개인정보(주민등록번호, 전화, 상세주소 등)를 무단으로 게시하는 경우
타인의 ID 혹은 닉네임을 도용하는 경우
-
게시판 특성상 제한되는 내용
서비스 주제와 맞지 않는 내용의 글을 게재한 경우
동일 내용의 연속 게재 및 여러 기사에 중복 게재한 경우
부분적으로 변경하여 반복 게재하는 경우도 포함
제목과 관련 없는 내용의 게시물, 제목과 본문이 무관한 경우
돈벌기 및 직·간접 상업적 목적의 내용이 포함된 게시물
게시물 읽기 유도 등을 위해 내용과 무관한 제목을 사용한 경우
-
수사기관 등의 공식적인 요청이 있는 경우
-
기타사항
각 서비스의 필요성에 따라 미리 공지한 경우
기타 법률에 저촉되는 정보 게재를 목적으로 할 경우
기타 원만한 운영을 위해 운영자가 필요하다고 판단되는 내용
-
사실 관계 확인 후 삭제
저작권자로부터 허락받지 않은 내용을 무단 게재, 복제, 배포하는 경우
타인의 초상권을 침해하거나 개인정보를 유출하는 경우
당사에 제공한 이용자의 정보가 허위인 경우 (타인의 ID, 비밀번호 도용 등)
※이상의 내용중 일부 사항에 적용될 경우 이용약관 및 관련 법률에 의해 제재를 받으실 수도 있으며, 민·형사상 처벌을 받을 수도 있습니다.
※위에 명시되지 않은 내용이더라도 불법적인 내용으로 판단되거나 데일리팜 서비스에 바람직하지 않다고 판단되는 경우는 선 조치 이후 본 관리 기준을 수정 공시하겠습니다.
※기타 문의 사항은 데일리팜 운영자에게 연락주십시오. 메일 주소는 dailypharm@dailypharm.com입니다.
- [Reporter’s View] Medical Devices Act binds payment within 6 months
- Reporter's view | Hwang, byoung woo
- "Vabysmo PFS shifts the retinal disease treatment persistence·efficiency"
- Reporter's view | Son, Hyung Min







