- LOGIN
- MemberShip
- 2026-05-06 12:41:40
- K-pharma advances in new Alzheimer’s drug discovery
- by | translator Kim, Jung-Ju | 2024-01-09 05:50:07
New drugs for treating Alzheimer’s disease developed by Korean pharmaceutical companies have entered the late phase of clinical trials, and industry watchers are closely monitoring their potential for commercialization.
Aribio has recently submitted an Investigational New Drug (IND) application for its oral treatment candidate AR1001 for Alzheimer’s disease, to eight European countries.
Aribio is about to enter the late phase of clinical trials in Europe, following its success in initiating Phase 3 clinical trials in Korea and United States.
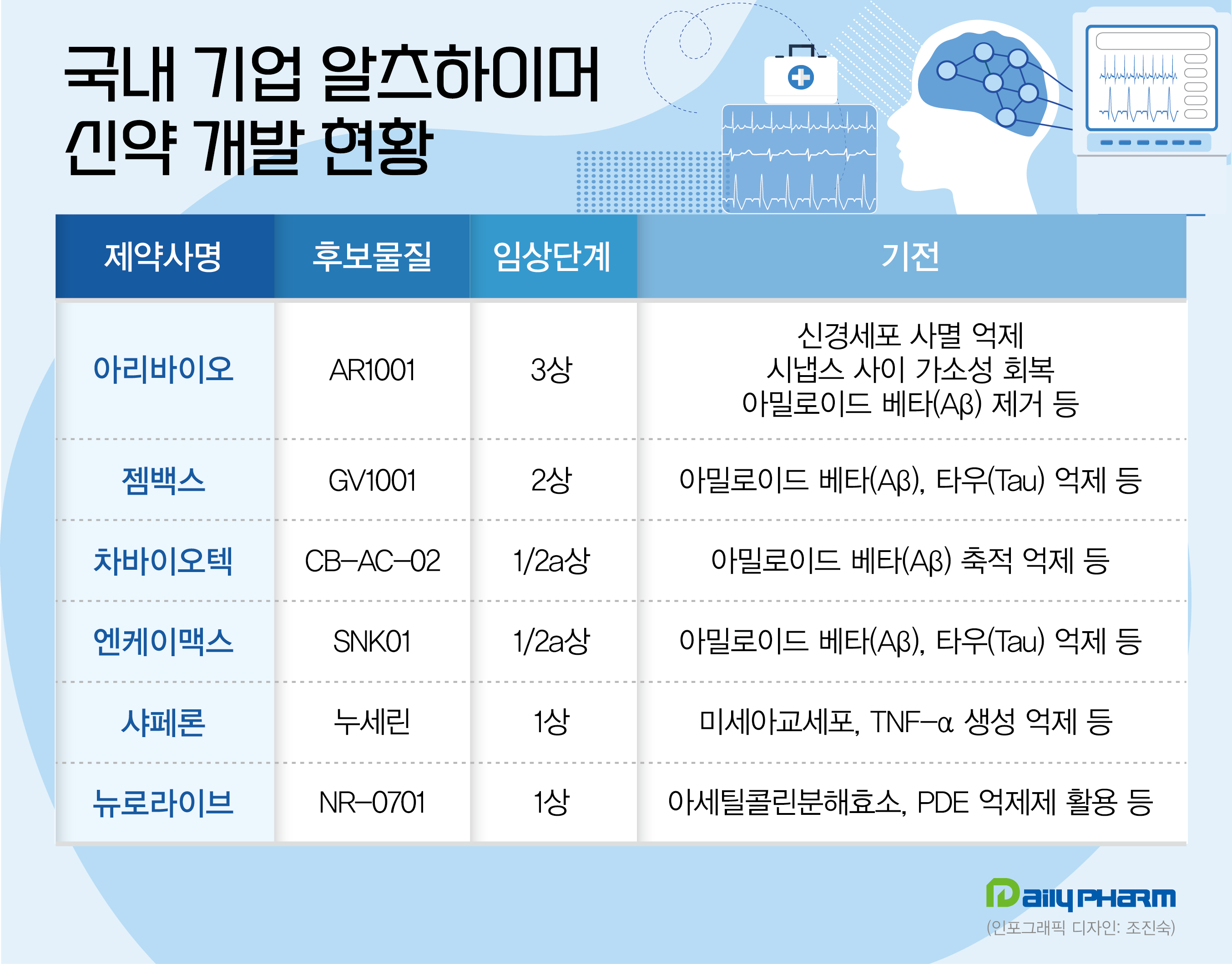
Additionally, each of the new Alzheimer’s disease drug candidates developed by GemVex, CHA Biotech, and NKMAX has entered Phase 2 clinical trials.
The European clinical trials will enroll 400 patients with early Alzheimer’s disease from eight European countries, including the U.K., France, Germany, Spain, Italy, Denmark, Netherlands, the Czech Republic, and Slovakia.
AR1001 utilizes multimodal mechanisms to target the underlying causes of Alzheimer’s disease, such as PDE5 and toxic proteins.
In 2022, Phase 3 clinical trials were initiated in the United States, and these trials are recruiting patients and administering the drug at 60 major clinical sites across the United States.
Samjin Pharmaceutical holds exclusive sales rights for AR1001 in Korea.
Samjin Pharmaceutical and Aribio have signed a joint development of Phase 3 trials in Korea, as well as the exclusive sales rights for the domestic market.
Both companies are currently conducting Phase 3 trials in Korea.
In Phase 2 clinical trials, AR1001 demonstrated therapeutic effects in patients with elevated levels of blood pTau-181, a significant factor associated with Alzheimer’s disease.
Additionally, the AR1001 10mg cohort demonstrated a decrease in cognitive decline compared to the placebo group, while the AR1001 30mg cohort demonstrated enhancements in cognitive abilities related to pattern recognition.
GemVex is currently developing GV1001, a candidate multimodal treatment for Alzheimer’s disease.
GV1001 has successfully concluded the Korean Phase 2 clinical trials and is preparing for global Phase 2 clinical trials.
GV1001 binds to the Gonadotropin-releasing hormone receptor (GnRHR) expressed in microglia and astrocytes, effectively suppressing neuroinflammation.
By binding to GnRHR, present on these two cell types, GV1001 functions as a cytokine that modulates brain immune responses.
GemVex will conduct simultaneous clinical trials in seven European countries using the Phase 2 clinical trials IND application submitted to the FDA.
The clinical trials will evaluate the therapeutic effects and safety of the drug with 185 moderate to severe patients administered with doses of 0.56 mg and 1.12 mg over 52 weeks.
CHA Biotech is conducting Phase 1/2a clinical trials for its new drug candidate CB-AC-02.
CB-AC-02 is a stem cell therapy utilizing placenta-derived mesenchymal stem cells and is under development using mass culture and cryopreservation techniques.
NKMAX is currently developing the cell therapy SNK01 through its subsidiary NKGen Biotech.
The company has successfully completed the drug administration to patients enrolling in the Phase 1/2a clinical trials.
SNK01 is designed to recognize and eliminate reactive T cells and damaged neurons, thereby reducing neuroinflammation and improving the overall brain immune system.
In the Phase 1 clinical trials conducted in Mexico, NKGen Biotech’s SNK01 demonstrated the therapeutic effects in patients with moderate to severe Alzheimer’s disease.
Three out of ten patients who were administered SNK01 showed improved symptoms in the AD Composite Score (ADCOMS), while six patients showed no change without further deterioration.
Furthermore, the FDA has granted permission to continue the Phase 1/2a clinical trials without requiring preclinical trials, based on the results obtained from the Mexico Phase 1 clinical trials.
Neurorive and Shaperon, completing pre-clinical trials, aim to enter a late phase of clinical trials. Shaperon is developing NuCerin for treating patients with moderate to severe Alzheimer’s disease.
NuCerin is designed to inhibit microglia and TNF-α production and under development to alleviate neuroinflammation.
NuCerin is currently in the Korean Phase 1 clinical trials.
Nucerin demonstrated no Dose Limiting Toxicities (DLT) up to the third level of dosage during the trial, following a dose escalation design.
Additionally, Shaperon signed a technology transfer contract with Kukjeon Pharmaceutical in March 2021.
Neurorive is currently conducting Korean Phase 1 clinical trials for their candidate product NR-0701.
NR-0701 utilizes acetylcholinesterase and phosphodiesterase (PDE) inhibitors, which are the active ingredients found in medications like Donepezil, used for Alzheimer’s disease, and Viagra, respectively.
Through this mechanism, Neurorive aims to achieve effects that are comparable to increased therapeutic effects of Alzheimer's disease drug Donepezil while simultaneously reducing the toxicity associated with Viagra-class drugs, maximizing neurotransmission capacity.
-

- 0
댓글 운영방식은
댓글은 실명게재와 익명게재 방식이 있으며, 실명은 이름과 아이디가 노출됩니다. 익명은 필명으로 등록 가능하며, 대댓글은 익명으로 등록 가능합니다.
댓글 노출방식은
댓글 명예자문위원(팜-코니언-필기모양 아이콘)으로 위촉된 데일리팜 회원의 댓글은 ‘게시판형 보기’와 ’펼쳐보기형’ 리스트에서 항상 최상단에 노출됩니다. 새로운 댓글을 올리는 일반회원은 ‘게시판형’과 ‘펼쳐보기형’ 모두 팜코니언 회원이 쓴 댓글의 하단에 실시간 노출됩니다.
댓글의 삭제 기준은
다음의 경우 사전 통보없이 삭제하고 아이디 이용정지 또는 영구 가입제한이 될 수도 있습니다.
-
저작권·인격권 등 타인의 권리를 침해하는 경우
상용 프로그램의 등록과 게재, 배포를 안내하는 게시물
타인 또는 제3자의 저작권 및 기타 권리를 침해한 내용을 담은 게시물
-
근거 없는 비방·명예를 훼손하는 게시물
특정 이용자 및 개인에 대한 인신 공격적인 내용의 글 및 직접적인 욕설이 사용된 경우
특정 지역 및 종교간의 감정대립을 조장하는 내용
사실 확인이 안된 소문을 유포 시키는 경우
욕설과 비어, 속어를 담은 내용
정당법 및 공직선거법, 관계 법령에 저촉되는 경우(선관위 요청 시 즉시 삭제)
특정 지역이나 단체를 비하하는 경우
특정인의 명예를 훼손하여 해당인이 삭제를 요청하는 경우
특정인의 개인정보(주민등록번호, 전화, 상세주소 등)를 무단으로 게시하는 경우
타인의 ID 혹은 닉네임을 도용하는 경우
-
게시판 특성상 제한되는 내용
서비스 주제와 맞지 않는 내용의 글을 게재한 경우
동일 내용의 연속 게재 및 여러 기사에 중복 게재한 경우
부분적으로 변경하여 반복 게재하는 경우도 포함
제목과 관련 없는 내용의 게시물, 제목과 본문이 무관한 경우
돈벌기 및 직·간접 상업적 목적의 내용이 포함된 게시물
게시물 읽기 유도 등을 위해 내용과 무관한 제목을 사용한 경우
-
수사기관 등의 공식적인 요청이 있는 경우
-
기타사항
각 서비스의 필요성에 따라 미리 공지한 경우
기타 법률에 저촉되는 정보 게재를 목적으로 할 경우
기타 원만한 운영을 위해 운영자가 필요하다고 판단되는 내용
-
사실 관계 확인 후 삭제
저작권자로부터 허락받지 않은 내용을 무단 게재, 복제, 배포하는 경우
타인의 초상권을 침해하거나 개인정보를 유출하는 경우
당사에 제공한 이용자의 정보가 허위인 경우 (타인의 ID, 비밀번호 도용 등)
※이상의 내용중 일부 사항에 적용될 경우 이용약관 및 관련 법률에 의해 제재를 받으실 수도 있으며, 민·형사상 처벌을 받을 수도 있습니다.
※위에 명시되지 않은 내용이더라도 불법적인 내용으로 판단되거나 데일리팜 서비스에 바람직하지 않다고 판단되는 경우는 선 조치 이후 본 관리 기준을 수정 공시하겠습니다.
※기타 문의 사항은 데일리팜 운영자에게 연락주십시오. 메일 주소는 dailypharm@dailypharm.com입니다.
- [Reporter’s View] Medical Devices Act binds payment within 6 months
- Reporter's view | Hwang, byoung woo
- "Vabysmo PFS shifts the retinal disease treatment persistence·efficiency"
- Reporter's view | Son, Hyung Min







